Clear Sky Science · fr
L’édition de bases de PIK3CD adaptée aux CAR renforce la puissance anti-tumorale des lymphocytes T
Reprogrammer les cellules combattantes du cancer
La thérapie par lymphocytes T à récepteur antigénique chimérique (CAR) a transformé le traitement de certains cancers du sang, mais de nombreux patients rechutent ou ne répondent jamais. Un problème clé est que ces cellules immunitaires modifiées peuvent s’épuiser ou ne pas persister suffisamment longtemps dans l’organisme. Cette étude pose une question simple mais puissante : au lieu de repenser complètement les CAR, et si l’on « réaccordait » subtilement le câblage interne des lymphocytes T pour qu’ils conservent leur puissance plus longtemps, et ce de manière sûre ?
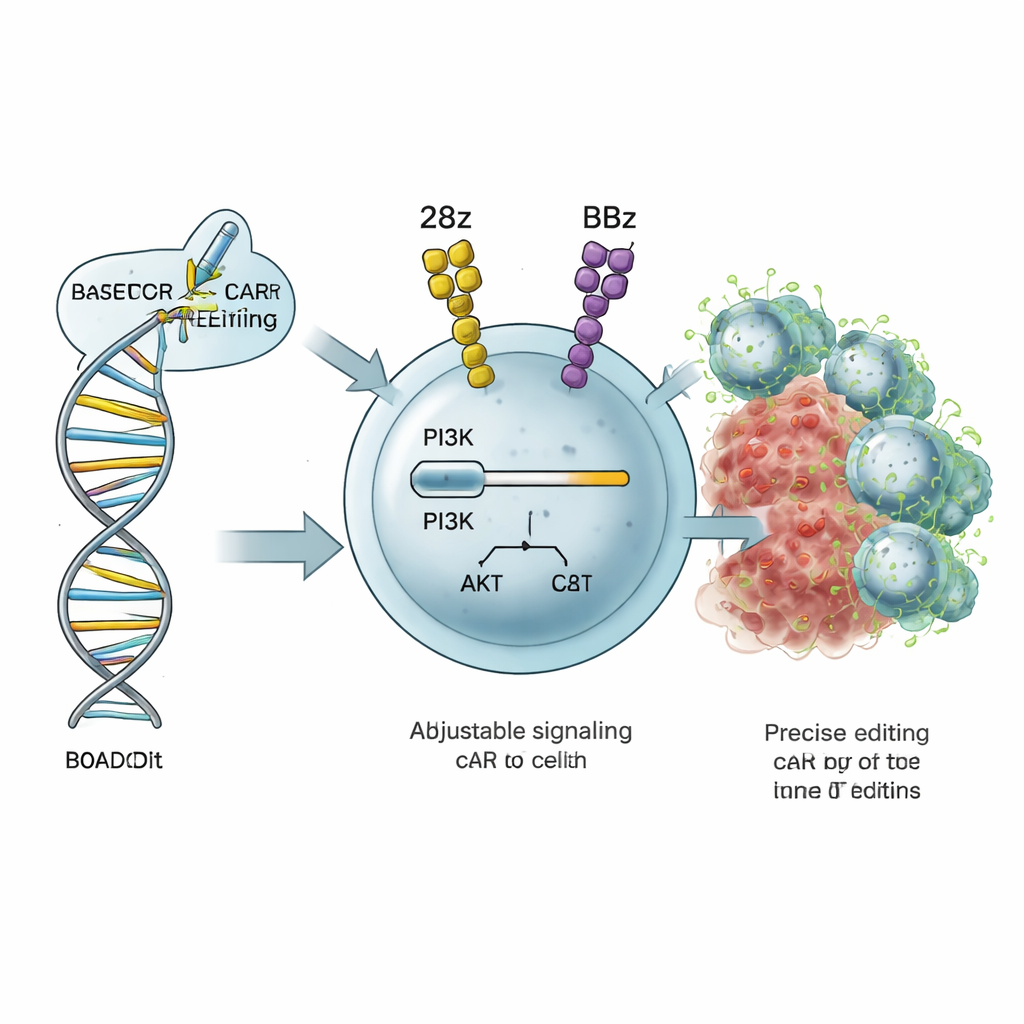
Viser le potentiomètre du lymphocyte T
Les lymphocytes T tueurs de cancer reposent sur des circuits de signalisation internes qui leur indiquent l’intensité d’activation, la vitesse de division et s’ils doivent devenir des effecteurs à courte durée de vie ou des cellules mémoire durables. Un circuit majeur est la voie PI3K–AKT, dans laquelle une protéine appelée PI3Kδ — codée par le gène PIK3CD — joue un rôle d’« interrupteur de volume » pour l’activation et le métabolisme. Les auteurs ont développé une stratégie qu’ils nomment ROADSTAR, qui utilise l’édition de bases, une forme très précise d’ingénierie génomique CRISPR, pour modifier des « lettres » individuelles dans PIK3CD. Plutôt que d’activer ou d’éteindre complètement la voie, ROADSTAR recherche de petites mutations qui augmentent ou diminuent légèrement la signalisation de manière optimale pour le design CAR spécifique présent dans le lymphocyte T.
Découvrir des mutations utiles
L’équipe a construit une bibliothèque de 34 changements d’une seule lettre dans la région régulatrice de PIK3CD et les a introduits dans des lymphocytes T humains portant déjà l’un de deux designs CAR courants : 28z (basé sur la molécule CD28) et BBz (basé sur 4‑1BB). Ces CAR diffèrent dans la façon dont ils stimulent les lymphocytes T : le 28z tend à induire une attaque forte et rapide mais aussi l’épuisement, tandis que le BBz favorise une meilleure survie et mémoire mais peut être moins agressif. Les CAR T modifiés ont été soumis à un « test de résistance » en les exposant de façon répétée à des cellules leucémiques. Grâce au séquençage profond, les chercheurs ont suivi quelles mutations permettaient aux CAR T modifiés de surpasser leurs homologues non modifiés sur plusieurs semaines.
Deux mutations se sont clairement démarquées. Dans les CAR T BBz, un changement appelé E81K a légèrement augmenté l’activité de PI3Kδ, renforçant les signaux de la voie PI3K–AKT. Dans les CAR T 28z, un autre changement, L32P, a atténué l’activité de PI3Kδ. La modélisation structurelle suggère que les deux modifications altèrent subtilement l’interaction de PI3Kδ avec son partenaire régulateur, modulant la force du signal plutôt que l’allumer ou l’éteindre complètement. Fait important, la mutation bénéfique pour un design CAR n’était pas la même que pour l’autre, soulignant que chaque architecture CAR exige un réglage interne optimal propre.
Des CAR T plus fortes, plus aptes et plus durables
Lorsque les éditions prometteuses ont été testées individuellement, E81K a rendu les CAR T BBz plus activées face aux cellules tumorales, meilleures en prolifération et nettement plus efficaces pour éliminer les cibles cancéreuses, y compris celles exprimant de faibles niveaux d’antigène. Ces cellules ont évolué en lymphocytes T mémoire effecteurs combinant une puissance de destruction robuste et la capacité de persister. Dans des modèles murins de leucémie et de neuroblastome métastatique, les CAR T BBz édités E81K ont contrôlé les tumeurs de façon plus complète et pendant beaucoup plus longtemps que les cellules BBz non éditées, résistant même à plusieurs reprises aux rechallenges tumoraux. Des profils transcriptomiques et métaboliques en cellule unique détaillés ont montré que les cellules E81K présentaient une fonction mitochondriale améliorée, une réserve respiratoire et glycolytique plus élevée et moins de signes d’épuisement — en somme, elles étaient plus énergiques et résilientes.
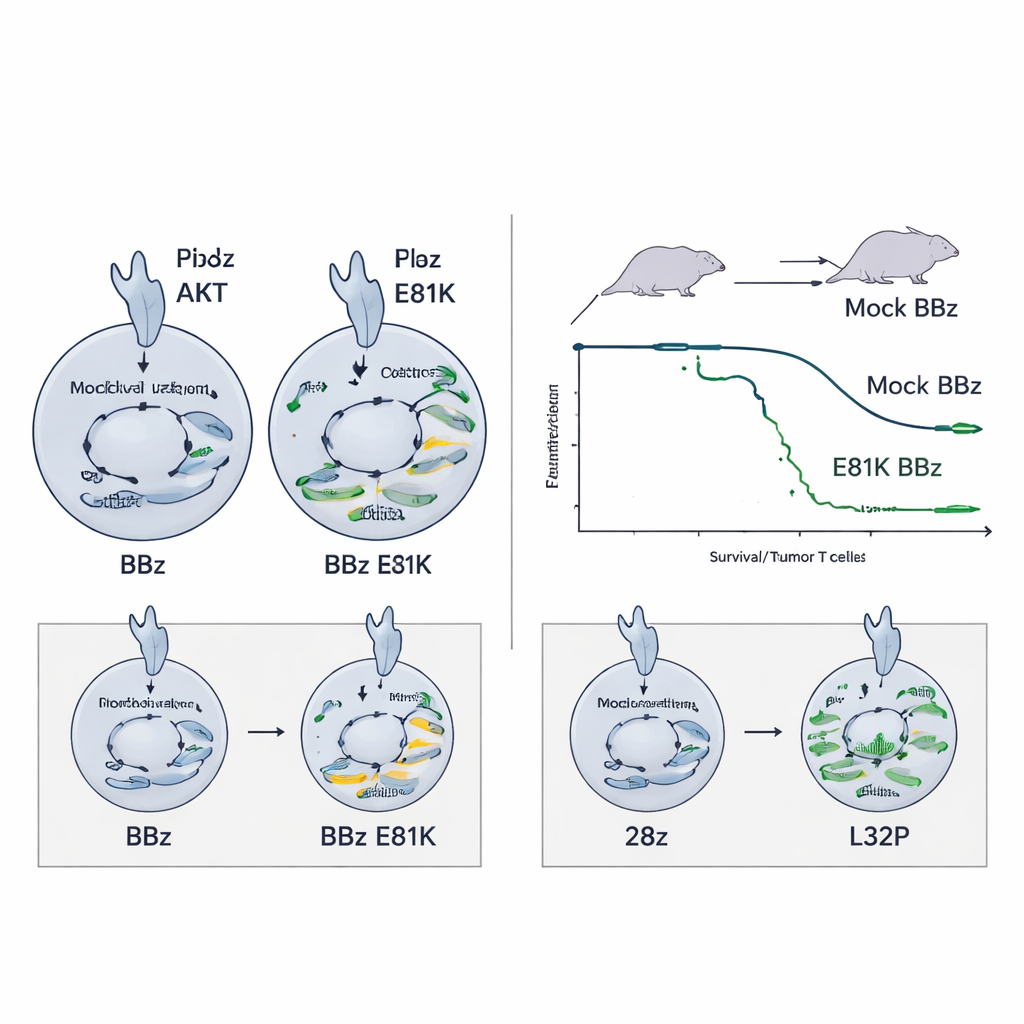
Prévenir l’épuisement dans des CAR très actifs
Le même renforcement par E81K n’a pas aidé — et pouvait même nuire — aux CAR T 28z, qui signalent déjà fortement. Dans ce contexte, une activité PI3K supplémentaire augmentait les marqueurs d’épuisement sans améliorer la fonction. La mutation L32P s’est avérée mieux adaptée : en réduisant modestement la signalisation PI3K–AKT, les CAR T 28z édités L32P montraient une activation basale diminuée tout en conservant une forte capacité cytotoxique et en proliférant davantage au fil du temps. Ils maintenaient également un état moins différencié, proche d’une mémoire, incluant un pool de mémoire de type cellule souche supposé soutenir des réponses à long terme. Dans un modèle exigeant de neuroblastome, les CAR T 28z modifiés L32P ont amélioré la survie par rapport à leurs homologues non édités.
Sécurité et promesse future
Une préoccupation centrale quant à la modification permanente de la signalisation immunitaire est le risque de croissance incontrôlée ou de cancers secondaires. Les auteurs ont donc réalisé des contrôles de sécurité étendus. Les CAR T BBz édités E81K ne proliféraient pas anormalement en culture, n’ont pas provoqué de lésions d’organes ni de crises inflammatoires chez la souris et n’ont montré aucun signe de lymphome ou d’invasion tissulaire des mois après perfusion. Les bases de données cliniques ne montrent pas non plus un enrichissement de ces mutations PIK3CD spécifiques dans les leucémies T. Dans l’ensemble, ce travail démontre que des éditions génomiques de « lettre » choisies avec soin peuvent servir de boutons de réglage de précision pour le comportement des lymphocytes T — augmentant à la fois la puissance anti‑tumorale et la persistance tout en respectant la biologie propre à chaque CAR. L’approche ROADSTAR pourrait contribuer à concevoir la prochaine génération de thérapies CAR T, à la fois plus efficaces et plus fiables contre les hémopathies et, potentiellement, les tumeurs solides.
Citation: Bucher, P., Brückner, N., Kortendieck, J. et al. CAR-adapted PIK3CD base editing enhances T cell anti-tumor potency. Nat Cancer 7, 368–383 (2026). https://doi.org/10.1038/s43018-025-01099-7
Mots-clés: cellules CAR T, signalisation PI3K, édition de base, immunothérapie du cancer, métabolisme des lymphocytes T