Clear Sky Science · fr
Gliome diffus midline H3.3K27M d’apparition de novo dans des organoïdes du tronc cérébral humain pour disséquer la fonction des cellules CAR T anti‑GD2
Pourquoi cette étude sur le cancer cérébral infantile est importante
Le gliome diffus midline est l’un des cancers cérébraux les plus meurtriers chez l’enfant, touchant des très jeunes enfants au niveau du tronc cérébral et laissant peu d’options thérapeutiques efficaces pour les familles. Parce que ces tumeurs siègent profondément dans le cerveau et sont rarement opérées, les chercheurs disposent de peu de tissu à étudier et de peu de moyens sûrs pour tester de nouvelles thérapies. Cette étude construit un « mini‑tronc cérébral en boîte » réaliste et l’utilise pour observer pendant des semaines le comportement d’une immunothérapie prometteuse — les cellules CAR T anti‑GD2 — et comprendre pourquoi elle échoue parfois.
Construire un mini tronc cérébral en laboratoire
L’équipe a commencé par des cellules souches humaines et les a guidées, étape par étape, pour qu’elles croissent en organoïdes cérébraux tridimensionnels ressemblant à la région du tronc appelée le pont, où ces tumeurs apparaissent généralement. En synchronisant précisément les signaux de croissance, ils ont produit des organoïdes riches en mêmes types de cellules de soutien, ou glie, qui résident normalement dans cette zone. Des analyses génétiques détaillées ont montré que les types cellulaires et leur maturation suivaient des schémas observés au cours du développement cérébral humain précoce, en particulier les lignées gliales typiques du pont et de la moelle adjacente. Cela signifie que les organoïdes peuvent servir de contexte réaliste pour étudier l’apparition et la progression de ce cancer.
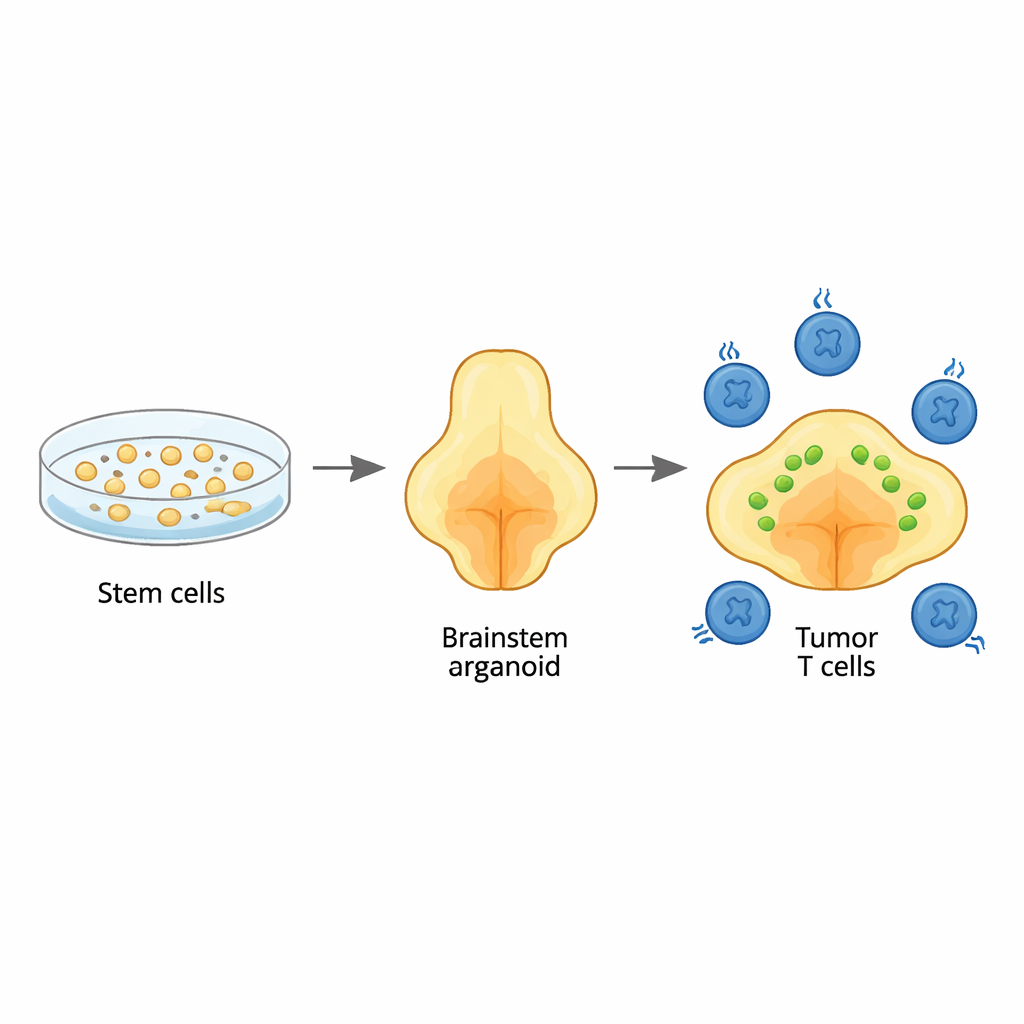
Recréer la tumeur de l’enfant à l’intérieur de l’organoïde
Pour imiter le gliome diffus midline, les chercheurs ont introduit trois altérations génétiques clés dans de jeunes organoïdes : une mutation emblématique d’une protéine histone (H3.3K27M), la perte du suppresseur de tumeur TP53 et une modification activatrice du récepteur de croissance PDGFRA. Lorsqu’elles sont introduites à un stade développemental très précoce, ces altérations transforment certaines cellules gliales en cellules cancéreuses. Les tumeurs qui en résultent se sont propagées de façon diffuse dans les organoïdes, comme elles le font dans les tronc cérébraux d’enfants, et présentaient les mêmes signatures larges d’ADN et d’ARN observées dans les tumeurs de patients. Le séquençage unicellulaire a révélé un mélange d’états cellulaires cancéreux, y compris des cellules gliales immatures spécifiques du pont équivalentes à celles trouvées dans les tumeurs pédiatriques réelles, soulignant que le modèle reproduit fidèlement la maladie humaine.
Observer les thérapies immunitaires combattre — et s’épuiser — au fil du temps
Avec ce modèle de tumeur dans un tronc cérébral, l’équipe a ajouté des cellules CAR T anti‑GD2 — des lymphocytes T de patients génétiquement modifiés pour reconnaître une molécule appelée GD2 à la surface des cellules tumorales — et a suivi la taille des tumeurs et le comportement des cellules T pendant jusqu’à un mois. Certains organoïdes ont montré une forte régression tumorale, d’autres un contrôle partiel seulement, reflétant les résultats mixtes observés en essais cliniques. Le séquençage ARN unicellulaire de plus de 20 000 cellules CAR T exposées aux tumeurs a mis au jour une diversité surprenante d’états des cellules T. Certaines étaient hautement cytotoxiques « tueur·euse·s », d’autres activées mais pas pleinement létales, et un groupe distinct présentait des signes d’épuisement, avec l’atténuation des gènes tueurs et une forte expression de freins inhibiteurs. Ces cellules épuisées ressemblaient aux lymphocytes T lassés observés lors d’infections chroniques et dans des tumeurs humaines, indiquant que le système d’organoïdes capture la fatigue des cellules T pertinente cliniquement, induite par un contact prolongé avec le cancer.
Trouver des cellules T puissantes mais de courte durée
En creusant plus loin, les chercheurs ont identifié un sous‑ensemble de cellules CAR T marqué par une protéine de surface appelée NCAM1, particulièrement efficaces comme tueuses à court terme. Lorsqu’elles étaient isolées et utilisées seules, ces cellules NCAM1‑positives contrôlaient les tumeurs plus fortement au début que leurs homologues NCAM1‑négatives. Cependant, elles s’épuisèrent aussi et diminuèrent plus rapidement, entraînant un contrôle affaibli au fil du temps. Ce compromis entre puissance immédiate et persistance aide à expliquer pourquoi les thérapies CAR T peuvent produire des réponses spectaculaires mais temporaires, et suggère que la présélection ou la reprogrammation des sous‑ensembles de cellules T pourrait optimiser la durabilité du traitement.
Comment les cellules immunitaires cérébrales peuvent réduire l’efficacité du traitement
Dans le cerveau réel, les tumeurs sont entourées non seulement de neurones et de glie, mais aussi de microglies, les cellules immunitaires résidentes du cerveau. Pour capturer cette couche de complexité, les scientifiques ont ajouté des microglies dérivées de cellules souches dans leurs organoïdes. Ces cellules ont maturé, adopté des morphologies et des profils d’expression génique spécifiques aux microglies observées dans le gliome diffus midline, et produit des molécules associées à un environnement immunosuppressif. Lorsque des cellules CAR T ont été ajoutées à des organoïdes porteurs de tumeur contenant des microglies, les cellules T ont basculé davantage vers des états épuisés et à faible effecteur, et le contrôle tumoral s’est détérioré. Parallèlement, des facteurs inflammatoires liés aux effets secondaires du traitement, tels que l’IL‑6, ont augmenté, suggérant que le modèle peut aussi aider à étudier les toxicités associées aux CAR T.
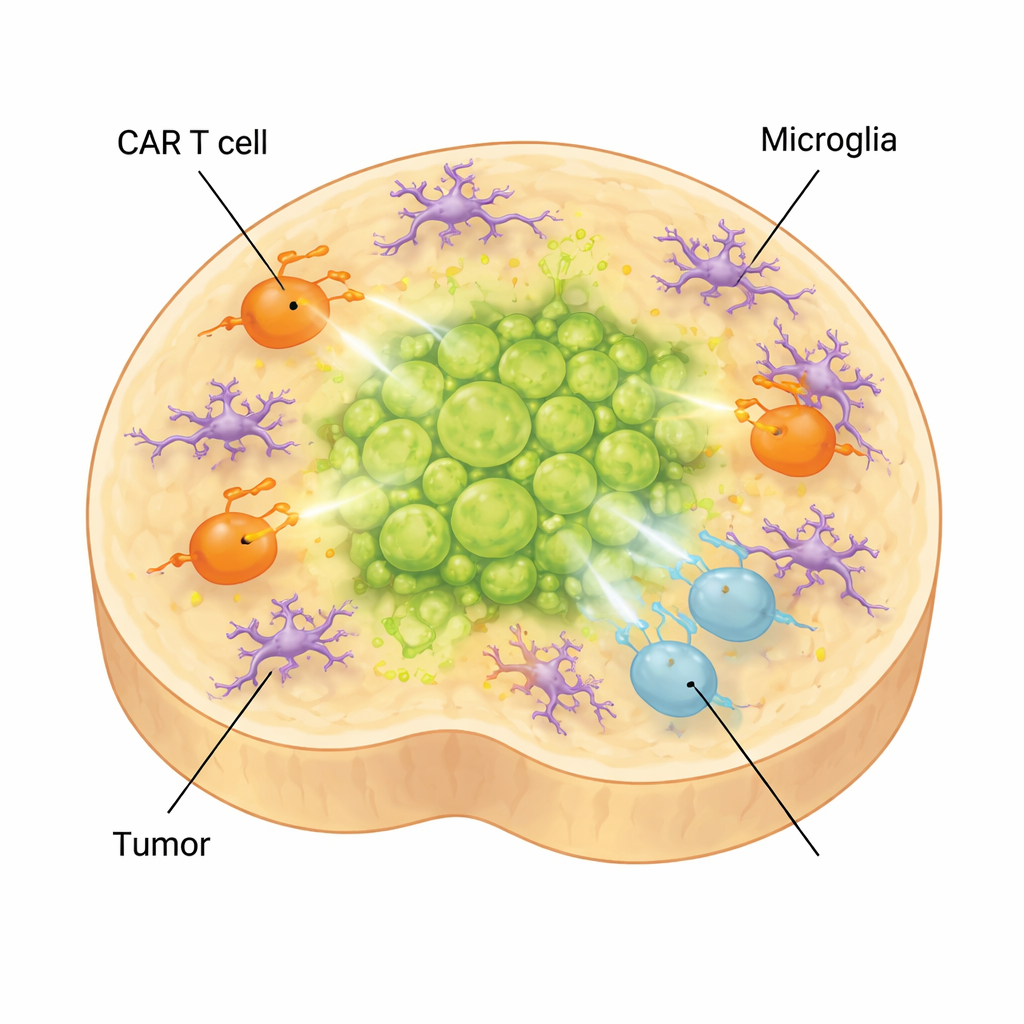
Ce que cela signifie pour les enfants atteints de ce cancer
Pour les familles confrontées au gliome diffus midline, ce travail n’offre pas encore de nouveau remède, mais il fournit un terrain d’essai puissant pour y parvenir plus rapidement. En recréant l’environnement du tronc cérébral de l’enfant et la tumeur dans une boîte, les scientifiques peuvent désormais observer, en temps réel, comment différents types de cellules tumorales, types de cellules CAR T et microglies interagissent sur des semaines. Cela leur permet d’identifier quelles cellules T génétiquement modifiées sont les plus efficaces, comment et quand elles s’épuisent, et comment les cellules immunitaires résidentes du cerveau sapent leurs efforts. En fin de compte, de tels modèles d’organoïdes pourraient être personnalisés pour des patients individuels et utilisés pour affiner les immunothérapies avant administration, augmentant les chances que de futures thérapies CAR T soient à la fois plus sûres et plus efficaces pour les enfants.
Citation: Bessler, N., Wezenaar, A.K.L., Ariese, H.C.R. et al. De novo H3.3K27M-altered diffuse midline glioma in human brainstem organoids to dissect GD2 CAR T cell function. Nat Cancer 7, 316–333 (2026). https://doi.org/10.1038/s43018-025-01084-0
Mots-clés: gliome diffus midline, organoïdes cérébraux, cellules CAR T, cancer cérébral pédiatrique, microglie