Clear Sky Science · fr
Prédire et interpréter les réponses aux médicaments spécifiques aux types cellulaires en régime de peu de données grâce à des priori inductifs
Pourquoi cette recherche compte pour les médicaments de demain
Lorsque l’on teste un nouveau médicament, l’une des grandes inconnues est la manière dont il affectera différemment les nombreux types cellulaires de notre corps. Un composé qui aide un type cellulaire peut n’avoir que peu d’effet sur un autre, voire être nocif. Générer expérimentalement ces informations pour des milliers de médicaments et d’innombrables types cellulaires est beaucoup trop lent et coûteux. Cet article présente une approche informatique, appelée PrePR-CT, qui apprend à prédire comment des types cellulaires individuels réagissent aux médicaments, même lorsque les données disponibles sont limitées. Ce travail ouvre la voie à des méthodes plus rapides, moins coûteuses et plus précises pour explorer in silico des candidats-médicaments avant d’engager des études de laboratoire et cliniques onéreuses.
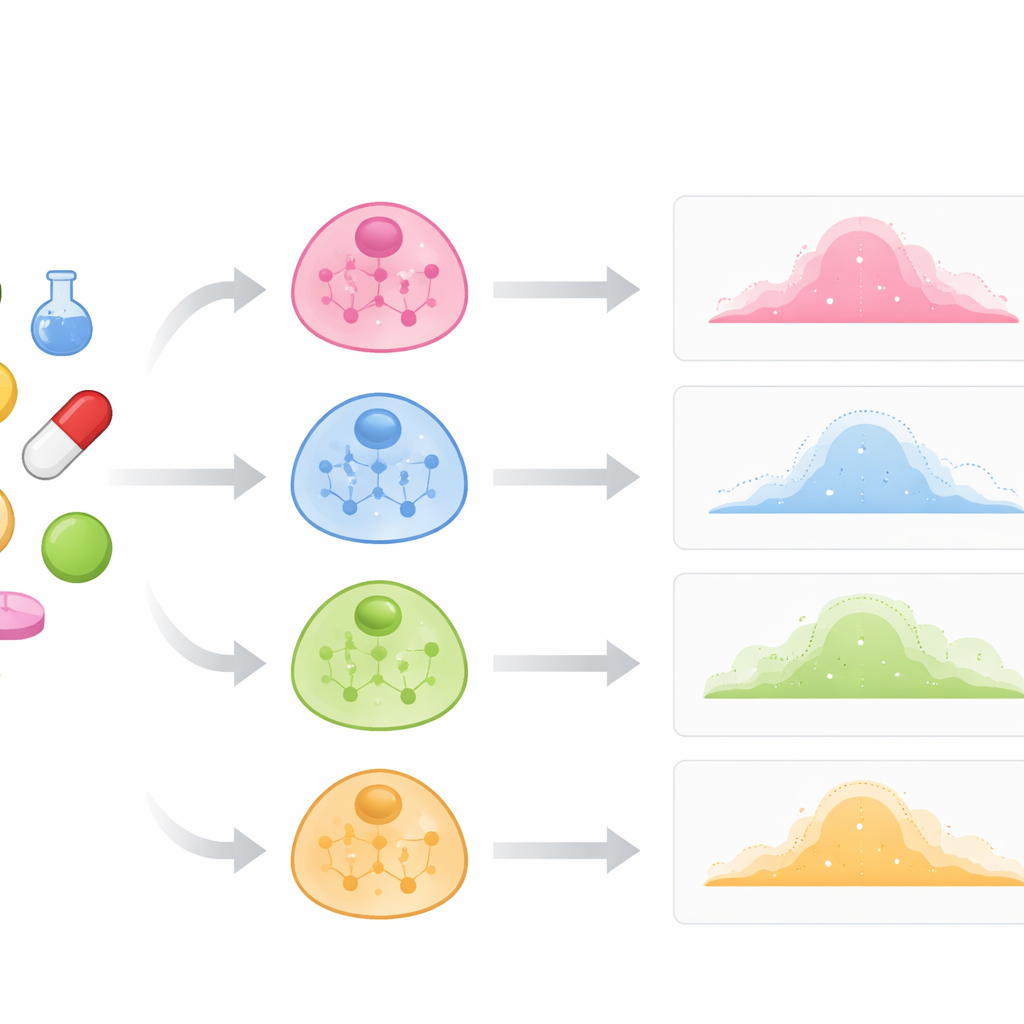
Regarder à l’intérieur des cellules plutôt que seulement les médicaments
Les criblages médicamenteux traditionnels traitent souvent les cellules comme si elles étaient toutes identiques et se concentrent principalement sur des moyennes globales. En réalité, les cellules immunitaires, hépatiques ou tumorales peuvent réagir très différemment au même composé. Les auteurs soutiennent que, pour prédire ces différences, un modèle doit comprendre l’organisation interne de chaque type cellulaire : quelles gènes ont tendance à s’activer ensemble et comment ces motifs définissent l’identité de la cellule. Ils construisent des « cartes » de types cellulaires en examinant quels gènes, dans des cellules non perturbées (contrôle), augmentent et diminuent de concert. Chaque carte est représentée comme un réseau, où les nœuds représentent des gènes et les liens reflètent une forte co-activité. Ces réseaux servent de connaissances a priori sur la manière dont un type cellulaire est structuré avant l’ajout de tout médicament.
Un moteur d’apprentissage conscient des réseaux
PrePR-CT combine trois éléments : le réseau d’activité génique d’un type cellulaire, l’expression génique de base de ce type cellulaire et une description compacte de la structure chimique du médicament. Le modèle utilise une classe de réseaux neuronaux conçus pour les graphes afin d’ingérer le réseau génique de la cellule et d’extraire un résumé capturant ses motifs caractéristiques. En parallèle, il convertit chaque médicament en une empreinte numérique dérivée de sa structure moléculaire. Ces éléments sont introduits dans un module de prédiction en aval qui apprend, à partir des expériences disponibles, comment un médicament donné va modifier la distribution d’activité génique dans ce type cellulaire. Plutôt que de produire un unique nombre par gène, la méthode estime à la fois le changement moyen et la variabilité de la réponse entre cellules individuelles, ce qui est crucial pour comprendre tant les effets subtils que les effets forts.
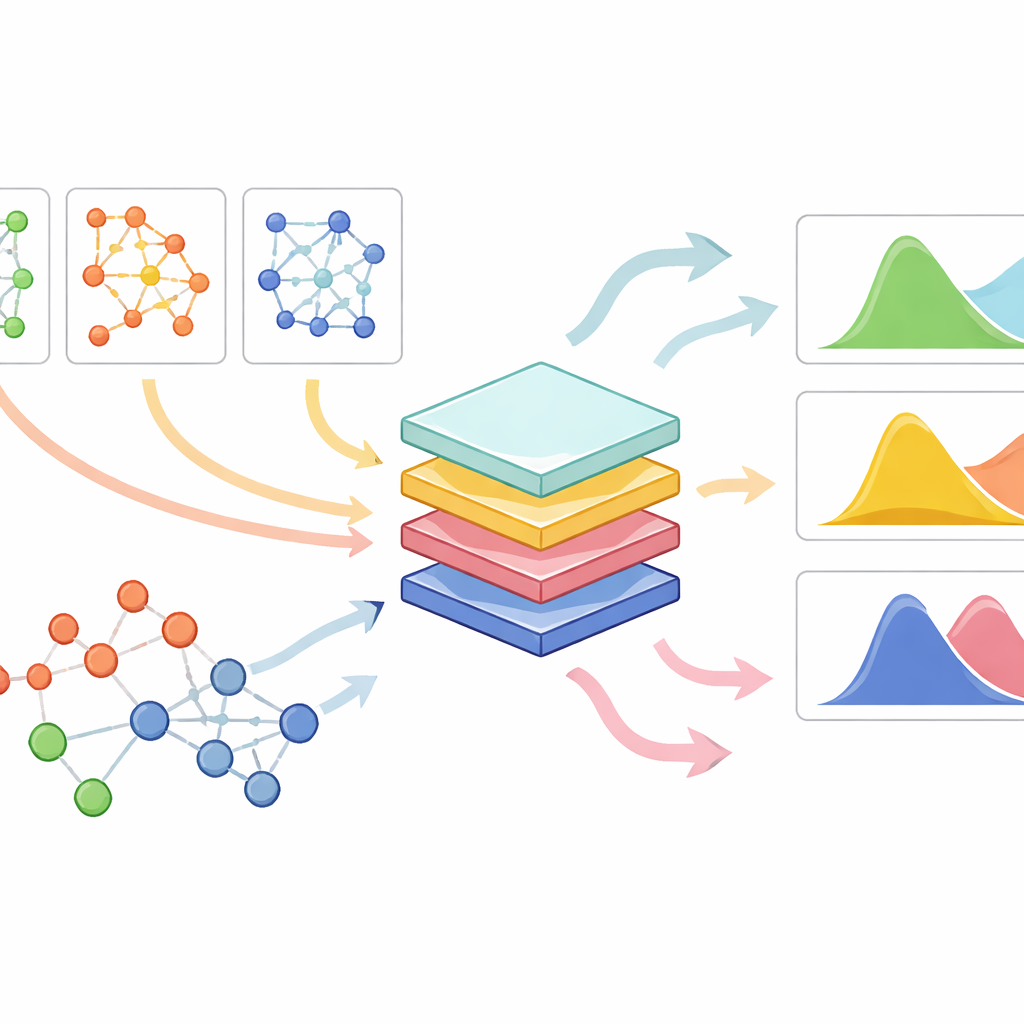
Fonctionner à travers de nombreux types cellulaires, médicaments et petits jeux de données
Les chercheurs ont testé PrePR-CT sur une large collection de jeux de données, y compris des cellules sanguines humaines exposées à des signaux immunitaires, plusieurs lignées cellulaires cancéreuses traitées par divers composés, des cellules hépatiques de souris exposées à un polluant et des criblages médicamenteux à grande échelle issus de ressources publiques. Dans des scénarios difficiles où un type cellulaire entier était exclu de l’entraînement, le modèle a quand même pu prédire comment ce nouveau type cellulaire réagirait à un médicament connu, souvent avec une précision supérieure à celle de modèles génératifs antérieurs. De même, lorsqu’un nouveau médicament mais un type cellulaire familier étaient exclus, la méthode a anticipé son impact en n’utilisant que son empreinte chimique. Fait important, le modèle restait performant lorsqu’il était entraîné sur des nombres relativement faibles de cellules, un contexte où de nombreuses approches d’apprentissage profond peinent.
Du « boîte noire » à des indices sur le mécanisme
Au-delà de la simple prédiction, les auteurs voulaient savoir si leur modèle pouvait fournir des indications sur les gènes et voies qui pilotent la réponse d’une cellule. L’architecture basée sur les graphes inclut un mécanisme d’attention qui met en évidence les gènes que le modèle juge particulièrement influents pour chaque type cellulaire. Beaucoup de ces gènes à « forte attention » n’étaient pas les suspects habituels identifiés par l’analyse classique d’expression différentielle, et pourtant ils se regroupaient dans des voies liées au système immunitaire, cohérentes avec la biologie des médicaments testés. Lorsque les chercheurs ont délibérément perturbé ces gènes influents dans l’entrée du modèle, la qualité des prédictions a chuté, notamment pour les gènes les plus réactifs, ce qui suggère que les scores d’attention pointent vers des acteurs mécanistiques significatifs plutôt que du bruit.
Ce que cela signifie pour concevoir de meilleurs médicaments
En termes simples, ce travail montre que fournir aux modèles d’intelligence artificielle une vue structurée de la manière dont chaque type cellulaire est câblé — son réseau génique interne — améliore grandement leur capacité à prévoir comment les médicaments vont remodeler ces cellules, même lorsque les données sont modestes. PrePR-CT ne remplace pas les expériences, mais il peut aider à restreindre les composés et types cellulaires qui valent la peine d’être testés et suggérer pourquoi certaines cellules réagissent ainsi. À mesure que les jeux de données s’enrichiront et que d’autres caractéristiques cellulaires seront intégrées, de telles approches pourraient devenir des outils clés pour adapter les thérapies à des tissus ou types cellulaires de patients spécifiques, réduisant les tâtonnements en laboratoire et rapprochant des médicaments plus précis de la réalité.
Citation: Alsulami, R., Lehmann, R., Khan, S.A. et al. Predicting and interpreting cell-type-specific drug responses in the small-data regime using inductive priors. Nat Mach Intell 8, 461–473 (2026). https://doi.org/10.1038/s42256-026-01202-2
Mots-clés: prédiction de la réponse aux médicaments, transcriptomique unicellulaire, réseaux neuronaux graphiques, découverte de médicaments, spécificité par type cellulaire