Clear Sky Science · fr
Les acides gras favorisent la respiration découplée via les transporteurs ATP/ADP dans les adipocytes blancs
Pourquoi les cellules graisseuses peuvent aider à brûler de l’énergie
La plupart des gens considèrent la graisse corporelle comme une réserve passive de calories. Cette étude révèle un côté étonnamment actif des cellules adipeuses blanches : dans certaines conditions, elles peuvent gaspiller des carburants et produire de la chaleur. En découvrant un nouveau mécanisme par lequel les cellules graisseuses laissent « fuir » de l’énergie, ce travail ouvre des pistes pour aider l’organisme à brûler plus de calories et, potentiellement, lutter contre l’obésité.
Quand la graisse stockée redevient carburant
Au quotidien, les adipocytes blancs passent une grande partie de leur temps à stocker de l’énergie sous forme de triglycérides—de grosses gouttelettes lipidiques. Lors d’exercice, de jeûne ou d’exposition au froid, des signaux de stress déclenchent la dégradation de ces triglycérides, processus appelé lipolyse, qui libère des acides gras et du glycérol. Les chercheurs ont confirmé que lorsque la lipolyse est stimulée dans des adipocytes blancs cultivés en laboratoire, ces cellules augmentent fortement leur consommation d’oxygène, signe que leurs centrales énergétiques, les mitochondries, travaillent davantage. Bloquer la première étape de la lipolyse arrêtait à la fois la libération d’acides gras et l’augmentation de la consommation d’oxygène, montrant que ce phénomène dépend bien des acides gras eux-mêmes.
Les acides gras libres comme interrupteurs d’activation de la combustion énergétique
Les acides gras libérés par l’adipocyte ne quittent pas tous le tissu ; certains restent à l’intérieur. L’équipe a montré que ces acides gras libres résiduels jouent un rôle clé pour augmenter l’activité mitochondriale. Lorsqu’une protéine du milieu de culture a été utilisée pour capter les acides gras, les cellules ont libéré plus de lipides au total mais leur consommation d’oxygène a diminué, indiquant que des niveaux élevés d’acides gras intracellulaires—et pas seulement la lipolyse en elle-même—sont responsables de la respiration supplémentaire. À l’inverse, bloquer la reformation des triglycérides, une voie qui reconditionne normalement les acides gras, augmentait la consommation d’oxygène et abaissait encore davantage la différence de potentiel électrique à travers la membrane mitochondriale. Ensemble, ces résultats suggèrent que les acides gras libres poussent les mitochondries vers un état « poreux » et énergétiquement gaspilleur.
Un nouvel acteur dans la respiration productrice de chaleur
Dans le tissu adipeux brun, producteur de chaleur classique, une protéine appelée UCP1 crée des passages dans la barrière mitochondriale pour que l’énergie des nutriments soit libérée sous forme de chaleur plutôt que stockée sous forme d’ATP. Les adipocytes blancs possèdent peu ou pas d’UCP1, aussi les auteurs ont-ils cherché une autre voie. Ils se sont intéressés au transporteur ATP/ADP, une protéine d’échange qui transporte normalement la monnaie énergétique de la cellule à travers la membrane mitochondriale. En utilisant à la fois un bloqueur chimique spécifique et des outils génétiques pour réduire l’expression de ce transporteur, ils ont montré qu’il est nécessaire au « leak » induit par les acides gras : bloquer le transporteur préservait la différence de potentiel mitochondriale et empêchait l’augmentation de la consommation d’oxygène pendant la lipolyse, alors même que la lipolyse se déroulait normalement. Cela suggère que les acides gras libres agissent de concert avec ce transporteur pour créer une fuite contrôlée de protons à travers la membrane mitochondriale, déclenchant la respiration découplée.
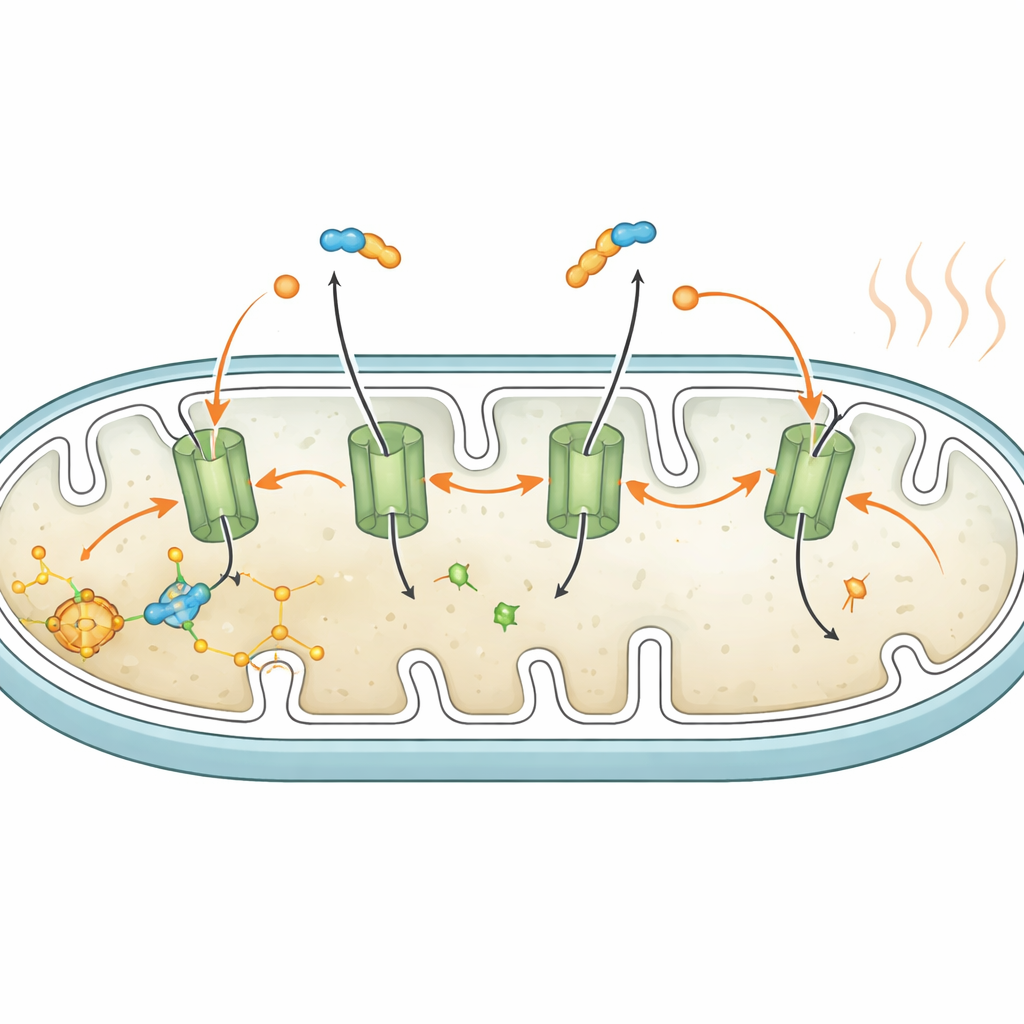
De la culture cellulaire à l’animal vivant
Pour tester si cette fuite énergétique a un impact chez l’animal entier, les chercheurs ont utilisé des souris dont la protéine de signalisation STAT3 avait été supprimée spécifiquement dans les cellules adipeuses. Ces animaux effectuent la lipolyse normalement mais présentent une respiration induite par les acides gras réduite dans leur tissu adipeux blanc. Dans des conditions d’élevage standard, où la graisse brune est active et assure la plupart de la défense contre le froid, ces souris restaient aussi chaudes que leurs congénères. En revanche, lorsque les souris devenaient obèses et étaient maintenues à une température où la graisse brune est largement inactive, les animaux dépourvus de STAT3 dans leur tissu adipeux devenaient sensibles au froid et montraient une augmentation plus faible de la consommation d’oxygène globale lors d’une exposition au froid ou d’une lipolyse pharmacologique. De façon importante, des changements similaires n’étaient pas observés lorsque STAT3 était supprimé seulement dans la graisse brune, ce qui indique un rôle spécifique du tissu adipeux blanc.
Le tissu adipeux blanc, un chauffagiste caché
L’étude conclut que, dans les adipocytes blancs, les acides gras libres générés pendant la lipolyse active peuvent se lier au transporteur ATP/ADP des mitochondries et déclencher une fuite d’énergie qui produit de la chaleur plutôt que du carburant cellulaire utile. Chez les animaux obèses maintenus au chaud, cette respiration découplée dans le tissu adipeux blanc contribue de manière significative au maintien de la température corporelle et à la dépense énergétique globale, en particulier quand la graisse brune et les frissons musculaires sont limités. Parce que le tissu adipeux blanc est abondant chez l’adulte, surtout en cas d’obésité, stimuler modérément cette fuite pourrait offrir un nouveau moyen d’augmenter la dépense calorique quotidienne et d’appuyer des thérapies de perte de poids, à condition que cela puisse être réalisé en toute sécurité sans nuire aux autres tissus.
Citation: Ahmadian, M., Aksu, A.M., Dhillon, P. et al. Fatty acids promote uncoupled respiration via ATP/ADP carriers in white adipocytes. Nat Metab 8, 572–586 (2026). https://doi.org/10.1038/s42255-026-01467-2
Mots-clés: tissu adipeux blanc, acides gras, découplage mitochondrial, thermogenèse, obésité