Clear Sky Science · fr
PFKM régule les basculements métaboliques tout au long de la différenciation du muscle squelettique
Pourquoi les cellules musculaires ont besoin d’une gestion intelligente du sucre
Quand nous faisons de l’exercice ou que nous nous levons d’une chaise, nos muscles squelettiques se mettent en marche, brûlant du sucre pour alimenter chaque contraction. Mais les cellules souches musculaires immatures et les fibres musculaires complètement formées n’utilisent pas le sucre de la même façon. Cette étude révèle un système de commutation intégré — centré sur une seule enzyme appelée PFKM — qui décide si le glucose est brûlé pour produire de l’énergie immédiate ou redirigé pour protéger et reconstruire les cellules. Comprendre cet interrupteur pourrait ouvrir de nouvelles voies pour traiter la faiblesse musculaire, le vieillissement musculaire et les maladies métaboliques héréditaires.
Un feu tricolore pour le carburant cellulaire
Le glucose qui entre dans une cellule peut emprunter plusieurs itinéraires. Une voie majeure, la glycolyse, convertit rapidement le sucre en énergie et en éléments de construction pour les fibres musculaires en croissance. Une autre voie, la voie des pentoses phosphates, produit des molécules qui protègent les cellules contre le stress oxydatif et soutiennent la synthèse d’ADN et de lipides. Les chercheurs se sont concentrés sur PFKM, une isoforme musculaire de la phosphofructokinase‑1 située à un carrefour clé de la glycolyse. En mesurant des centaines de métabolites sur plusieurs minutes à heures après l’activation d’un signal de croissance appelé Wnt, ils ont observé que les intermédiaires précoces de la glycolyse s’accumulaient rapidement tandis que le produit de PFKM diminuait et que les métabolites de la voie des pentoses phosphates augmentaient. Cela suggère que les cellules freinaient activement PFKM pour détourner le sucre vers une chimie protectrice plutôt que vers la production pure d’énergie. 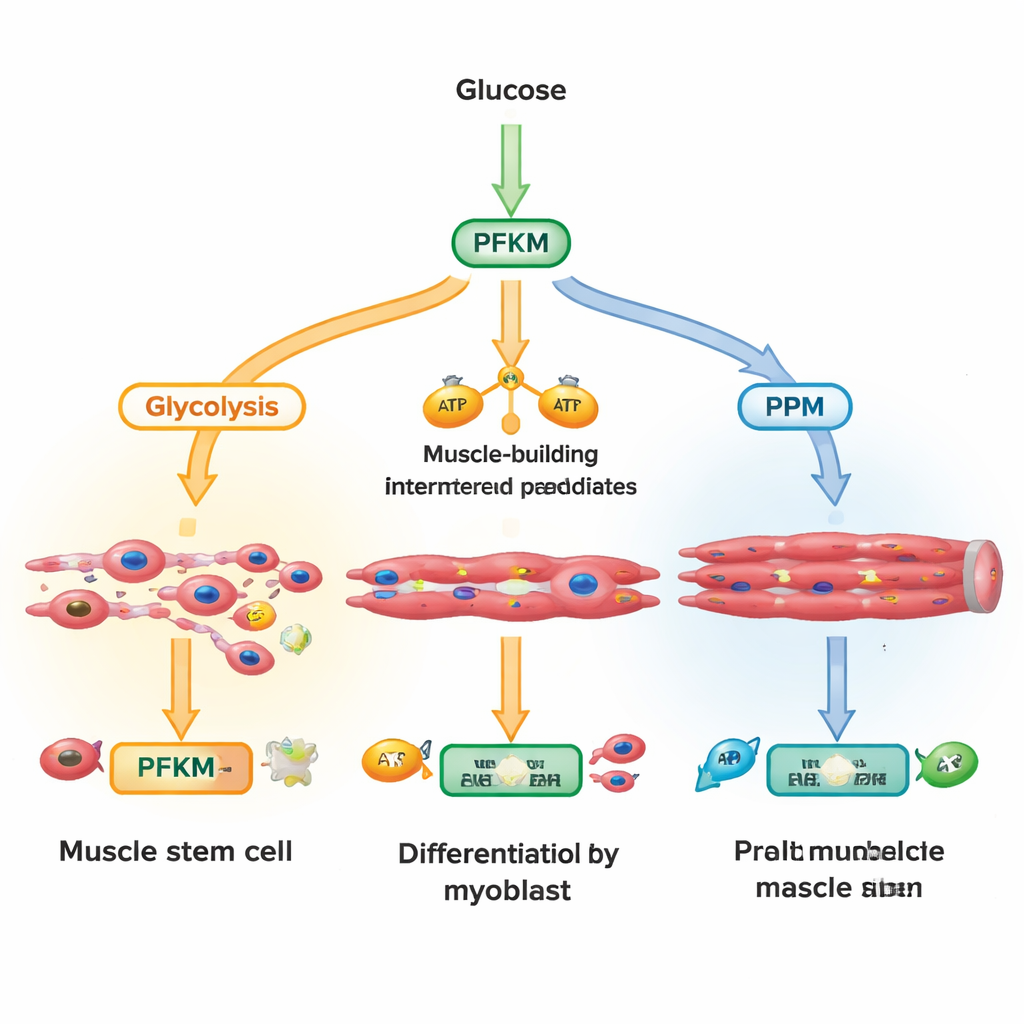
Étiqueter et éliminer l’enzyme gardienne
Pour comprendre comment PFKM est contrôlée, l’équipe a suivi la localisation de la protéine dans les cellules. En conditions de repos, PFKM était répartie dans le cytoplasme. Quelques minutes après la stimulation par Wnt, elle se rassemblait en points lumineux qui chevauchaient les lysosomes, les compartiments cellulaires responsables du déchiquetage des protéines. Deux isoformes apparentées, PFKL et PFKP, ne changeaient ni de localisation ni de niveau, montrant que seule l’isoforme musculaire PFKM était ciblée. Des tests biochimiques ont montré que bloquer la fonction lysosomale empêchait la perte de PFKM, tandis qu’inhiber le protéasome — l’autre grand système d’élimination des protéines — n’avait aucun effet. L’analyse de la séquence a révélé un court motif unique à PFKM, un « degron » d’arginine méthylée. L’enzyme PRMT1 ajoutait une marque de méthylation sur une arginine de ce motif, et cette étiquette permettait à la machinerie de la microautophagie, y compris la protéine VPS4, d’entraîner PFKM vers les lysosomes pour dégradation. Désactiver PRMT1 ou VPS4 stabilisait PFKM et bloquait son élimination.
De la cellule souche à la fibre musculaire fonctionnelle
En utilisant de larges jeux de données unicellulaires humains, les auteurs ont cartographié les niveaux de PFKM à travers de nombreux types cellulaires musculaires. Les cellules souches musculaires, qui restent dormantes jusqu’à ce qu’on ait besoin d’elles pour la réparation, présentaient très peu de PFKM mais exprimaient fortement les gènes de la voie des pentoses phosphates et des composants lysosomaux. À mesure que les cellules s’engageaient vers le destin musculaire et fusionnaient en fibres multinucléées, les transcrits et la protéine PFKM augmentaient fortement, tandis que les gènes cibles de Wnt et les gènes lysosomaux déclinaient. Dans des cultures de cellules musculaires humaines et murines, Wnt entraînait rapidement PFKM dans les lysosomes des cellules précoces à noyau unique mais pas dans les fibres matures multinucléées. Ce schéma soutient un modèle où les cellules indifférenciées maintiennent de faibles niveaux de PFKM — via la dégradation lysosomale — pour favoriser un métabolisme protecteur, puis réexpriment l’enzyme à mesure qu’elles basculent vers des fibres contractiles gourmandes en énergie.
Que se passe-t-il quand l’interrupteur reste bloqué
Pour tester l’importance de PFKM dans la formation du muscle, l’équipe a réduit ses niveaux par interférence ARN. Les cellules avec peu de PFKM avaient du mal à activer les gènes caractéristiques du muscle, produisaient moins de myosine et formaient moins de fibres multinucléées, plus petites, alors que le nombre global de cellules restait inchangé. Le profil métabolique a montré une diminution des intermédiaires glycolytiques en aval et des carburants du cycle des acides tricarboxyliques, mais une augmentation des gènes et marqueurs de la voie des pentoses phosphates, associée à une meilleure résistance au stress oxydatif. Fait important, l’apport de 3‑phosphoglycérate — un intermédiaire glycolytique situé normalement en aval de PFKM — a permis de sauver de nombreux défauts de différenciation. Les marqueurs musculaires et la formation de fibres ont rebondi, montrant que le manque de métabolites, plutôt que l’absence de la protéine PFKM elle‑même, constituait le principal goulot d’étranglement. 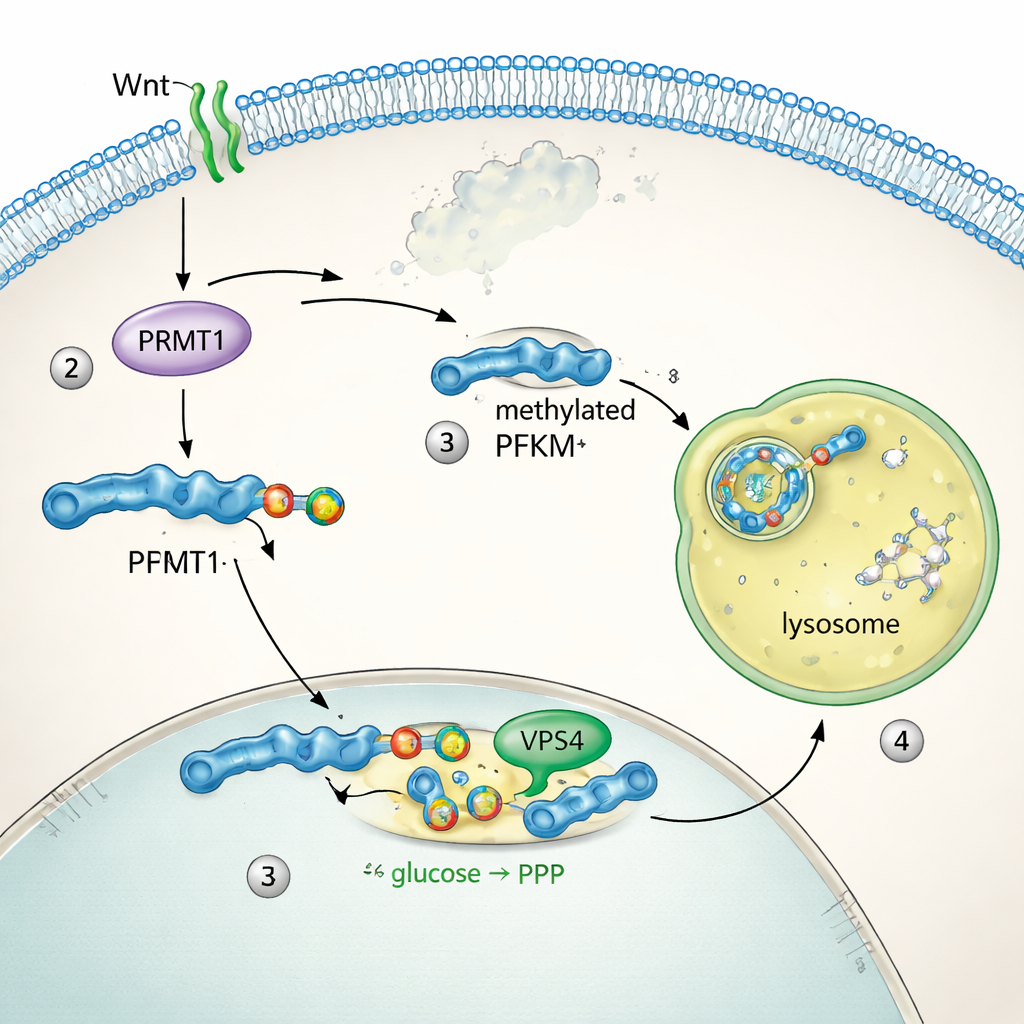
Implications pour la santé et la réparation musculaires
Pour un non‑spécialiste, le message central est que les cellules musculaires ne se contentent pas de « brûler du sucre » plus ou moins ; elles le réacheminent finement entre production d’énergie et protection cellulaire selon leur stade de vie. PFKM agit comme une vanne contrôlable à ce carrefour. Dans les cellules de type souche, l’étiquetage et la destruction lysosomale pilotés par Wnt redirigent le glucose vers une voie qui protège les cellules et les prépare à une croissance future. À mesure que les cellules mûrissent en fibres actives, elles reconstituent leurs réserves de PFKM et orientent le métabolisme vers une utilisation énergétique à haut rendement. Perturber cet équilibre, comme on le voit dans de rares troubles de carence en PFKM, compromet le développement musculaire normal. En dévoilant la poignée moléculaire de cet interrupteur, l’étude suggère que des thérapies futures pourraient ajuster finement la régénération musculaire ou protéger les muscles dans les maladies et le vieillissement en modulant légèrement l’activité de PFKM ou en fournissant les bons métabolites en aval.
Citation: Campos, M., Nguyen, S.T., Kong, X. et al. PFKM governs metabolic shifts throughout skeletal muscle differentiation. Nat Metab 8, 489–505 (2026). https://doi.org/10.1038/s42255-026-01457-4
Mots-clés: différenciation du muscle squelettique, métabolisme du glucose, enzyme PFKM, voie des pentoses phosphate, dégradation lysosomale des protéines