Clear Sky Science · fr
Expression ectopique de la DHODH cytosolique découplant la biosynthèse de novo des pyrimidines du transport d’électrons mitochondrial
Pourquoi rompre un lien caché dans nos cellules est important
Chaque cellule de votre corps doit constamment copier et réparer son ADN, un processus qui exige un apport régulier de « lettres » chimiques appelées pyrimidines. Chez la plupart des animaux, la synthèse de ces lettres est étroitement liée à la façon dont les mitochondries — les centrales énergétiques de la cellule — brûlent du carburant en utilisant l’oxygène. Ce couplage signifie que lorsque la respiration mitochondriale faiblit, les blocs de construction de l’ADN se raréfient et les cellules peinent à se développer. L’étude résumée ici montre qu’en empruntant un seul gène à la levure de boulanger, on peut découpler clairement ces deux processus. Cette modification génétique permet aux cellules de mammifères de continuer à fabriquer des lettres d’ADN même lorsque leurs mitochondries sont déficientes, ouvrant une nouvelle voie pour étudier — et peut‑être un jour traiter — des maladies liées à un métabolisme énergétique défaillant.
Un outil emprunté à la levure
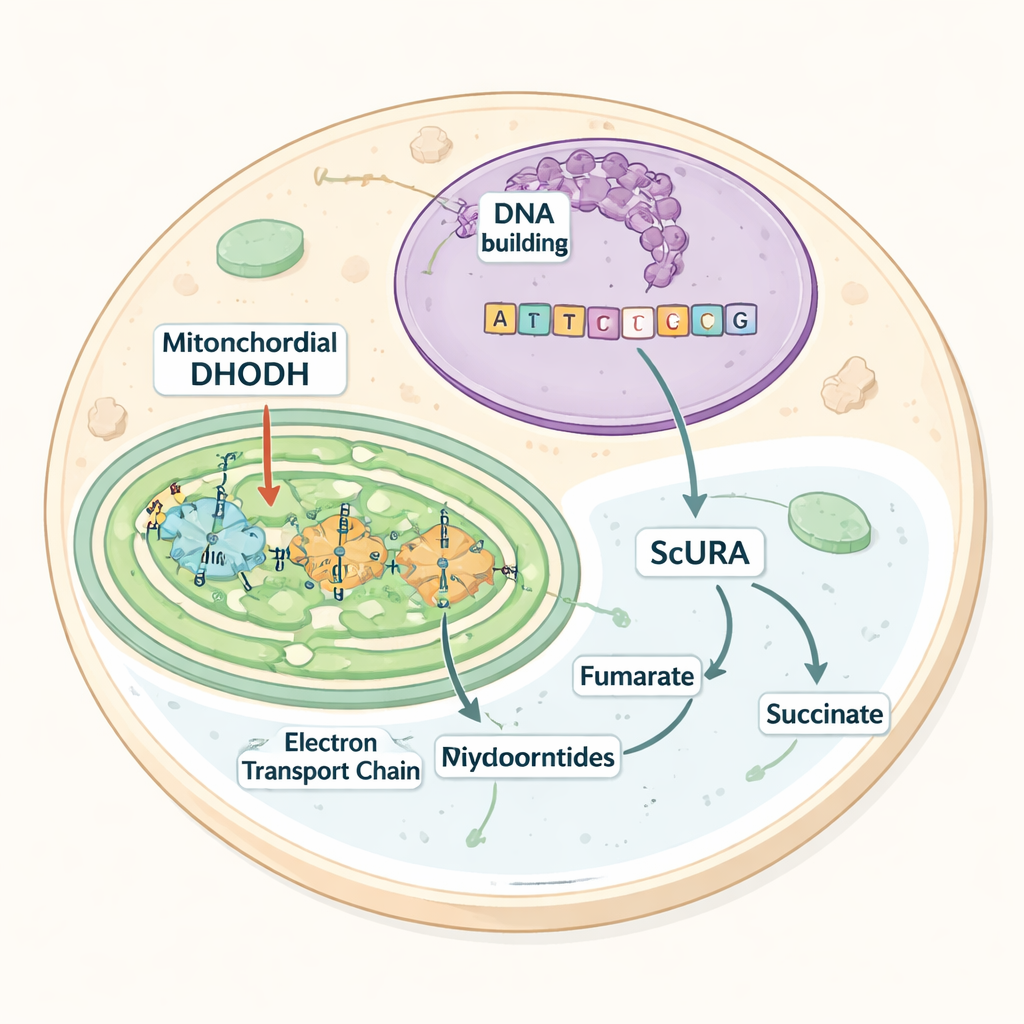
Le travail porte sur une enzyme appelée dihydroorotate déshydrogénase (DHODH), qui réalise une étape clé de la synthèse des pyrimidines. Chez les mammifères, la DHODH est située sur la membrane interne des mitochondries et transfère des électrons à une molécule porteuse qui alimente la chaîne respiratoire. Si ce flux d’électrons est bloqué — par exemple par des inhibiteurs pharmacologiques ou des défauts génétiques — la DHODH s’arrête, la production de pyrimidines s’interrompt et les cellules deviennent dépendantes de l’uridine alimentaire ou apportée. De nombreux microbes qui prospèrent sans oxygène évitent ce goulet d’étranglement en utilisant des versions alternatives de la DHODH qui flottent dans le cytosol et utilisent d’autres accepteurs d’électrons. Les auteurs se sont demandé s’il était possible d’installer une telle voie indépendante de l’oxygène dans des cellules de mammifère.
Reconfigurer la fabrication des lettres d’ADN
Les chercheurs ont introduit le gène URA1 de la levure Saccharomyces cerevisiae dans des cellules humaines. URA1 code pour une enzyme cytosolique, appelée ScURA, qui réalise la même étape chimique que la DHODH mitochondriale mais transfère les électrons à une molécule appelée fumarate au lieu du transporteur mitochondrial. Des tests biochimiques ont montré que ScURA formait des dimères actifs dans le cytosol et apportait une nouvelle activité DHODH résistante aux médicaments. Dans des conditions normales, l’ajout de ScURA ne perturbait ni la structure mitochondriale, ni la respiration, ni la croissance, ce qui indique qu’elle fonctionne comme une voie de secours plutôt que comme une charge supplémentaire.
Des cellules qui surmontent les obstacles mitochondriaux
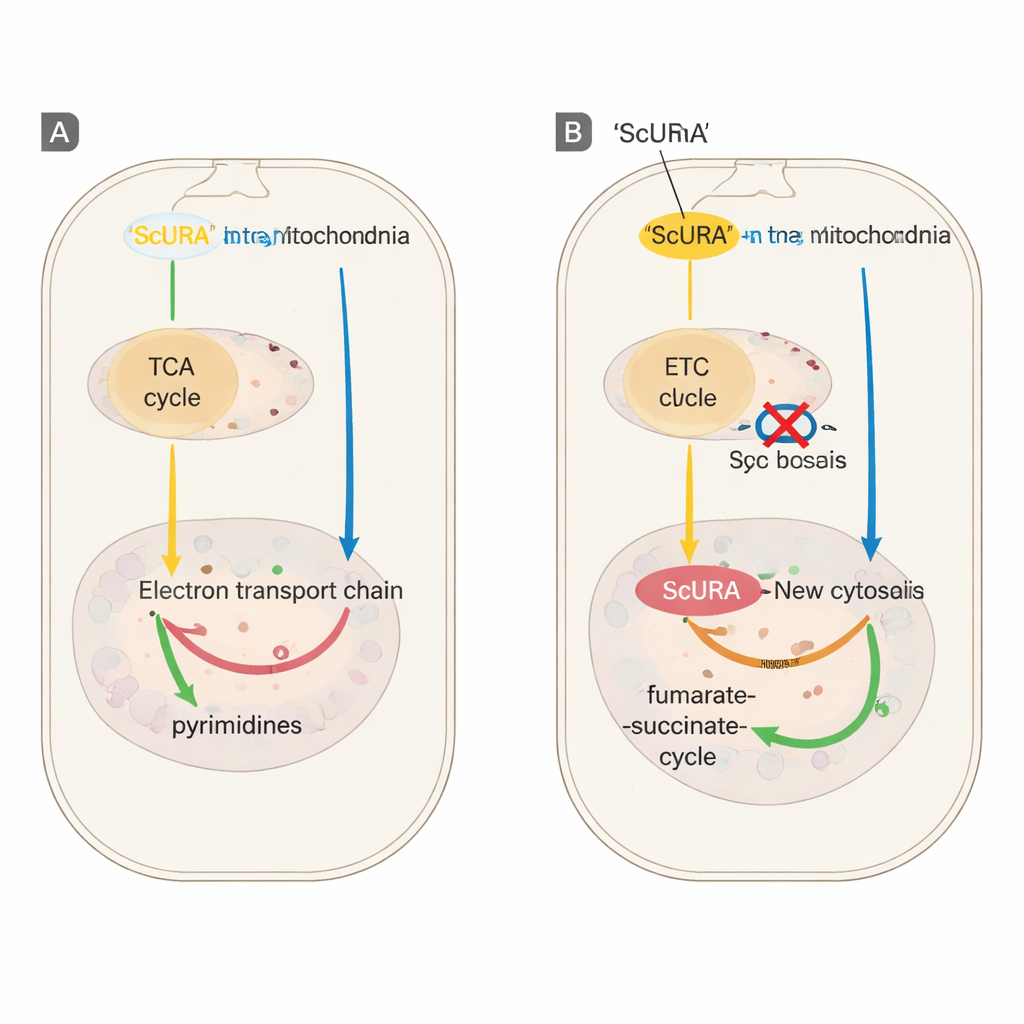
Pour vérifier si cette voie de secours pouvait remplacer le système natif, l’équipe a bloqué chimiquement soit la DHODH elle‑même soit la chaîne de transport d’électrons mitochondriale — traitements qui arrêtent normalement la division cellulaire sauf si de l’uridine est fournie. Les cellules exprimant ScURA ont continué à proliférer sans aide, même sous une forte inhibition du complexe III respiratoire ou après suppression génétique du gène DHODH endogène. Le suivi détaillé des atomes d’azote et de carbone provenant de glutamine marquée a montré que les cellules exprimant ScURA continuaient à synthétiser des nucléotides pyrimidiques malgré ces blocages. Les mesures de métabolites ont révélé que, au lieu d’accumuler des précurseurs toxiques, les cellules ScURA canalisaient les électrons vers le fumarate, produisant du succinate et remodelant subtilement le cycle des acides tricarboxyliques (TCA) pour soutenir une navette fumarate–succinate entre le cytosol et les mitochondries.
Sauver des cellules aux centrales énergétiques endommagées
Les auteurs ont ensuite testé ScURA dans des modèles cellulaires de maladie mitochondriale. Les cellules dépourvues d’ADN mitochondrial, ou porteuses de mutations qui compromettent les complexes III ou IV respiratoires, dépendent normalement d’uridine ajoutée pour croître. Une fois modifiées pour exprimer ScURA, ces cellules mutants divers ont pu proliférer sans uridine, bien qu’elles aient encore requis du pyruvate, reflétant un besoin subsistant d’une certaine activité mitochondriale. Au niveau de l’expression génique, ScURA a également empêché l’arrêt des gènes codant pour les protéines ribosomales qui suit habituellement une inhibition chronique du transport d’électrons, en maintenant des réserves de blocs de construction pyrimidiques suffisantes pour soutenir la production d’ARN.
Ce que cela signifie pour la santé et la maladie
En séparant clairement la synthèse des pyrimidines de la respiration mitochondriale, ScURA offre aux chercheurs un nouvel levier puissant : ils peuvent désormais se demander, dans de nombreux contextes, si un défaut donné ou l’effet d’un médicament provient réellement d’une perte de production d’énergie ou plutôt d’une pénurie de précurseurs d’ADN et d’ARN. À long terme, des stratégies similaires pourraient compléter les thérapies géniques existantes pour les troubles mitochondriaux, ou aider à expliquer pourquoi certaines tumeurs dépendent fortement de la restauration de leur fonction mitochondriale. Bien que la traduction d’une enzyme de levure en traitement humain nécessite une grande prudence, cette étude montre qu’un seul gène judicieusement choisi peut réécrire une connexion métabolique fondamentale que l’évolution a longtemps maintenue liée.
Citation: Curtabbi, A., Jaroszewicz, S.N., Sanz-Cortés, R. et al. Ectopic expression of cytosolic DHODH uncouples de novo pyrimidine biosynthesis from mitochondrial electron transport. Nat Metab 8, 454–466 (2026). https://doi.org/10.1038/s42255-026-01454-7
Mots-clés: métabolisme des pyrimidines, fonction mitochondriale, chaîne de transport d’électrons, réorganisation métabolique, maladie mitochondriale