Clear Sky Science · fr
Démêler les mécanismes moléculaires causaux du diabète de type 2 dans des populations mondiales et des tissus pertinents pour la maladie
Pourquoi comprendre les racines du diabète est important
Le diabète de type 2 touche des centaines de millions de personnes dans le monde, et pourtant nous ignorons encore, de façon surprenante, quels commutateurs moléculaires provoquent réellement la maladie plutôt que de simplement l’accompagner. Cette étude fouille en profondeur notre ADN et plusieurs organes pour identifier quels gènes et quelles protéines poussent effectivement la glycémie vers le diabète, et lesquels la protègent. En incluant des personnes d’ascendances diverses et en examinant plusieurs tissus clés, les chercheurs nous rapprochent de stratégies de prévention et de traitements plus précis susceptibles de fonctionner pour de nombreuses populations, pas seulement celles d’origine européenne.
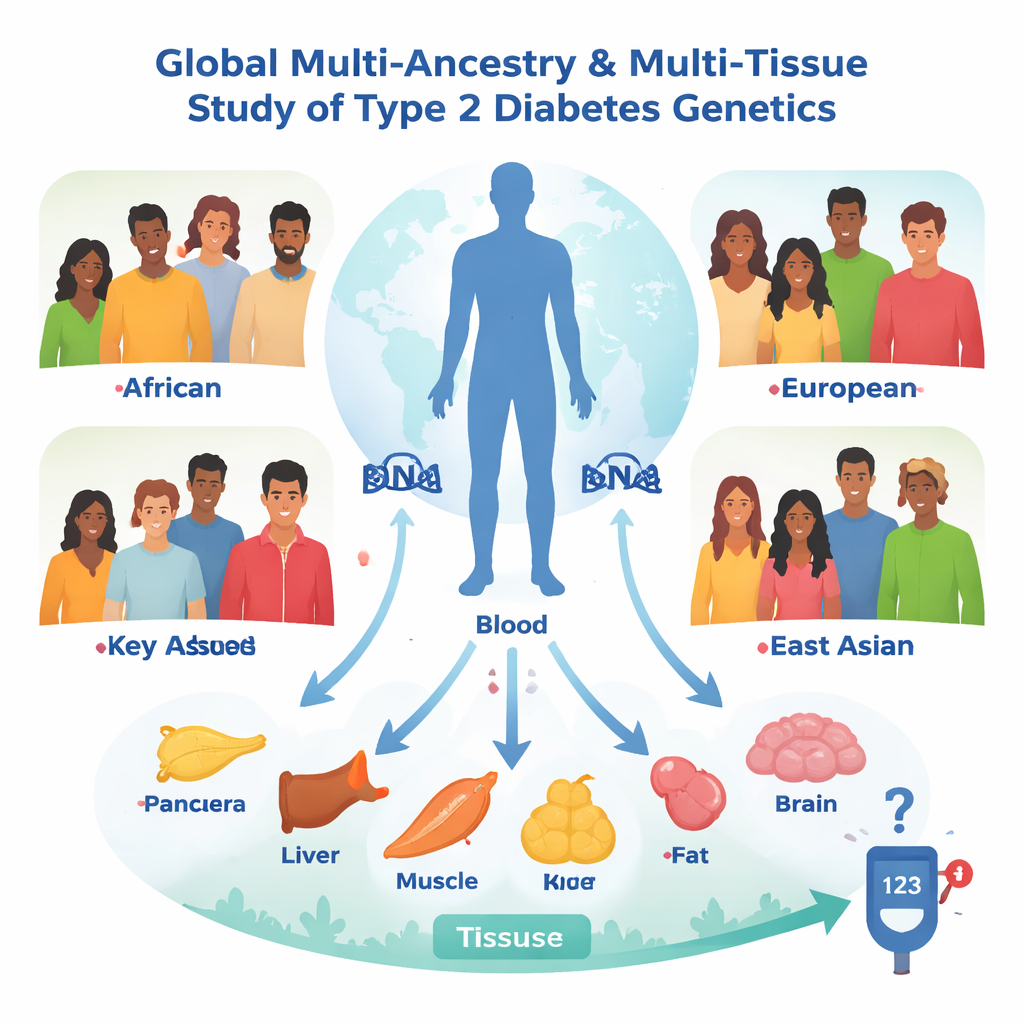
Regarder à l’échelle mondiale et à l’intérieur du corps
L’équipe a commencé avec des données génétiques de plus de 2,5 millions de personnes rassemblées par le Type 2 Diabetes Global Genomics Initiative. Plutôt que de se limiter à demander quels variants d’ADN sont associés au diabète, ils ont posé une question plus puissante : quels variants modifient l’activité de gènes ou de protéines spécifiques dans l’organisme, et ces modifications altèrent-elles ensuite le risque de diabète ? Pour cela, ils ont utilisé une approche statistique appelée randomisation mendélienne, qui traite les différences génétiques naturelles comme une sorte d’essai randomisé intégré. Ils ont analysé plus de 20 000 mesures d’activité génique et plus de 1 600 protéines sanguines chez des personnes de quatre groupes d’ascendance — européen, africain, américain admixte et est-asiatique — puis ont répliqué les analyses dans sept tissus centraux pour le contrôle de la glycémie, notamment le pancréas, les îlots producteurs d’insuline, le foie, le muscle et différents dépôts adipeux.
Identifier des leviers moléculaires qui augmentent ou réduisent le risque
En retraçant ces voies génétiques, les chercheurs ont identifié 335 gènes et 46 protéines sanguines dont les niveaux prédits génétiquement ont un impact causal sur le risque de diabète de type 2, et ils ont confirmé nombre de ces résultats dans des cohortes indépendantes. Certains leviers moléculaires étaient déjà suspects, comme MTNR1B, un gène impliqué dans la libération d’insuline par les cellules des îlots pancréatiques, et BAK1, qui influence la mort cellulaire dans le pancréas et le tissu adipeux. D’autres étaient nouveaux ou moins connus, notamment CPXM1, une protéine liée au développement du tissu adipeux et à la résistance à l’insuline, et HIBCH, un gène impliqué dans la fonction mitochondriale. Au total, ils ont répertorié 923 gènes et 46 protéines avec des preuves indiquant que modifier leur activité dans au moins un tissu peut changer la probabilité de développer un diabète.
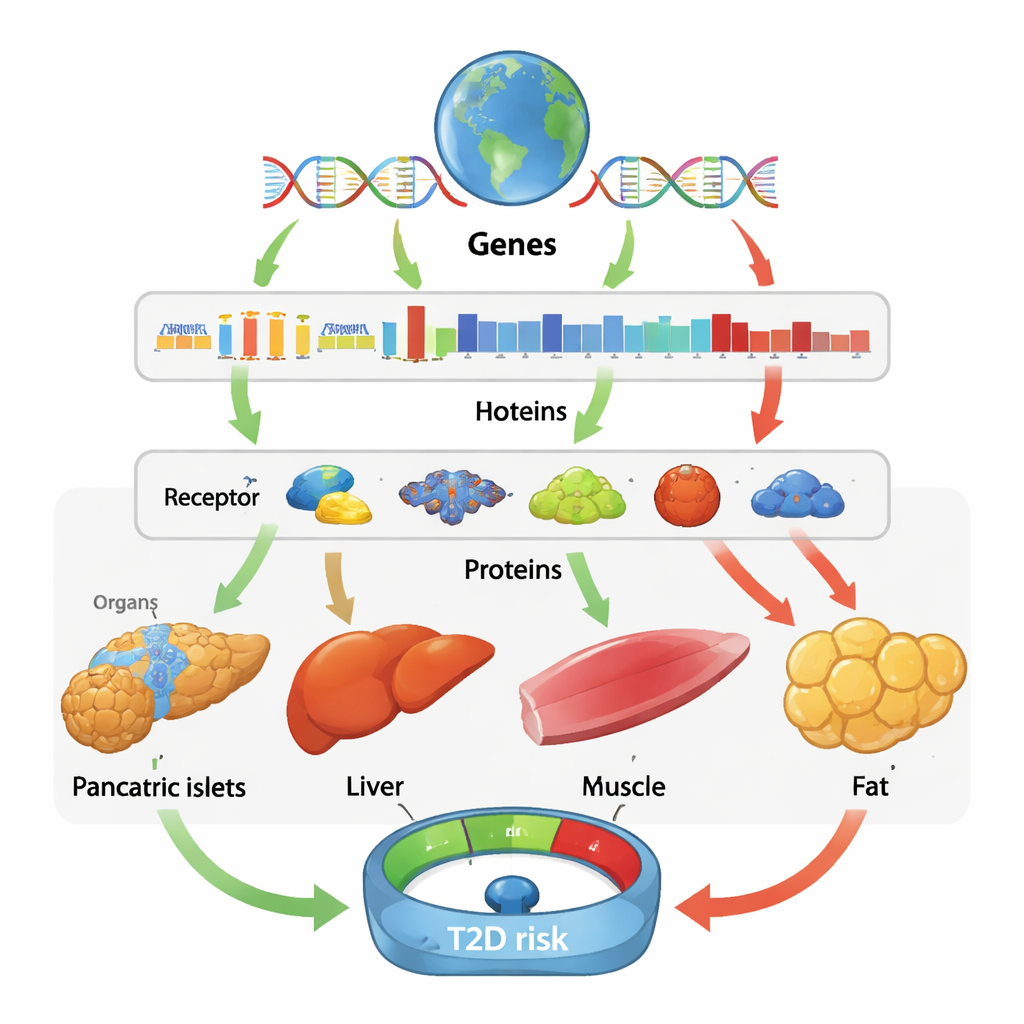
Mêmes gènes, histoires différentes selon les tissus et les populations
Une leçon marquante est que l’effet d’un gène est souvent fortement spécifique au tissu. Par exemple, une activité accrue de BAK1 dans le pancréas et les îlots semble augmenter le risque de diabète, vraisemblablement en contribuant à la perte des cellules productrices d’insuline, tandis qu’un BAK1 plus actif dans le tissu adipeux et le muscle paraît protecteur. HIBCH a montré un schéma tout aussi mixte : dans certains tissus, une activité plus élevée diminuait le risque de diabète, alors que dans d’autres elle l’augmentait. Ces résultats montrent qu’une analyse limitée au sang peut manquer une biologie cruciale se déroulant à l’intérieur des organes, et que la même molécule peut être bénéfique dans un tissu et nocive dans un autre. En revanche, quand l’équipe a comparé les résultats entre les ascendances, elle a observé relativement peu de différences dans l’amplitude des effets, ce qui suggère que de nombreux mécanismes causaux sous-jacents sont partagés à l’échelle mondiale, même si certains signaux — comme des protéines protectrices ou délétères spécifiques aux populations est-asiatiques ou africaines — n’ont été détectables que grâce aux données non européennes.
Relier les nouvelles découvertes à la biologie connue du diabète
Pour vérifier si leur approche avait du sens biologiquement, les auteurs ont mis en regard leurs gènes causaux avec des listes annotées de gènes liés au diabète issues d’études humaines et d’expériences sur souris. Les gènes avec les preuves antérieures les plus solides d’implication dans le diabète avaient beaucoup plus de chances de montrer des effets causaux dans leurs analyses que des gènes choisis au hasard. De plus, les tissus où ces effets causaux apparaissaient correspondaient aux mécanismes connus de la maladie : les gènes liés à la défaillance des cellules bêta importa ent principalement dans les îlots pancréatiques, tandis que les gènes associés au syndrome métabolique montraient leurs effets les plus forts dans la graisse viscérale (adiposité profonde abdominale). Cet alignement soutient l’idée que la chaîne statistique identifie avec succès des mécanismes et non de simples corrélations.
Ce que cela signifie pour les traitements et la prévention à venir
Pour les non-spécialistes, la conclusion clé est que ce travail transforme de longues listes impersonnelles de variants d’ADN en une carte plus claire de gènes, protéines et organes qui conduisent réellement au diabète de type 2. En distinguant la cause de l’effet et en révélant quand une même molécule joue des rôles opposés selon les tissus, il fournit aux développeurs de médicaments des cibles plus précises et met en garde contre les traitements universels susceptibles d’avoir des effets indésirables. Surtout, en incluant délibérément des populations diverses, l’étude contribue à garantir que les futurs médicaments ou scores de risque fondés sur ces découvertes aient plus de chances d’être efficaces de manière large, et pas seulement chez des personnes d’ascendance européenne.
Citation: Bocher, O., Arruda, A.L., Yoshiji, S. et al. Unravelling the molecular mechanisms causal to type 2 diabetes across global populations and disease-relevant tissues. Nat Metab 8, 506–520 (2026). https://doi.org/10.1038/s42255-025-01444-1
Mots-clés: diabète de type 2, mécanismes génétiques, génomique multi-ancestrale, expression génique spécifique aux tissus, inférence causale