Clear Sky Science · fr
Le flux catabolique de la cystéine régulé par Lamin A/C module le destin des cellules souches via le reprogrammation de l’épigénome
Comment le squelette cellulaire communique avec son métabolisme
Pourquoi certaines cellules restent‑elles jeunes et flexibles dans leurs possibles destinées, tandis que d’autres vieillissent ou se figent dans une identité inappropriée ? Cette étude révèle une conversation surprenante au sein de nos cellules entre le « châssis » nucléaire qui organise l’ADN et un nutriment sulfuré, la cystéine. En montrant comment ce dialogue oriente les cellules souches vers des destinées saines — ou vers un vieillissement prématuré — le travail suggère que ce que les cellules « ingèrent » et la manière dont elles le traitent pourraient un jour être modulés pour prévenir certaines maladies génétiques et peut‑être ralentir certains aspects du vieillissement.
Le rôle caché de la coque nucléaire
Au cœur de chaque cellule, l’ADN est appuyé contre un maillage protéique appelé la lamina nucléaire, composé en partie de protéines nommées lamin A et C. Ces lamins donnent non seulement sa forme au noyau ; ils contribuent aussi à décider quels gènes sont verrouillés et lesquels restent accessibles. Les auteurs ont étudié des cellules souches embryonnaires de souris dans leur état le plus flexible, dit « naïf », et ont trouvé que lamin A/C limite normalement deux enzymes métaboliques, CBS et CTH, qui participent à la fabrication et à la dégradation de la cystéine. Quand lamin A/C est présent et actif, ces enzymes sont réprimées et le traitement de la cystéine reste faible, ce qui soutient un état de cellule souche stable et jeune. 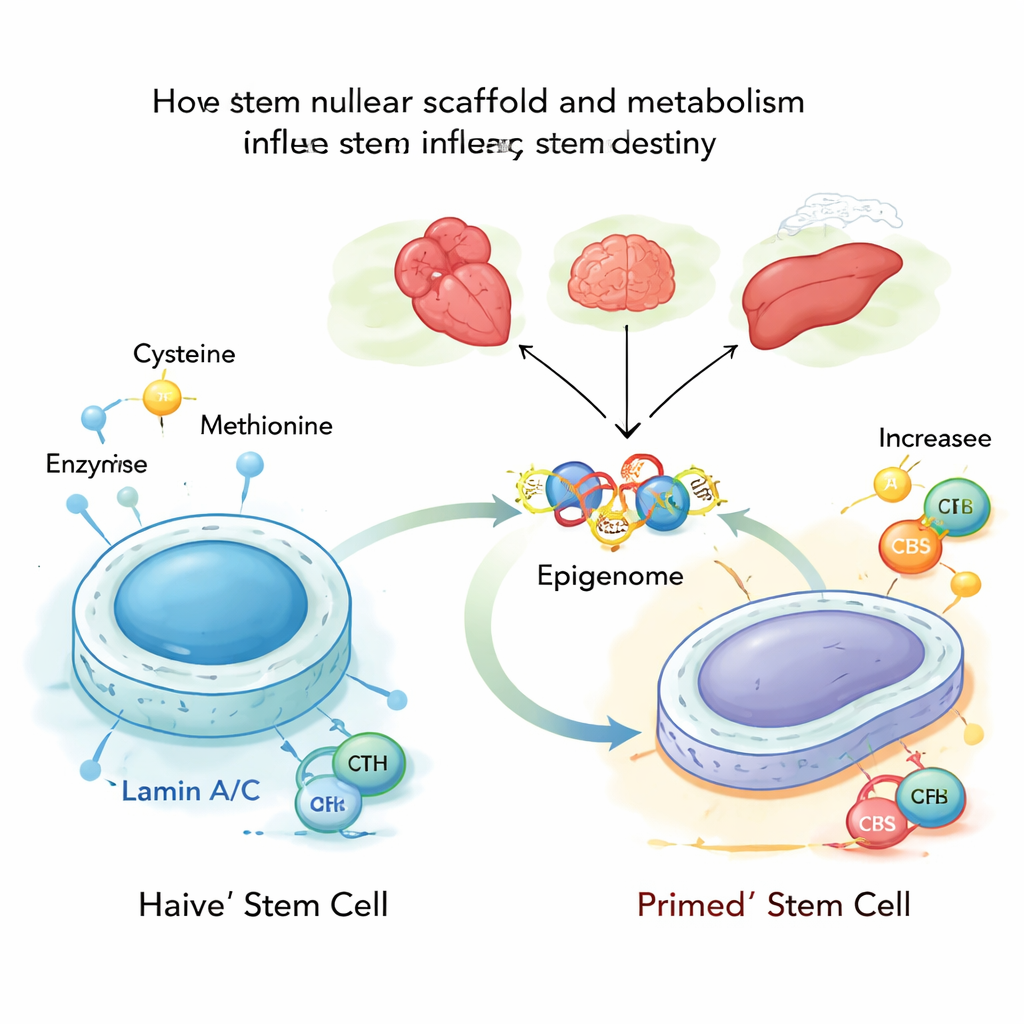
Quand la structure faillit, le métabolisme s’emballe
Puis, les chercheurs ont supprimé lamin A/C ou introduit une mutation liée à une maladie qui mime un trouble humain de vieillissement prématuré appelé progéria de Hutchinson–Gilford. Sans lamin A/C normal, les gènes CBS et CTH deviennent plus accessibles et davantage liés par un facteur de transcription nommé SP1, ce qui les active. Ce changement pousse plus de cystéine dans une voie métabolique aboutissant à l’acétyl‑CoA, une petite molécule qui transporte des groupes acétyle utilisés pour desserrer le compactage de l’ADN. À mesure que la cystéine est acheminée vers l’acétyl‑CoA, les groupes acétyle sont préférentiellement ajoutés à des sites spécifiques des histones — en particulier deux positions de l’histone H3 connues sous les noms K9 et K27 — facilitant l’activation des gènes avoisinants.
Des marques chimiques aux décisions de destin cellulaire
Ces modifications des « tags » histoniques agissent comme un réglage global du panneau de contrôle de la cellule. Dans les cellules souches naïves, l’augmentation de CBS et CTH, ou simplement l’apport accru de cystéine, pousse les cellules vers un état plus avancé, dit « primed », plus proche de la formation de tissus réels. Les gènes impliqués dans le développement cardiaque et d’autres lignées deviennent plus actifs, et le repliement tridimensionnel de l’ADN évolue pour favoriser ces programmes. À l’inverse, réduire CBS et CTH ou limiter la cystéine aide à restaurer une identité plus naïve et jeune, même lorsque la lamina nucléaire est endommagée. Dans des modèles embryonnaires, ce dérèglement métabolique a entraîné une formation biaisée des trois feuillets embryonnaires — les blocs de construction précoces de tous les organes — et une propension anormale vers les cellules musculaires cardiaques, sauf lorsque CBS et CTH étaient rééquilibrés. 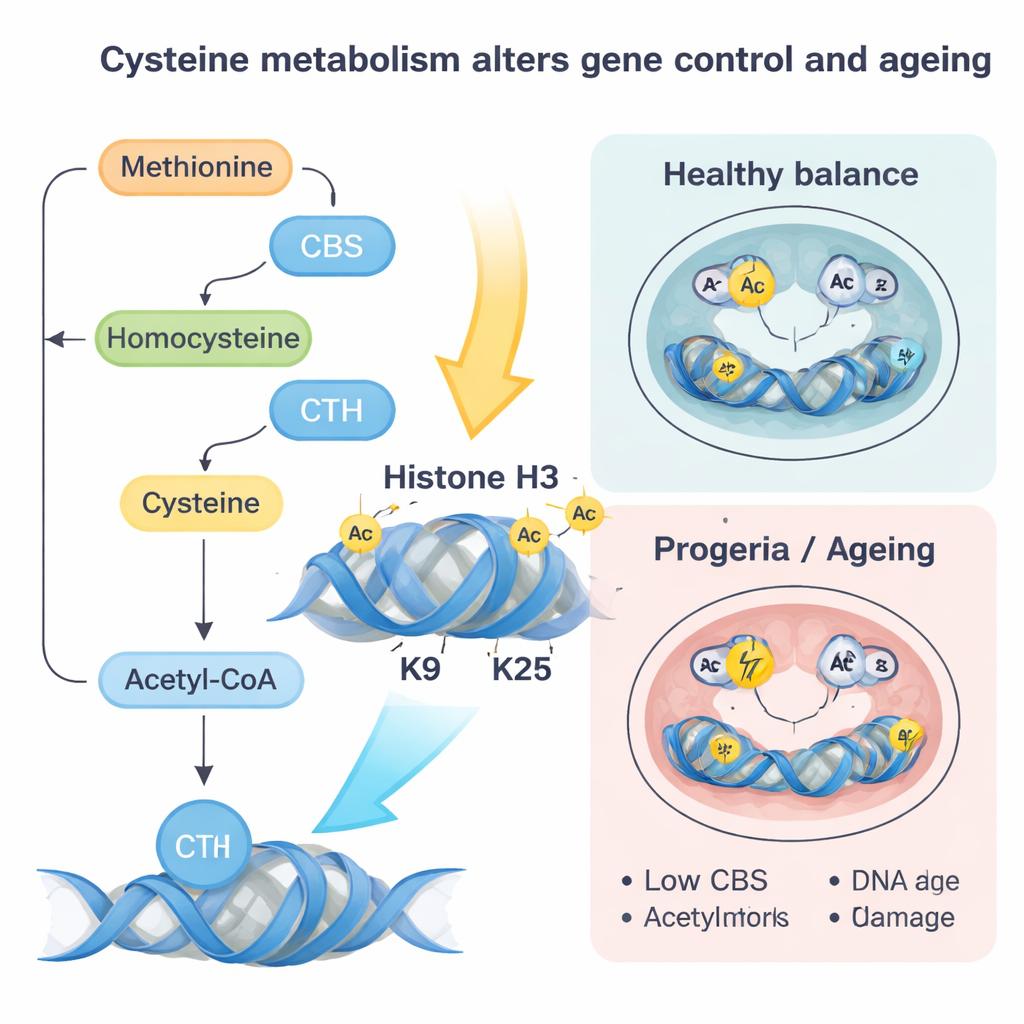
Métabolisme, marques sur l’ADN et vieillissement prématuré
La mutation lamin de type progéria a raconté une histoire complémentaire. Ici, les niveaux de CBS et CTH diminuent, réduisant le flux de cystéine et la production d’acétyl‑CoA par cette voie. Parallèlement, l’homocystéine est réorientée vers le cycle de la méthionine, augmentant les niveaux de SAM, le donneur universel de groupes méthyle. Cela favorise des marques méthyles supplémentaires, en particulier un marqueur appelé H3K9me3 placé par l’enzyme SUV39H1, qui resserre la chromatine et est associé à une réparation de l’ADN altérée. Les auteurs ont montré qu’en restaurant doucement CBS ou en restreignant la méthionine, on abaissait le SAM, on réduisait ces marques méthyles répressives, on améliorait la réparation de l’ADN, on diminuait le stress oxydatif et les marqueurs de sénescence, et on sauvait partiellement la différenciation des cellules cardiaques. Des baisses similaires de CBS et des augmentations de marques répressives ont été observées dans des cœurs de souris âgés normaux et dans des fibroblastes humains de personnes âgées et de patients atteints de progéria, ce qui suggère que ce circuit fonctionne aussi dans le vieillissement naturel.
Ce que cela signifie pour la santé et le vieillissement
Pour un non‑spécialiste, le message est que l’armature structurale de la cellule et son métabolisme sont étroitement liés : quand la coque nucléaire formée par lamin A/C est perturbée, l’utilisation de la cystéine change, ce qui réécrit à son tour les marques chimiques sur les protéines qui emballent l’ADN. Ces marques déterminent quels gènes s’activent pendant que les cellules souches construisent l’organisme et influencent la capacité des cellules à réparer les dégâts au cours de la vie. En modulant soigneusement des enzymes comme CBS et CTH — ou en ajustant l’apport en nutriments tels que la méthionine et la cystéine — il pourrait être possible de corriger une partie de la mauvaise écriture de ces marques dans les maladies liées à la lamina et peut‑être d’atténuer certains aspects du vieillissement prématuré ou normal.
Citation: Wang, Y., Shi, H., Wittig, J. et al. Lamin A/C-regulated cysteine catabolic flux modulates stem cell fate through epigenome reprogramming. Nat Metab 8, 431–453 (2026). https://doi.org/10.1038/s42255-025-01443-2
Mots-clés: cellules souches, lamina nucléaire, métabolisme de la cystéine, épigénétique, vieillissement