Clear Sky Science · fr
ABEL-FRET comble l’écart temporel dans les mesures monocellulaires de la dynamique structurale du récepteur A2A de l'adénosine
Observer de minuscules commutateurs cellulaires en temps réel
Beaucoup de médicaments actuels agissent en basculant des « commutateurs » moléculaires à la surface des cellules appelés récepteurs. Ces commutateurs changent continuellement de conformation lorsqu’ils activent ou désactivent des signaux, mais la plupart des outils ne peuvent voir que les mouvements très rapides ou les mouvements très lents — pas les deux. Cet article présente une méthode pour observer un récepteur cible unique en solution beaucoup plus longtemps qu’auparavant, révélant comment il reste dans certaines conformations cruciales pour l’action des médicaments.
Pourquoi ces protéines changeant de forme sont importantes
L’étude se concentre sur une grande classe de protéines de surface cellulaire connues sous le nom de récepteurs couplés aux protéines G, ou GPCR. Ces protéines contrôlent des processus vitaux tels que la vision, l’humeur, la pression artérielle et les réponses immunitaires, et plus d’un tiers des médicaments approuvés agissent sur elles. Un membre bien étudié, le récepteur de l’adénosine A2A, participe à la régulation du sommeil, de la douleur, de l’inflammation et de la signalisation cérébrale, et constitue une cible prometteuse pour traiter des pathologies comme la maladie de Parkinson et le cancer. Les GPCR sont très flexibles : selon la molécule qui se lie, le récepteur adopte des conformations distinctes qui favorisent certaines voies de signalisation plutôt que d’autres. Cette même flexibilité complique cependant la conception de médicaments à partir d’instantanés statiques obtenus par cristallographie ou cryo‑microscopie électronique.
Suivre un récepteur unique sans l’immobiliser
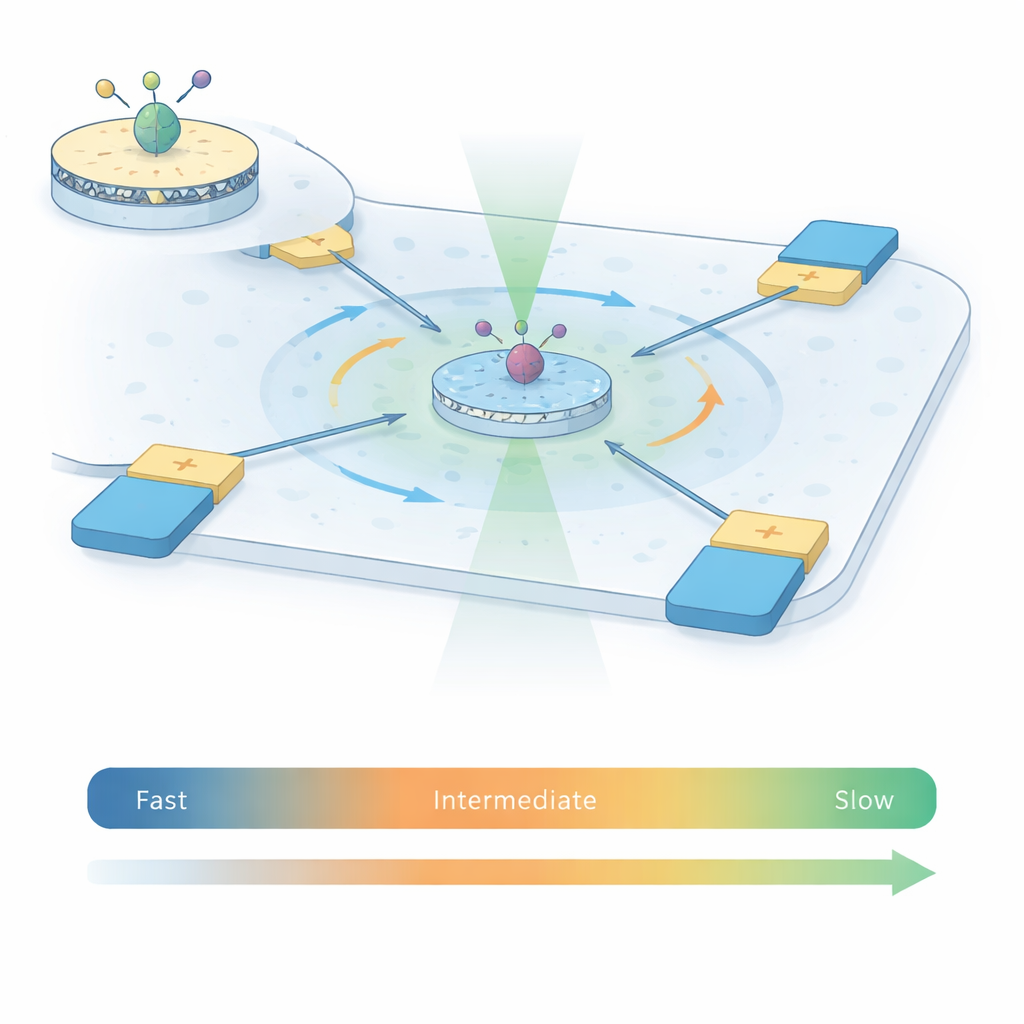
Pour capturer les mouvements des récepteurs A2A, les auteurs combinent deux techniques puissantes dans ce qu’ils appellent ABEL‑FRET. D’abord, ils reconstituent des récepteurs uniques dans de petites nappes de membrane artificielle appelées nanodisques, offrant à chaque protéine un environnement plus naturel que le détergent seul. Ils fixent une paire de colorants fluorescents à deux parties mobiles à l’intérieur du récepteur. Lorsque le récepteur change de conformation, la distance et l’orientation relative entre ces colorants varient, modifiant le transfert d’énergie entre eux — un phénomène connu sous le nom de Förster resonance energy transfer (FRET). Ensuite, au lieu d’ancrer le récepteur sur une surface, ils utilisent un piège électrocinétique anti‑Brownien (ABEL) : une chambre microfluidique équipée d’électrodes qui détectent où se trouve une particule fluorescente et la renvoient doucement au centre, contrebalançant le mouvement brownien aléatoire.
Combler la fenêtre temporelle manquante
Les expériences FRET monocellulaires traditionnelles observent soit des récepteurs en diffusion libre pendant seulement quelques millièmes de seconde, soit des récepteurs immobilisés sur une surface pendant des secondes à des minutes. Chaque approche couvre une fenêtre temporelle différente. Avec le piège ABEL, ce travail maintient des récepteurs A2A individuels en vue pendant une à deux secondes alors qu’ils restent libres en solution, soit environ 100 fois plus longtemps que dans les expériences limitées par diffusion. Ce temps d’observation étendu permet à l’équipe de mesurer comment le signal FRET fluctue au sein de chaque rafale piégée et à travers des milliers de récepteurs, dans quatre conditions : sans ligand, avec un antagoniste et avec deux agonistes différents. Des outils statistiques empruntés à l’analyse de signal — variance, corrélation et analyses de récurrence — leur permettent de distinguer le bruit photonique aléatoire des véritables changements structuraux lents du récepteur.
Des conformations cachées et longue durée révélées
Les lectures FRET montrent que les récepteurs occupent plusieurs conformations distinctes qui ne s’interconvertissent pas complètement pendant les temps d’observation typiques de quelques centaines de millisecondes. Dans toutes les conditions, la dispersion des valeurs FRET est bien plus large que prévue par le seul bruit, révélant une hétérogénéité structurale : différentes molécules résident dans différentes conformations de longue durée. Lorsque des agonistes se lient, le niveau moyen de FRET monte, indiquant que le récepteur passe davantage de temps dans une disposition « de type actif » de ses hélices internes. Pourtant, même dans ce cas, les analyses de corrélation montrent qu’une fois qu’un récepteur est dans un état à FRET élevé ou intermédiaire, il a une forte probabilité d’y rester pendant au moins plusieurs centaines de millisecondes. Ces résultats révisent les estimations antérieures basées sur des expériences plus rapides, étendant les « temps de résidence » caractéristiques dans des états de longue durée de quelques millisecondes à bien plus d’un dixième de seconde.
Une nouvelle cartographie du paysage énergétique du récepteur
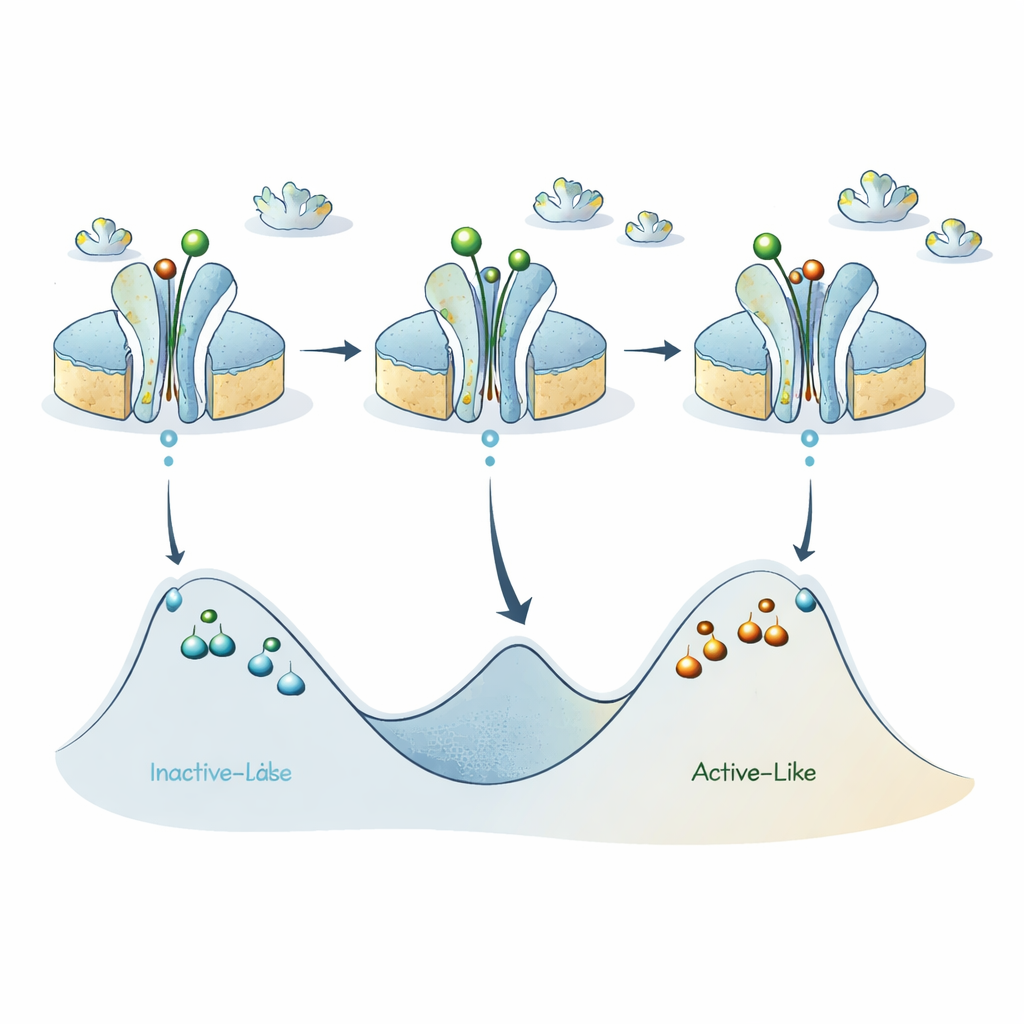
En réunissant ces éléments, les auteurs affinent un modèle antérieur dans lequel le récepteur A2A bascule principalement entre un état de type inactif et un état de type actif. Leurs nouvelles données suggèrent que chacune de ces deux grandes catégories cache en réalité plusieurs sous‑états séparés par des barrières énergétiques substantielles, de sorte que des récepteurs individuels peuvent rester « coincés » dans une version donnée de l’état actif‑like ou inactif‑like pendant des durées étonnamment longues. Les ligands activateurs abaissent la barrière entre les bassins principaux inactif‑like et actif‑like, favorisant des basculements rapides à l’échelle sous‑milliseconde, mais les barrières internes à chaque bassin restent élevées, donnant lieu aux sous‑états de longue durée détectés par ABEL‑FRET.
Ce que cela signifie pour les médicaments de demain
Pour les non‑spécialistes, le message clé est qu’une cible médicamenteuse comme le récepteur A2A ne se contente pas de basculer entre « éteint » et « allumé ». Elle explore plutôt un paysage accidenté de conformations, dont certaines persistent suffisamment longtemps pour influencer la manière dont les signaux sont transmis à l’intérieur des cellules et la façon dont les médicaments agissent au fil du temps. En prolongeant la durée pendant laquelle on peut observer des récepteurs individuels dans leur état naturel et non attaché, ABEL‑FRET comble une lacune cruciale entre les mesures ultrarapides et très lentes. Cette approche peut désormais être appliquée à de nombreuses protéines membranaires, offrant une image temporellement résolue plus complète de la façon dont les cibles médicamenteuses potentielles respirent, se déplacent et répondent aux composés thérapeutiques.
Citation: Maslov, I., Borshchevskiy, V., Pérez, I. et al. ABEL-FRET bridges the timescale gap in single-molecule measurements of the structural dynamics in the A2A adenosine receptor. Commun Chem 9, 114 (2026). https://doi.org/10.1038/s42004-026-01941-8
Mots-clés: récepteurs couplés aux protéines G, FRET monocellulaire, récepteur de l’adénosine A2A, dynamique conformationnelle des protéines, piège ABEL