Clear Sky Science · fr
Étude mécanistique de la migration du sulfate dans les glycosaminoglycanes lors de la fragmentation en spectrométrie de masse
Pourquoi le déplacement des étiquettes chimiques sur les sucres compte
Nos cellules sont recouvertes de longues chaînes de sucres qui contribuent à réguler des processus aussi variés que la coagulation sanguine, la défense immunitaire et l’attachement des virus aux cellules. Bon nombre de ces chaînes portent de minuscules étiquettes chimiques appelées groupes sulfate dont la position précise le long de l’épine dorsale sucrée joue le rôle d’un code moléculaire, indiquant aux protéines où et quand se lier. Les scientifiques s’appuient largement sur la spectrométrie de masse, une technique de mesure très puissante, pour lire ces codes. Cette étude révèle que, lors de telles mesures, les groupes sulfate peuvent discrètement changer de position, induisant en erreur sur la véritable architecture de ces sucres d’importance biologique.
Chaînes de sucres complexes avec des marques critiques
Les glycosaminoglycanes sont de longues chaînes linéaires de sucres souvent attachées à des protéines à la surface des cellules. Leurs décorations sulfates ne sont pas aléatoires ; de légères variations de la position d’un groupe sulfate sur une unité sucrée donnée peuvent modifier radicalement l’interaction de la chaîne avec des facteurs de croissance, des protéines de coagulation ou des agents pathogènes. Pour cette raison, les chercheurs cherchent à déterminer non seulement combien de sulfates sont présents, mais aussi précisément où ils sont placés. La spectrométrie de masse, souvent associée à une fragmentation contrôlée des chaînes, est l’une des principales méthodes pour le faire. Cependant, des indices antérieurs suggéraient que des groupes chargés comme les sulfates pourraient se déplacer pendant la mesure, compliquant l’interprétation du véritable motif de modifications.
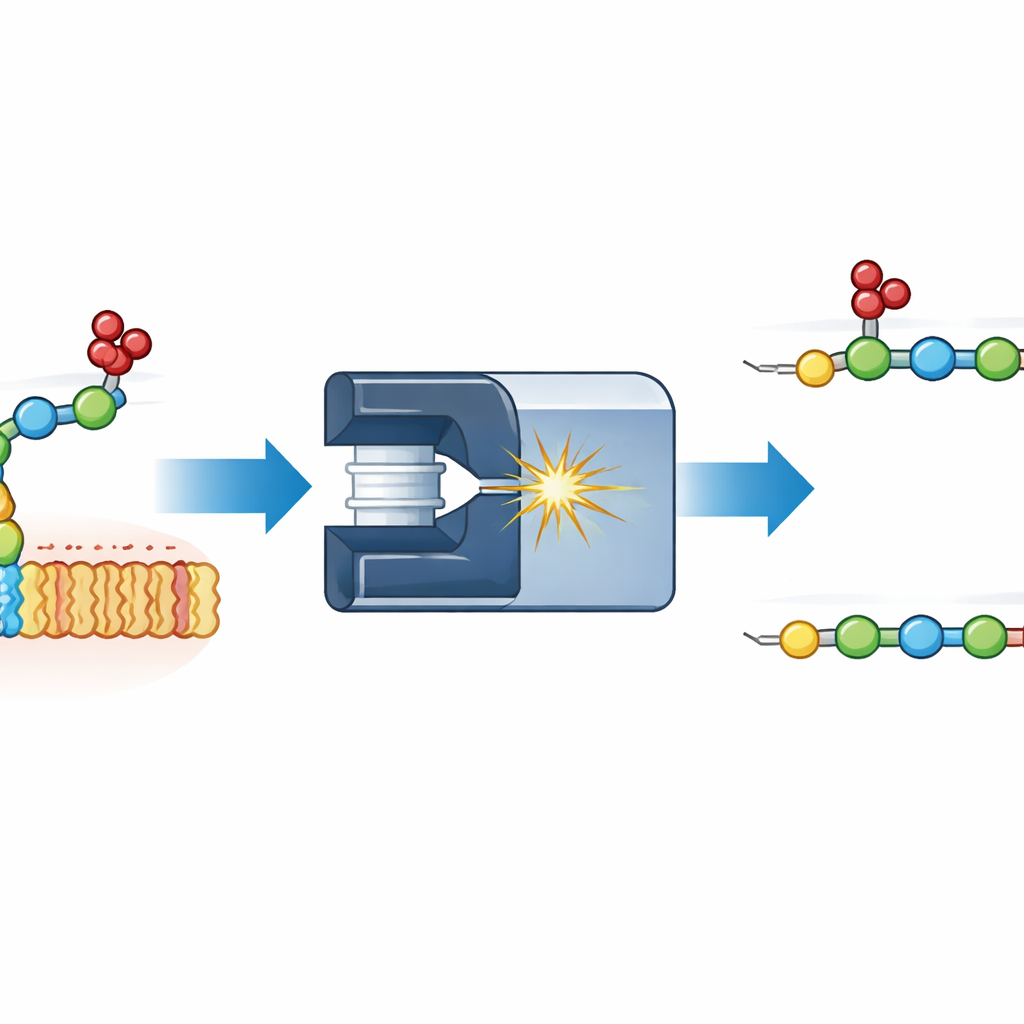
Observer le déplacement des sulfates pendant la mesure
Les auteurs se sont focalisés sur un modèle simple : un fragment disaccharidique de l’héparane sulfate, l’un des glycosaminoglycanes les mieux connus. Ils ont fixé différentes étiquettes fluorescentes à une extrémité du disaccharide et l’ont fragmenté à l’intérieur d’un spectromètre de masse. En mesurant comment les fragments résultants dérivent à travers un gaz sous champ électrique, une technique appelée mobilité ionique, ils ont pu distinguer des conformations qui ont autrement la même masse. Un fragment inattendu est apparu, plus lourd d’exactement un groupe sulfate mais dans le mauvais emplacement : au lieu de rester sur le premier sucre, le sulfate avait migré sur le second. Des comparaisons avec des composés de référence soigneusement synthétisés ont montré que le sulfate migré pouvait atterrir en deux sites distincts du second sucre, donnant deux conformations différentes parfaitement résolues par mobilité ionique.
Identifier les nouveaux sites d’atterrissage et tester les étiquettes
Pour mieux comprendre où le sulfate avait abouti et si d’autres positions étaient possibles, l’équipe a combiné ses mesures avec des simulations informatiques détaillées. Ils ont calculé de nombreuses conformations tridimensionnelles possibles pour les structures candidates et prédit comment chacune devrait évoluer dans la phase gazeuse. Seuls des sulfates situés en deux sites spécifiques du second sucre — connus des spécialistes sous les positions 6O et 3O — correspondaient au comportement expérimental, tandis que d’autres emplacements hypothétiques semblaient improbables. Les chercheurs ont ensuite testé si les étiquettes attachées elles-mêmes pouvaient favoriser le réarrangement, en remplaçant l’étiquette initiale par trois étiquettes plus simples. Dans tous les cas, la migration du sulfate a persisté et a produit des fragments de nature similaire, indiquant que le choix de l’étiquette a peu d’effet sur l’occurrence de la migration, bien qu’il puisse modifier subtilement la facilité à distinguer les différents produits.
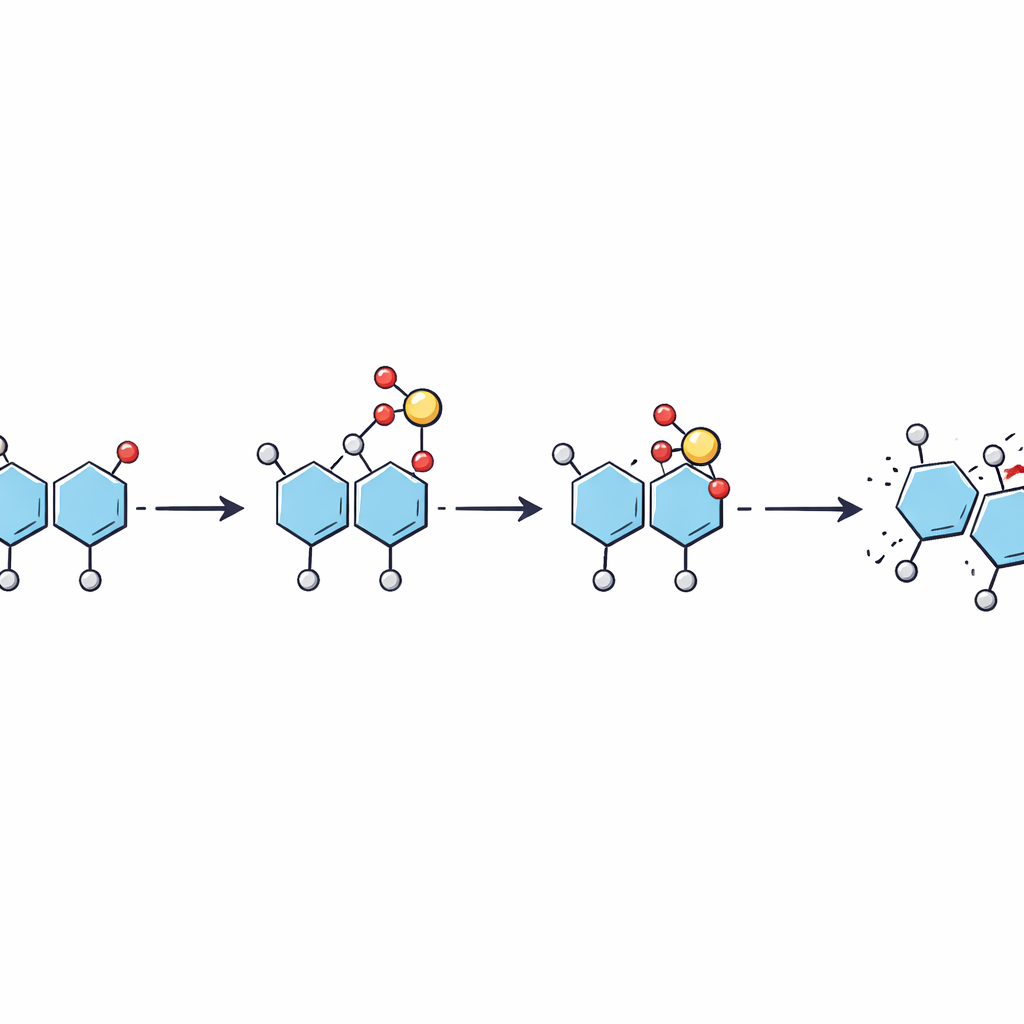
Un déplacement par étapes plutôt qu’un saut unique
En utilisant des expériences de fragmentation à énergie ajustée conjointement avec des simulations supplémentaires, les auteurs ont reconstitué un schéma étape par étape du mouvement du sulfate. Lorsque l’ion est énergisé dans le spectromètre de masse, un proton mobile active d’abord le groupe sulfate, qui saute ensuite du sucre d’origine vers un site particulier du sucre voisin au moment où la liaison entre eux se rompt. Cela produit un fragment dans lequel le sulfate se trouve dans une position intermédiaire. Avec une énergie supplémentaire, le sulfate peut se repositionner à nouveau le long du même sucre vers un site plus stable. Les résultats suggèrent que ces réarrangements peuvent se produire à des énergies inférieures à celles nécessaires pour casser l’épine dorsale sucrée, ce qui signifie qu’ils peuvent se produire discrètement lors d’analyses de routine.
Ce que cela signifie pour le décodage des structures sucrées
Pour les non-spécialistes, le message clé est que les étiquettes chimiques sur des sucres biologiques importants ne sont pas toujours figées pendant l’analyse ; elles peuvent glisser le long de la chaîne pendant que la molécule vole dans le spectromètre de masse. L’étude montre en détail que, du moins pour un fragment représentatif d’héparane sulfate, un groupe sulfate peut migrer d’une unité sucrée à une autre puis se stabiliser à de nouvelles positions, produisant des fragments trompeurs qui imitent des caractéristiques structurelles authentiques. Cela signifie que certaines mesures passées et futures pourraient mal interpréter le code des sulfates à moins que des techniques supplémentaires, telles que la mobilité ionique et la modélisation avancée, ne soient employées pour détecter ces mouvements cachés. Le travail appelle à des études plus systématiques pour déterminer l’ampleur de cette migration de sulfate, afin que les chercheurs puissent relier plus fiablement les motifs sucrés à la surface cellulaire à la santé et à la maladie.
Citation: Polewski, L., Yaman, M., Tokić, M. et al. Mechanistic study on the sulfate migration in glycosaminoglycans during MS fragmentation. Commun Chem 9, 130 (2026). https://doi.org/10.1038/s42004-026-01939-2
Mots-clés: sulfate d’héparane, glycosaminoglycanes, spectrométrie de masse, migration du sulfate, mobilité ionique