Clear Sky Science · fr
La profondeur de la pose de liaison module l’efficacité des ligands photosensibles au récepteur 5-HT2A
Éclairer les médicaments cérébraux commutables
Imaginez un médicament que l’on peut activer et désactiver d’un éclat de lumière, dirigeant avec précision des récepteurs cérébraux tout en évitant les effets indésirables. Cette étude explore précisément cette idée pour un récepteur clé de la sérotonine lié à l’humeur, à la perception et aux drogues psychédéliques. Les chercheurs ont cherché à comprendre pourquoi deux molécules sensibles à la lumière, presque identiques, se comportent si différemment — l’une agissant presque comme un interrupteur parfait marche/arrêt, l’autre refusant obstinément de s’éteindre complètement. Leur réponse tient à un facteur étonnamment simple : la profondeur à laquelle la molécule s’insère dans le récepteur.
Médicaments activés par la lumière dans le cerveau
Les médicaments activés par la lumière, appelés aussi outils photopharmacologiques, sont conçus de sorte qu’un faisceau lumineux bascule une partie de la molécule entre deux formes, comme une version pliée et une version allongée. Ces formes modifient la force avec laquelle le médicament s’accroche à sa cible. Dans ce travail, la cible est le récepteur humain 5-HT2A, une protéine à la surface des cellules cérébrales qui répond à la sérotonine et joue un rôle central tant dans les effets antipsychotiques que psychédéliques. Les molécules étudiées sont des dérivés de la N,N-diméthyltryptamine (DMT), modifiés par une unité azobenzène photosensible. Deux versions ne diffèrent que par la position d’un petit groupe méthoxy sur un cycle — soit en position « para », soit en position « méta » — pourtant leur comportement biologique sous lumière est radicalement différent.
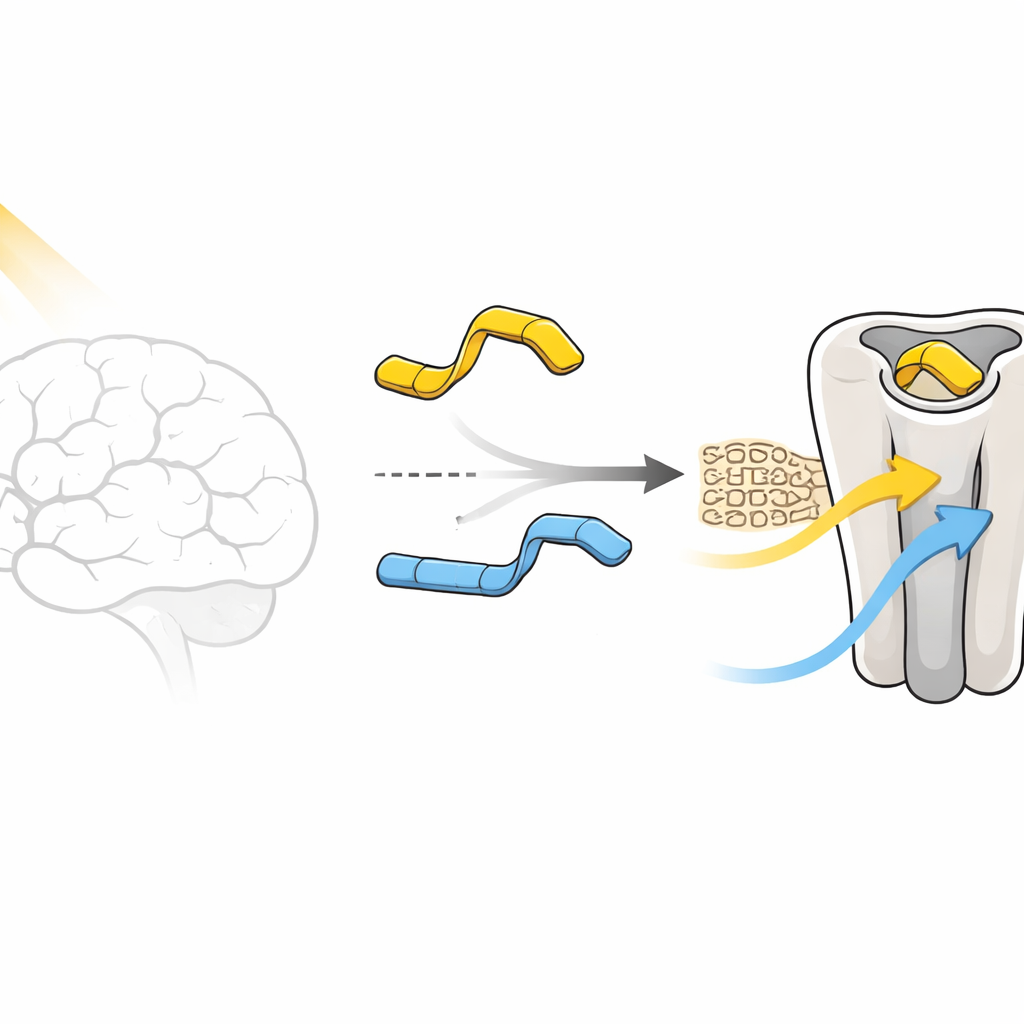
Deux molécules presque jumelles, des interrupteurs très différents
Dans des tests cellulaires, la version para, appelée composé 1, se comporte presque comme un interrupteur numérique. Dans l’obscurité, sa forme « trans » active à peine le récepteur et le bloque même légèrement, agissant comme un faible antagoniste. Lorsque la lumière le convertit en forme « cis », la même molécule devient un activateur modéré, activant partiellement le récepteur. La version méta, le composé 2, refuse de coopérer de la même manière : ses formes clair et sombre maintiennent toutes deux le récepteur assez actif, sans jamais fournir un véritable état « éteint ». L’énigme centrale de cet article est de savoir pourquoi une modification chimique si minimale — déplacer un petit groupe sur un anneau — change si fortement la réponse du récepteur.
Regarder à l’intérieur avec des films atomiques
Pour résoudre cela, l’équipe a utilisé de vastes simulations de dynamique moléculaire tout-atomes, tournant en quelque sorte des films détaillés de chaque atome du récepteur, de la membrane environnante, de l’eau et de chaque ligand sur un total d’environ 80 microsecondes. Ils ont simulé les deux molécules dans chacune de leurs formes commandées par la lumière, et dans les formes inactive et active du récepteur 5-HT2A. En suivant des « microswitchs » structurels connus à l’intérieur de la protéine — comme un tryptophane clé qui bascule, un pont salin qui se rompt, et le mouvement du sodium et de l’eau au cœur — ils pouvaient dire quand le récepteur penchait vers un état éteint ou allumé. Ils ont aussi comparé dans quelle mesure les nouvelles molécules imitaient la posture de liaison du LSD, un activateur partiel bien étudié, en utilisant le recouvrement de leurs systèmes d’anneaux comme repère.
La profondeur compte plus que la forme seule
L’idée centrale est que l’efficacité des molécules est surtout gouvernée par la profondeur à laquelle elles s’insèrent dans la poche de liaison du récepteur. Dans le récepteur inactif, la forme trans du composé para crée un ensemble particulier de liaisons hydrogène qui le tirent exceptionnellement en profondeur, en dessous de la région où se produisent typiquement les contacts activateurs. Cette « sur-insertion » l’empêche d’atteindre des résidus polaires clés qui contribuent à commuter le récepteur vers l’état actif, de sorte qu’il stabilise l’état éteint. La forme trans du composé méta ne peut pas établir les mêmes contacts d’ancrage et se place plutôt plus en surface, dans une pose plus semblable à celle du LSD, compatible avec l’activation, ce qui explique son activité résiduelle. Lorsque la lumière convertit les deux molécules en leurs formes cis, elles se déplacent généralement vers des positions plus superficielles et plus proches d’un pose d’activateur. Pourtant, même là, la géométrie compte : dans le récepteur actif, le cis du composé 2 peut glisser plus profondément dans un tunnel hydrophobe entre deux hélices et former une liaison hydrogène persistante qui renforce son fort comportement agoniste, tandis que le cis du composé 1 en est stériquement empêché.
Contrôle fin de l’eau interne et des ions
Les simulations montrent aussi que la profondeur de liaison module subtilement une poche interne de sodium et une voie d’eau qui sont connues pour influencer l’activation du récepteur. Une liaison profonde et rigide par le composé para en forme trans emprisonne fermement un ion sodium et laisse la région environnante relativement sèche, des caractéristiques associées à un état éteint. En revanche, la liaison plus mobile du composé méta ou des formes cis permet à plus d’eau d’entrer et assouplit l’environnement du sodium, préparant le récepteur à l’activation. Un résidu aromatique clé agissant comme « interrupteur » peut inverser plus facilement son orientation lorsque les ligands sont flexibles et non sur-ancrés, inclinant davantage le récepteur vers un état actif, surtout avec le cis du composé 2.
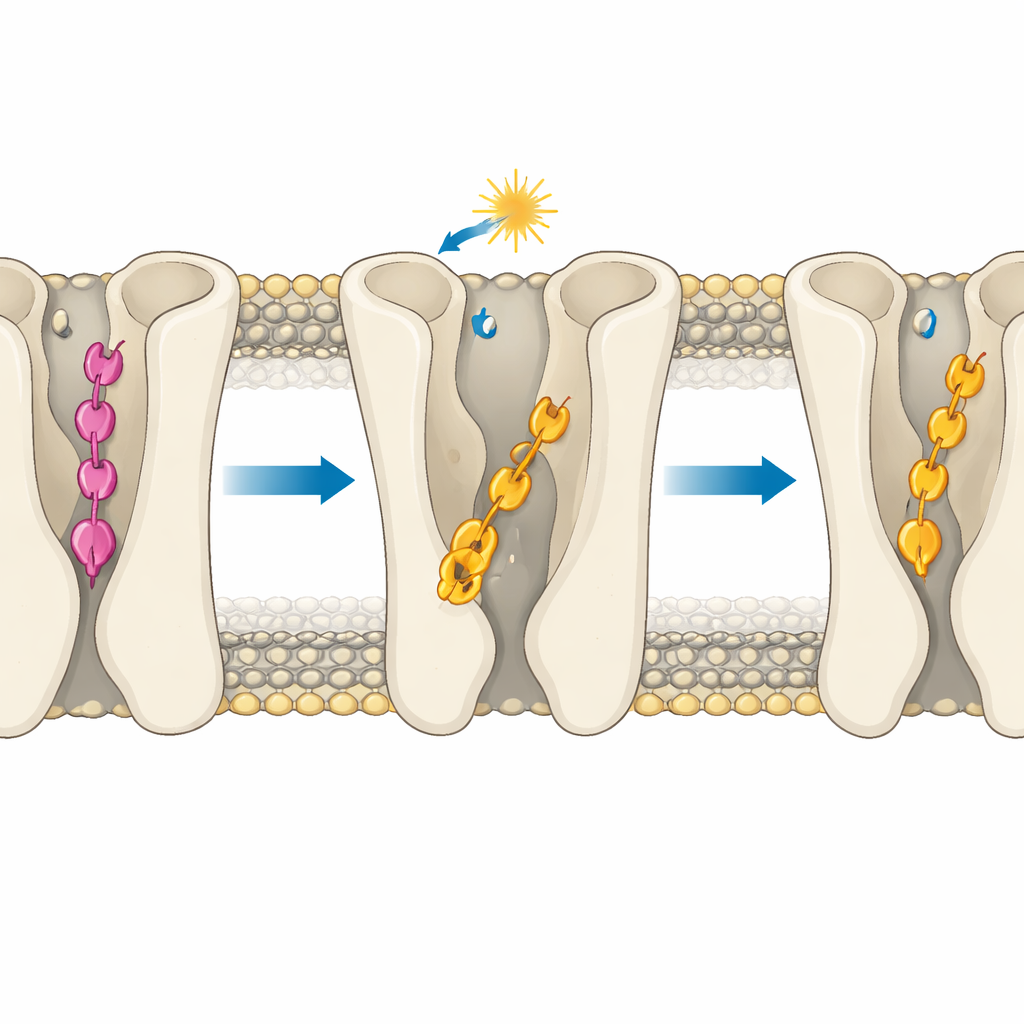
Règles de conception pour de futurs médicaments contrôlés par la lumière
Pour le non-spécialiste, le message est que la profondeur exacte à laquelle un médicament se place dans la poche de son récepteur peut faire la différence entre éteint, partiellement allumé et fortement allumé — même quand la modification chimique semble minime sur le papier. En montrant comment un ligand photosensible peut se sur-inserer et verrouiller le récepteur à l’état éteint, tandis qu’un ligand très proche reste à une profondeur favorable à l’activation, l’étude propose une règle de conception claire : contrôler la profondeur d’insertion aussi soigneusement que vous contrôlez les changements de forme induits par la lumière. Ces connaissances pourraient guider la création de composés photosensibles de nouvelle génération pour traiter les troubles cérébraux avec une précision sans précédent, modulant les voies de signalisation de manière réversible et contrôlée tout en minimisant les effets secondaires.
Citation: Weber, V., Salvadori, G., Natale, F. et al. Binding pose depth modulates photoswitchable ligands’ efficacy at the 5-HT2A receptor. Commun Chem 9, 121 (2026). https://doi.org/10.1038/s42004-026-01936-5
Mots-clés: photopharmacologie, récepteur sérotonine 5-HT2A, ligands photosensibles, activation des GPCR, simulations de dynamique moléculaire