Clear Sky Science · fr
Cristallisation déclenchée par diffusion de masse à une sursaturation locale plus faible
Pourquoi cela importe au-delà du laboratoire
Les cristaux de sel peuvent paraître banals, mais leur mode de formation a des conséquences majeures — de la fabrication des médicaments à la valorisation des ressources provenant d’eaux usées salées. Cette étude montre que les cristaux peuvent commencer à se former plus tôt, et à des endroits différents, lorsque le liquide est doucement poussé hors d’équilibre par des gradients de température et de concentration. Comprendre ce comportement subtil pourrait aider à concevoir des méthodes plus propres et moins coûteuses pour gérer les saumures, à fabriquer de meilleurs matériaux et à contrôler l’entartrage indésirable dans les canalisations et les équipements.

Comment les cristaux naissent habituellement
La cristallisation se produit lorsqu’une substance dissoute, comme le chlorure de potassium (KCl) dans l’eau, dépasse la quantité qui peut rester dissoute de manière stable. Cet état s’appelle la sursaturation. Les théories classiques affirment que les cristaux n’apparaissent que lorsque la sursaturation est suffisante pour surmonter une barrière énergétique, et que la nucléation devrait débuter là où la solution est la plus sursaturée. En industrie, on amène généralement les solutions à ce stade en les refroidissant, en évaporant le solvant ou en ajoutant un « antisolvant ». Dans ces conditions conventionnelles, presque uniformes, les chercheurs ont cartographié une zone métastable — une fenêtre où le liquide est sursaturé mais où aucun cristal visible ne s’est encore formé.
Trois façons différentes de faire cristalliser le même sel
Les auteurs ont étudié l’apparition des cristaux de KCl dans trois scénarios soigneusement contrôlés à l’intérieur d’une cellule plate conçue sur mesure avec un contrôle de température indépendant en haut et en bas. D’abord, ils ont réalisé des expériences de refroidissement standard, abaissant la température de façon uniforme depuis 20 °C et observant l’apparition des premiers cristaux. Cela a établi une frontière de référence dans la carte concentration–température : en dessous d’une certaine température, des cristaux se formaient toujours ; au-dessus, la solution restait sans cristaux pendant des heures. Ils ont ensuite comparé cette référence à deux situations plus complexes dans lesquelles la solution subissait un transport de masse directionnel plutôt qu’un refroidissement uniforme simple.
Quand la chaleur provoque le déplacement du sel
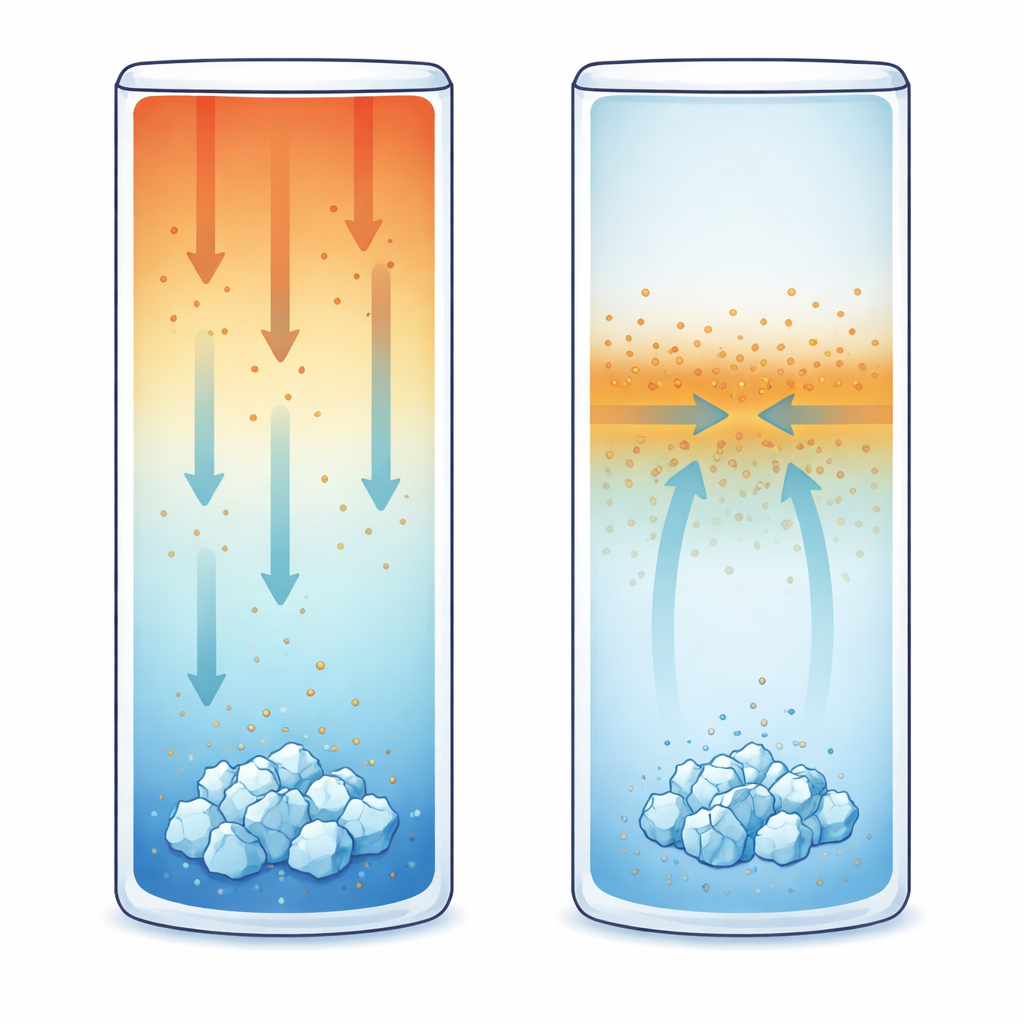
Dans la deuxième série d’expériences, la solution partait de la même composition mais était maintenue avec le haut à 20 °C et le bas refroidi à 15 °C. Ce gradient de température vertical induit la thermodiffusion, c’est‑à‑dire que les ions dissous dérivent en réponse à la température, pas seulement à la concentration. Pour le KCl dans la plage testée, le comportement est thermophobe : les ions ont tendance à migrer vers la région la plus froide, accumulant davantage de sel près du fond. À l’aide d’une méthode optique sensible appelée interférométrie à décalage de phase, les chercheurs ont suivi de minuscules variations d’indice de réfraction révélant l’évolution de la concentration et de la température. Ils ont constaté que les cristaux se formaient systématiquement sur la paroi froide inférieure, dans les régions où le gradient de concentration était le plus fort — pourtant la sursaturation locale y était légèrement inférieure à celle observée dans le cas de refroidissement uniforme. Autrement dit, la présence d’un flux de masse soutenu a permis à la cristallisation de démarrer plus tôt que prévu.
Quand le sel diffuse à température parfaitement homogène
Le troisième scénario supprimait complètement les différences de température. Toute la cellule était maintenue à 17 °C uniformément, remplie initialement avec la solution de référence. Puis un petit volume d’une solution de KCl plus diluée a été injecté doucement depuis un coin en haut, créant un contraste de concentration prononcé mais presque sans brassage du fluide. La diffusion a ensuite lissé ce contraste tandis que les ions migraient de la région la plus concentrée vers la plus diluée. Là encore, l’interférométrie a révélé comment le champ de concentration évoluait dans le temps. De manière surprenante, les premiers cristaux visibles n’apparaissaient pas là où la solution était la plus sursaturée. Ils se formaient plutôt à peu près à mi‑hauteur de la cellule, près de l’interface où le gradient de concentration — et donc le flux de masse diffusif — était le plus fort.
Ce que cela signifie pour la théorie et la technologie
Dans les trois méthodes — refroidissement, thermodiffusion et diffusion isotherme —, les premiers cristaux apparus se ressemblaient beaucoup : surtout des cristaux cubiques de KCl avec des formes de croissance familières. Ce qui changeait, ce n’était pas la structure cristalline mais les conditions ayant déclenché leur naissance. Sous des flux de masse imposés, les cristaux sont apparus à une sursaturation locale plus faible et à des emplacements gouvernés par des gradients plutôt que par les maxima de concentration. Cela suggère que le trafic moléculaire directionnel dans le liquide peut aider les ions à s’aligner en zones denses servant de noyaux précoces, réduisant effectivement la zone métastable. La théorie classique de la nucléation n’explique pas entièrement ce comportement, tandis que des idées plus récentes de nucléation en plusieurs étapes sont cohérentes avec ces observations. Sur le plan pratique, ce travail ouvre la voie à un contrôle plus fin de la cristallisation dans des procédés tels que la désalinisation sans rejet liquide, où exploiter la thermodiffusion pourrait aider à transformer les saumures en sels solides en consommant moins d’énergie et de produits chimiques.
Citation: Xu, S., Torres, J.F. Crystallisation triggered by mass diffusion at a lower local supersaturation. Commun Chem 9, 125 (2026). https://doi.org/10.1038/s42004-026-01925-8
Mots-clés: cristallisation, thermodiffusion, sursaturation, désembouage, transport de masse