Clear Sky Science · fr
Des effets synergiques cation‑facette accélèrent la cinétique de l’évolution de l’hydrogène en milieu alcalin sur des surfaces Pt escarpées
Pourquoi cela importe pour l’énergie propre
Produire de l’hydrogène propre à partir de l’eau est un élément clé de nombreux plans visant la neutralité carbone, mais les dispositifs les plus pratiques aujourd’hui gaspillent de l’énergie parce que la réaction qui génère les bulles d’hydrogène peut être étonnamment lente en solutions alcalines (basiques). Cette étude examine à l’échelle des atomes et des molécules d’eau pourquoi certaines surfaces de platine fonctionnent mieux que d’autres, et comment des ions dissous courants dans le liquide peuvent s’associer à la surface métallique pour accélérer la production d’hydrogène.
Façonner les surfaces métalliques pour guider l’eau
Les chercheurs se concentrent sur le platine, la référence pour le fractionnement de l’eau, et comparent deux types de paysages atomiques à sa surface. L’un est plat, comme une terrasse lisse (appelée Pt(111)) ; l’autre est escarpé, comme un petit escalier (Pt(311)). En utilisant des simulations quantiques avancées qui incluent à la fois les électrons et les molécules d’eau en mouvement, ils modélisent le comportement de ces surfaces sous des tensions de fonctionnement réalistes dans un électrolyseur alcalin. L’objectif est de voir comment l’environnement local juste à côté du métal — où se rencontrent eau, ions et électrons — contrôle la vitesse de la première étape de formation de l’hydrogène.
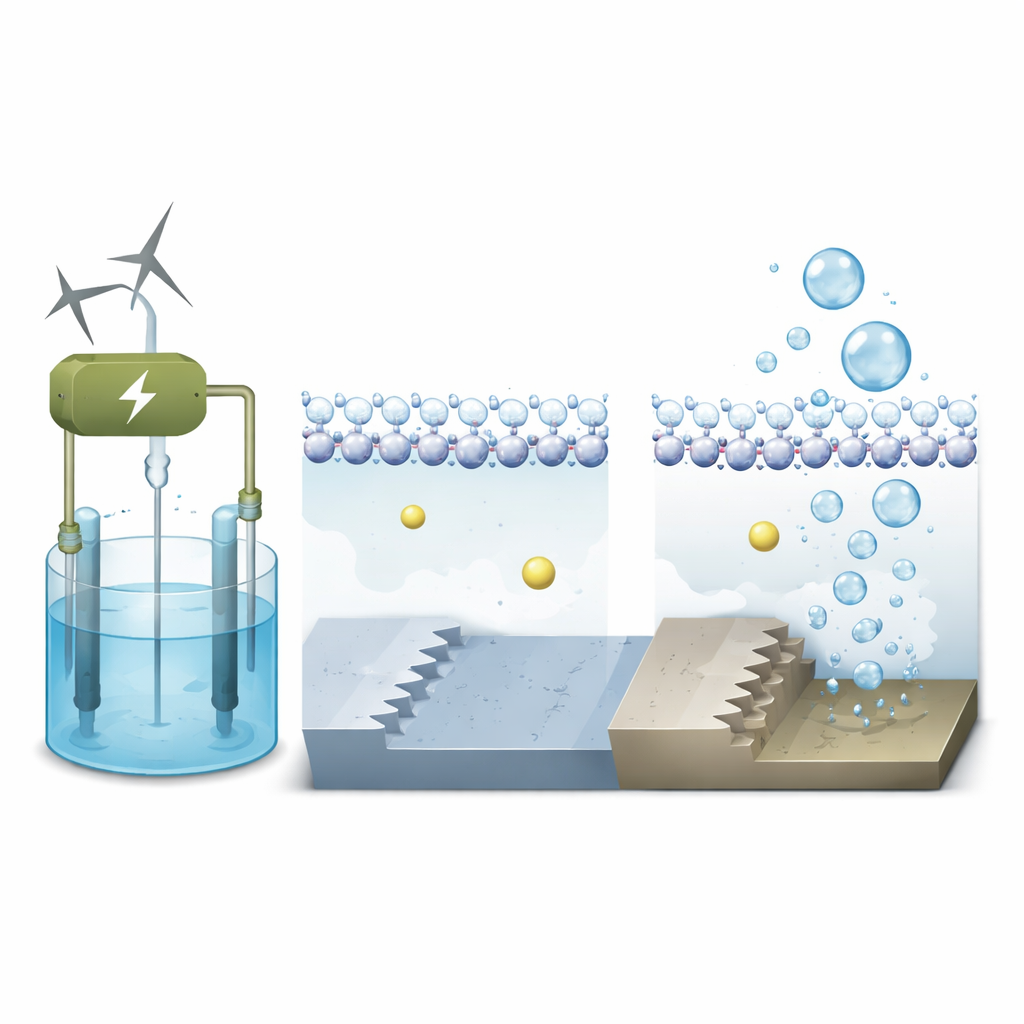
Les ions de sel comme aides cachées
Dans les électrolyseurs alcalins, le liquide contient des ions de métaux alcalins tels que le sodium. Ces ions chargés positivement ne se contentent pas de flotter ; ils peuvent s’accumuler près de l’électrode et remodeler subtilement le champ électrique à l’interface. Les simulations montrent que sur la terrasse de platine plate, l’eau forme une couche serrée et ordonnée avec les atomes d’hydrogène orientés vers la surface chargée négativement. Les ions sodium restent plus éloignés, séparés du métal par cette couche d’eau, de sorte que leur influence sur la réaction est modeste. Sur la surface escarpée, en revanche, les atomes sous‑coordonnés au bord des marches lient l’eau plus fortement et créent une structure d’eau locale plus rugueuse et désordonnée.
Un amas proche de la surface qui attire les ions
Aux arêtes de ces marches, l’équipe découvre un motif structurel récurrent : une molécule d’eau directement liée au pas de platine qui, à son tour, retient un ion sodium voisin entouré d’autres molécules d’eau. Ce petit agrégat platine–eau–sodium attire l’ion d’environ 2,3 angströms plus près du métal que sur la surface plate. Cette proximité renforce considérablement le champ électrique local dans cette zone minuscule, ce qui polarise fortement les molécules d’eau voisines. Les simulations révèlent qu’une liaison O–H dans ces molécules d’eau s’étire plus que d’habitude, indiquant qu’elle est partiellement prête à se rompre avant même que la réaction ne progresse formellement.
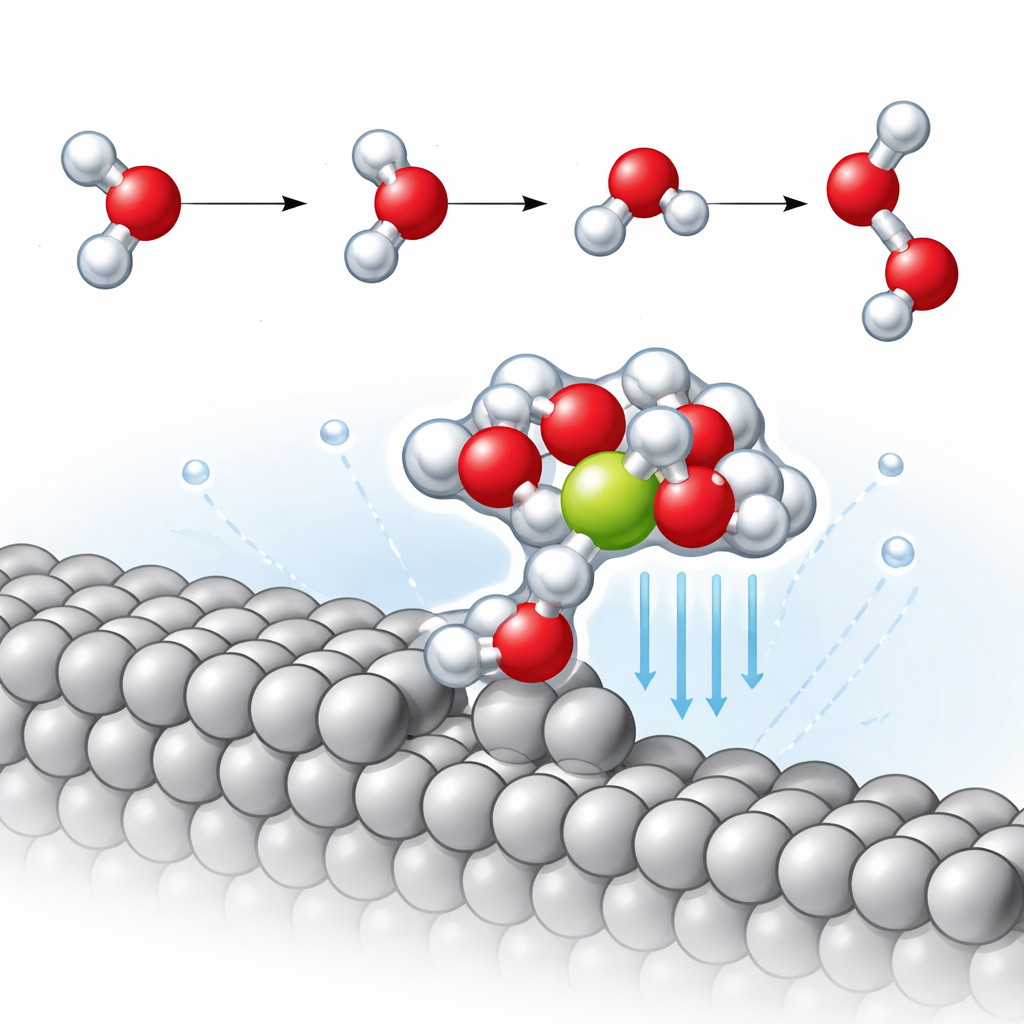
Abaisser la barrière de formation de l’hydrogène
L’étape clé et lente de l’évolution de l’hydrogène en milieu alcalin est connue sous le nom d’étape de Volmer, où une molécule d’eau se scinde : l’hydrogène se lie au métal tandis que l’hydroxyde restant migre dans le liquide. En retraçant la trajectoire réactionnelle de moindre énergie, les auteurs constatent que sur la surface de platine plate, le sodium n’a qu’un effet faible sur la barrière énergétique de cette étape. En revanche, sur la surface escarpée, l’amas stabilisé par le sodium abaisse l’énergie d’activation d’environ 0,14 électronvolt — soit à peu près trois fois l’amélioration observée sur la facette plate. Une analyse détaillée des mouvements vibrationnels montre que la liaison O–H orientée vers la surface devient sensiblement plus faible en présence de l’ion proche, ce qui facilite sa rupture et accélère ainsi la formation d’hydrogène.
Une règle de conception pour de meilleurs catalyseurs d’hydrogène
Globalement, l’étude conclut que les meilleures performances pour la production d’hydrogène en milieu alcalin ne proviennent ni uniquement de la surface métallique ni uniquement de l’électrolyte, mais de leur synergie. Les sites de platine escarpés capables d’ancrer des amas eau–ion particuliers rapprochent les cations alcalins, intensifient le champ électrique local, pré‑affaiblissent partiellement les liaisons d’eau et accélèrent fortement la première étape cruciale de l’évolution de l’hydrogène. Pour un lecteur non spécialiste, la conclusion est que, en sculptant soigneusement la forme microscopique des surfaces catalytiques et en choisissant des électrolytes qui amènent les bons ions aux bons endroits, les ingénieurs peuvent surmonter certaines des lenteurs fondamentales des dispositifs alcalins et concevoir des systèmes plus efficaces et économes en énergie pour la production d’hydrogène propre.
Citation: Zhang, Q., Sun, P., Li, H. et al. Synergistic cation-facet effects boost alkaline hydrogen evolution kinetics on stepped Pt surfaces. Commun Chem 9, 113 (2026). https://doi.org/10.1038/s42004-026-01924-9
Mots-clés: évolution de l’hydrogène, électrolyse alcaline, catalyseur au platine, eau interfaciale, cations des métaux alcalins