Clear Sky Science · fr
Base structurale de la formation de filaments de RegⅢα humain
Comment nos intestins combattent les germes
Nos intestins sont constamment exposés à des milliards de bactéries, dont beaucoup sont inoffensives voire bénéfiques. Mais lorsqu’apparaissent des microbes dangereux, notre organisme a besoin de moyens rapides et précis pour les attaquer sans endommager ses propres tissus. Cette étude examine de près l’un de ces protéines de défense naturelle, appelée RegIIIα, et révèle comment elle change de conformation pour tuer les bactéries puis bascule en une forme moins agressive et plus sûre. Comprendre cet acte de métamorphose pourrait aider les chercheurs à mieux saisir comment nous maintenons l’équilibre de la flore intestinale et ce qui se dérègle dans la maladie.
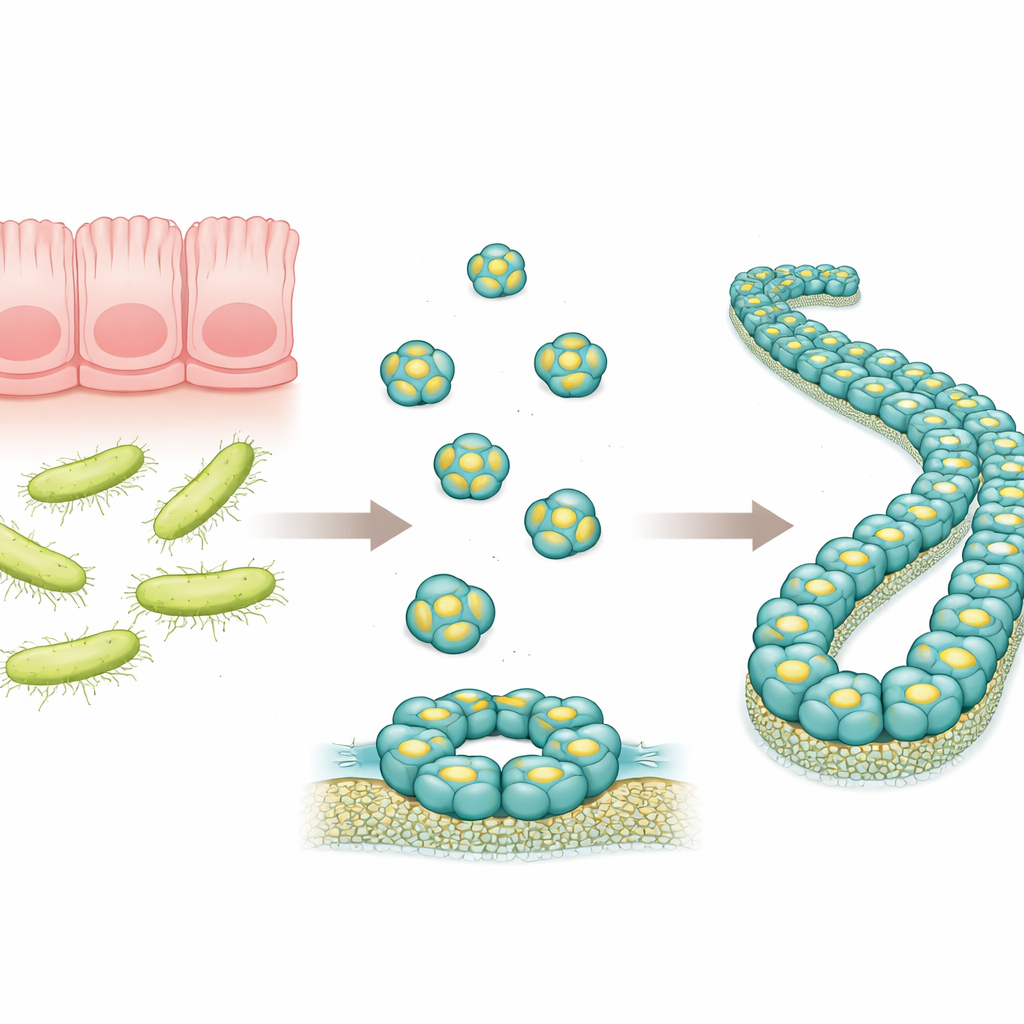
Un petit défenseur dans l’intestin
RegIIIα est une protéine produite dans le tube digestif qui cible certaines bactéries, en particulier celles à paroi externe épaisse connues sous le nom de bactéries à Gram positif. Des travaux antérieurs suggéraient que RegIIIα peut perforer les membranes bactériennes en formant des structures annulaires, permettant le contenu microbien de fuir et conduisant à la mort. Les chercheurs avaient aussi observé que, avec le temps, ces anneaux peuvent s’empiler en longs filaments, ce qui semble réduire le pouvoir létal de la protéine. Cependant, l’agencement exact des molécules de RegIIIα dans ces assemblages plus larges n’était pas connu en détail, rendant difficile la compréhension du fonctionnement de la protéine et de la manière dont son activité est régulée.
Observer le filament au détail atomique
Dans cette étude, les auteurs ont produit la RegIIIα humaine dans des bactéries puis l’ont incitée à s’assembler en filaments dans des conditions contrôlées. Ils ont utilisé une méthode d’imagerie puissante appelée cryomicroscopie électronique, qui permet de visualiser des molécules biologiques congelées dans une fine couche de glace à une résolution quasi atomique. Ils ont constaté que les filaments sont constitués d'ensembles répétitifs de trois unités identiques de RegIIIα, appelées trimères, qui s’empilent selon un motif hélicoïdal régulier. Chaque molécule individuelle de RegIIIα ressemble beaucoup à ce qui avait été observé auparavant dans des structures cristallines, mais leur orientation au sein du filament diffère de celle d’un modèle antérieur de résolution plus faible. Cette réorientation corrigée modifie la façon dont les chercheurs pensent que la protéine interagit avec les membranes bactériennes et avec son propre segment régulateur.
Comment les protéines se lient et pourquoi les lipides comptent
En examinant la structure de près, les chercheurs ont identifié deux régions de contact principales, ou interfaces, où les molécules voisines de RegIIIα se touchent et maintiennent le filament ensemble. Ils ont ensuite modifié des acides aminés spécifiques à ces interfaces et montré que ces altérations empêchaient la formation de filaments, confirmant que ces sites de contact sont essentiels. Fait intéressant, dans les deux interfaces, les cartes cryo-EM ont révélé des régions floues supplémentaires qui représentent probablement de petites molécules allongées coincées entre les surfaces protéiques. Leur forme et leur environnement chimique suggèrent qu’il peut s’agir de lipides, les mêmes types de molécules huileuses qui composent les membranes cellulaires. Cela corrobore des indices antérieurs selon lesquels les lipides favorisent l’assemblage de RegIIIα, peut-être en agissant comme une colle moléculaire qui stabilise les connexions entre sous-unités.
L’interrupteur marche–arrêt : le pH et un segment caché
L’équipe a également étudié ce qui contrôle l’assemblage de RegIIIα. Avant d’être active, la protéine porte un court « pro-segment » qui doit être coupé par des enzymes digestives. Dans leur structure de filament à haute résolution, il n’y a pas d’espace au centre de l’assemblage pour loger cette pièce supplémentaire, ce qui implique que le pro-segment empêche la capacité de RegIIIα à former les anneaux perforants et les filaments dès le départ. Ils ont constaté que la tendance à former des filaments dépend aussi de l’acidité : les filaments se forment facilement à un pH similaire à celui de l’intestin grêle mais mal à un pH plus acide. Un seul acide aminé, l’histidine 50, semble agir comme un interrupteur sensible au pH ; lorsqu’il est remplacé par un autre résidu, la formation de filaments devient beaucoup moins dépendante du pH. Ensemble, ces caractéristiques — clivage enzymatique, liaison aux lipides et pH — créent un système de régulation à plusieurs niveaux qui ajuste quand et où RegIIIα est actif.
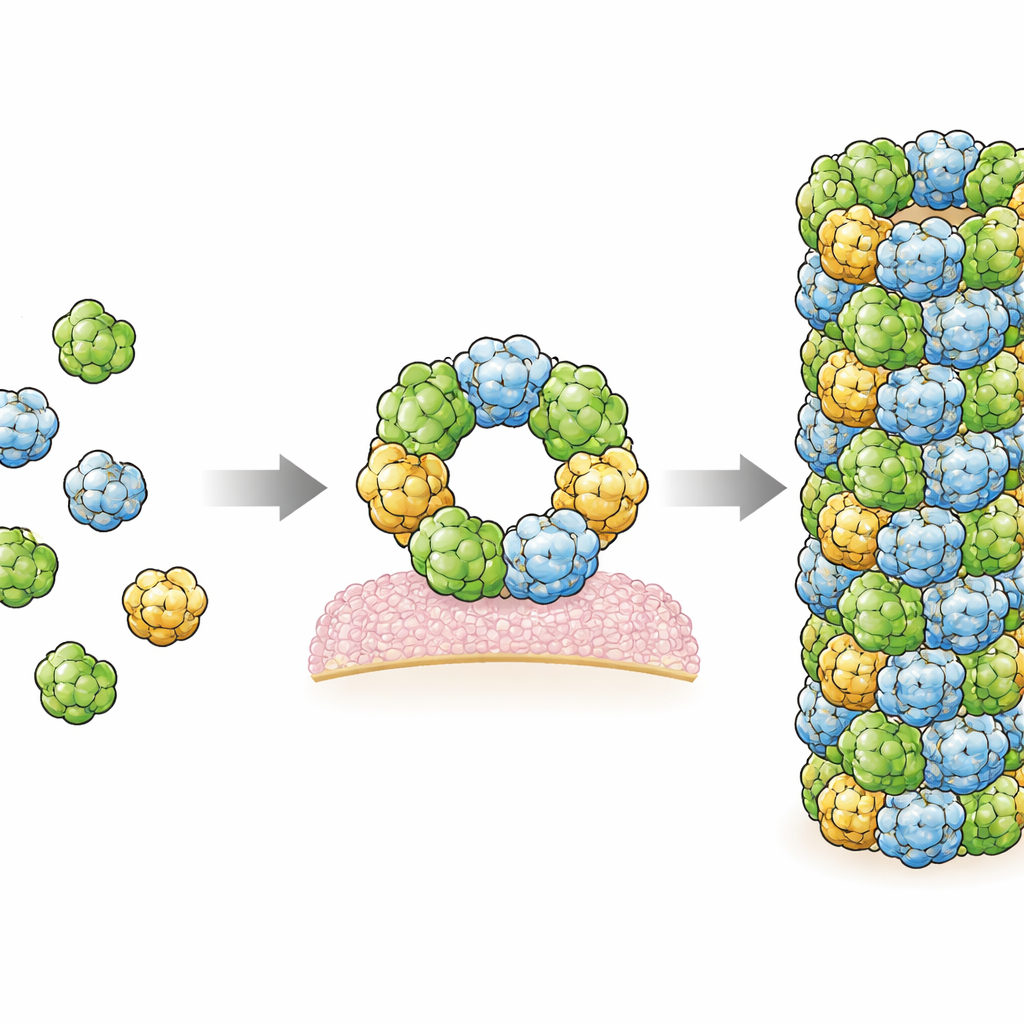
Ce que cela signifie pour la santé intestinale
Globalement, ce travail fournit l’image la plus détaillée à ce jour de la manière dont les molécules de RegIIIα s’assemblent en structures plus grandes liées à la fois à leur action antibactérienne et à leur comportement auto-limitant. Les mêmes interfaces qui forment les filaments construisent aussi les anneaux hexamériques supposés créer des pores dans les membranes bactériennes, suggérant un équilibre délicat entre une forme de forte activité létale et un état plus sûr et atténué. Cartographier les mutations associées à des maladies sur cette structure montre que beaucoup se situent à des points de contact clés, ce qui suggère que des perturbations de l’assemblage peuvent être à l’origine de certains troubles intestinaux ou pancréatiques. En clarifiant comment cet antibiotique naturel est activé, guidé par les lipides et modelé par le pH local, l’étude jette les bases d’efforts futurs visant à moduler nos défenses innées — soit en les renforçant contre l’infection, soit en les calmant lorsqu’elles sont déréglées.
Citation: Han, J., Cao, Q. Structural basis for human RegⅢα filament formation. Commun Chem 9, 117 (2026). https://doi.org/10.1038/s42004-026-01921-y
Mots-clés: RegIIIα, immunité intestinale, cryomicroscopie électronique, filaments protéiques, peptides antibactériens