Clear Sky Science · fr
Glycosides amphiphiles ionisables en pont azobenzène pour une délivrance de pDNA contrôlée par la lumière, mono-composante et modulable selon l’organe
Éclairer la voie d’une délivrance génique plus intelligente
Les thérapies géniques promettent de traiter les maladies à la source en apportant des fragments de code génétique directement dans nos cellules. Mais guider ce chargement fragile en toute sécurité dans le flux sanguin, vers les bons organes, puis à l’intérieur des cellules cibles reste un obstacle majeur. Cette étude présente une nouvelle classe de particules microscopiques à base de sucres dont le comportement peut être commuté par la lumière avant même leur entrée dans l’organisme, permettant aux chercheurs de rediriger où un gène thérapeutique se retrouve et quelle intensité d’expression il induit, tout en préservant largement l’intégrité cellulaire. 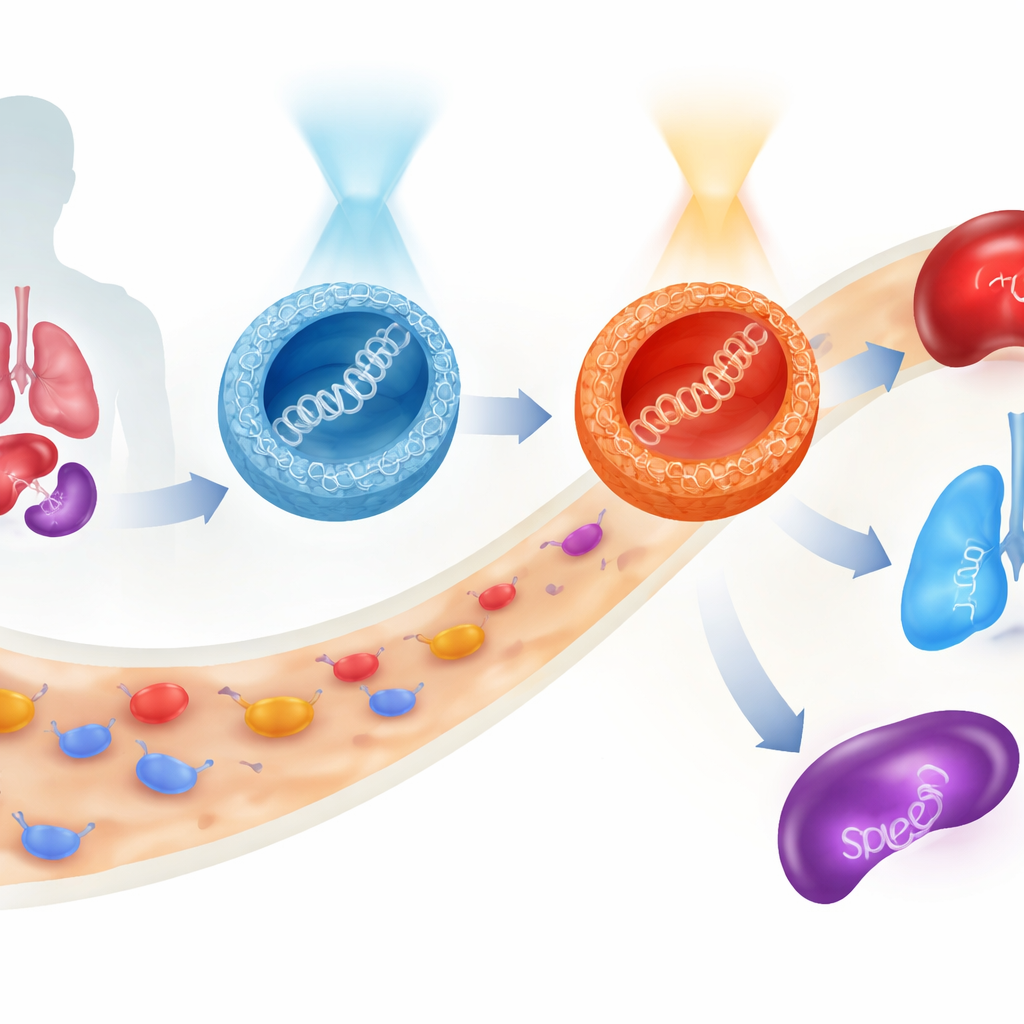
Le besoin de coursiers génétiques précis
Les véhicules de livraison génique les plus performants aujourd’hui sont les nanoparticules lipidiques, qui ont contribué à rendre possibles les vaccins à ARNm contre la COVID-19. Ces gouttelettes multi-composants enveloppent et protègent les acides nucléiques, mais elles ont tendance à s’accumuler principalement dans le foie et ne libèrent qu’une petite fraction de leur cargaison à l’intérieur des cellules. Ajuster leur composition peut modifier les organes ciblés, mais les mélanges sont complexes et difficiles à contrôler précisément. L’équipe à l’origine de ce travail a donc choisi de concevoir des molécules uniques et bien définies qui s’auto-assemblent en nanoparticules de formes et de comportements prévisibles — et qui peuvent être activement modulées de l’extérieur par un simple déclencheur lumineux.
Une bascule moléculaire contrôlée par la lumière
Au cœur du nouveau système se trouvent des glycosides « Janus » doubles : des molécules constituées de deux unités de glucose, dotées de têtes chargées hydrophiles et de queues lipophiles, reliées par une « charnière » centrale en azobenzène. L’azobenzène peut basculer entre deux conformations miroir, appelées E et Z, lorsqu’il est exposé à différentes longueurs d’onde lumineuses. En présence d’ADN dans l’eau, de nombreuses copies de ces molécules s’assemblent spontanément en particules souples et stratifiées qui enrobent les brins d’ADN plasmidique. Les chercheurs ont préparé deux variantes — l’une avec des liaisons oxygène et l’autre avec des liaisons soufre entre le sucre et la charnière — pour ajuster finement la stabilité et le comportement biologique. En pré-irradant les solutions, ils ont pu enrichir la forme E ou Z et étudier comment chaque état influence les particules de délivrance génique obtenues.
Comportement des particules métamorphes
Les mesures de la taille des particules, de la charge de surface et de la structure interne ont montré que la commutation induite par la lumière entre les états E et Z a des conséquences physiques nettes. En général, la forme Z engendrait des nanoparticules plus petites, de morphologie plus uniforme et à intérieur plus ordonné et stratifié que la forme E. La microscopie a révélé que ces agencements internes ressemblent à des feuilles alternées de matériau de type lipidique et d’ADN. Fait important, les deux états protégeaient l’ADN contre la dégradation enzymatique. Dans des cultures cellulaires issues de rein, de foie et de tissus immunitaires, les différents isomères ont produit des niveaux d’expression génique nettement différents, bien que l’ADN lui-même fût identique. Des impulsions lumineuses répétées appliquées après l’entrée des particules dans les cellules ont multiplié l’expression génique, ce qui suggère que le choc mécanique lié à la commutation aide les particules à se détendre et à libérer leur cargaison, et peut aussi favoriser leur sortie de compartiments intracellulaires. 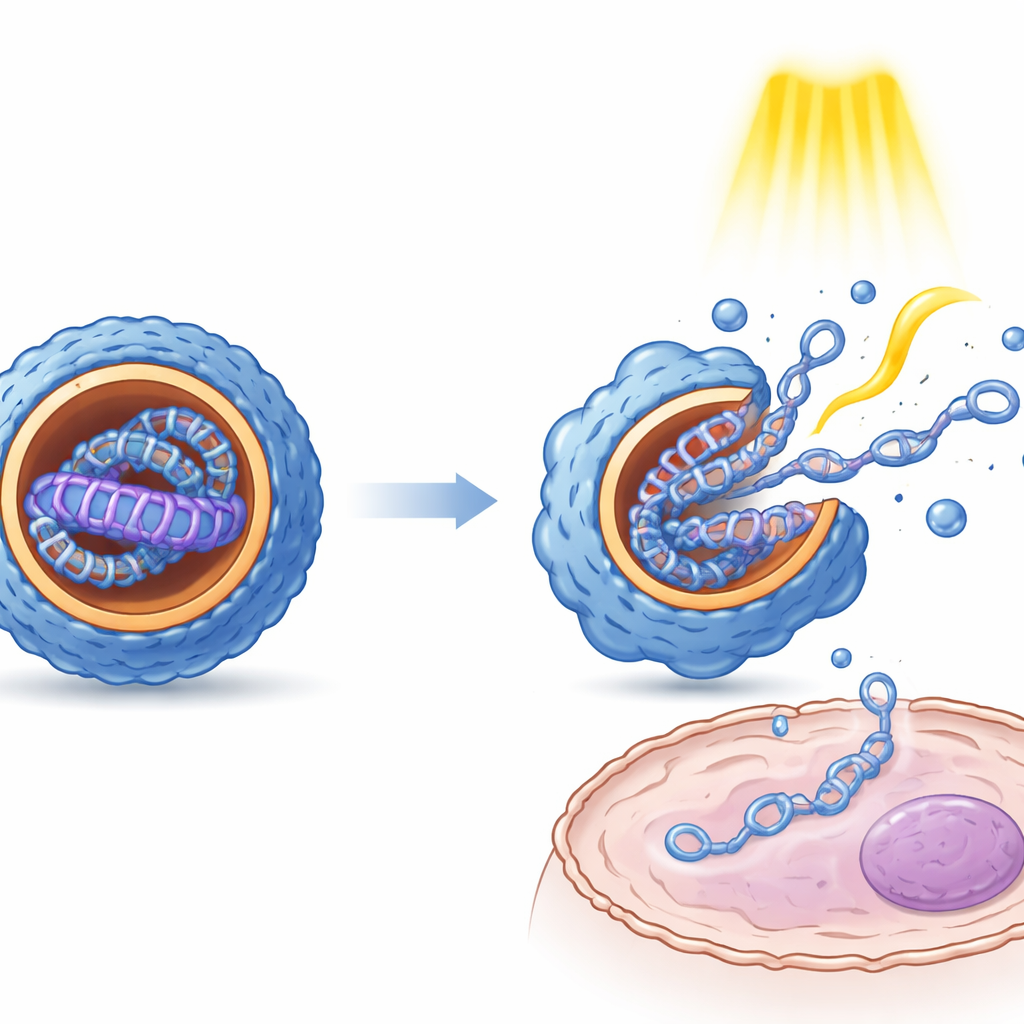
Orienter les gènes vers des organes spécifiques
Le comportement le plus surprenant est apparu chez la souris. Lorsque les particules oxygénées étaient administrées sous leur forme riche en E, l’expression d’un gène marqueur se produisait principalement dans le foie avec une part dans les poumons. Les précommuter en forme Z avant l’injection augmentait non seulement l’expression totale, mais déplaçait aussi l’équilibre en faveur des poumons. Les particules avec liaison soufre ont donné un résultat différent : leur forme Z favorisait la rate, un organe clé du système immunitaire. Ainsi, avec le même cadre moléculaire de base — et sans changer la cargaison d’ADN — les chercheurs ont pu diriger l’activité génique principalement vers le foie, les poumons ou la rate simplement en choisissant la liaison (oxygène ou soufre) et la conformation activée par la lumière (E ou Z) du transporteur. Tout au long de ces expérimentations, la viabilité cellulaire est restée élevée, ce qui suggère que le système est relativement doux.
Une voie modulable par la lumière pour les médicaments géniques futurs
En termes simples, l’équipe a construit une navette minuscule et commutable par la lumière pour l’ADN. Avant l’injection, un bref traitement lumineux « programme » ces navettes dans l’une des deux conformations. Chaque forme s’assemble en nanoparticules avec une taille et une sensation de surface caractéristiques, ce qui détermine ensuite leur affinité pour différents types cellulaires et leur destination dans l’organisme. Parce que le même échafaudage chimique peut être modifié de nombreuses petites façons, et parce que la commutation est réversible et n’altère pas l’ADN lui-même, cette plateforme offre un moyen flexible d’ajuster où et comment les thérapies géniques agissent. Bien que de nombreux travaux restent nécessaires avant une utilisation clinique, l’étude montre que des transporteurs mono-moléculaires soigneusement conçus et contrôlés par la lumière pourraient devenir des outils puissants pour des médicaments génétiques plus sûrs et plus précis.
Citation: Wang, Z., Rivero-Barbarroja, G., Benito, J.M. et al. Azobenzene-bridged ionizable amphiphilic Janus glycosides for light-controlled, single-component and organ-modulable pDNA delivery. Commun Chem 9, 118 (2026). https://doi.org/10.1038/s42004-026-01920-z
Mots-clés: livraison de gènes, nanoparticules sensibles à la lumière, interrupteurs azobenzène, thérapie ciblée par ADN, nanomédecine