Clear Sky Science · fr
Transfert de proton ultrarapide du solvant au soluté médié par des vibrations cohérentes intermoléculaires
Comment les molécules dissipent le stress induit par la lumière
Lorsque des molécules absorbent de la lumière ultraviolette, elles peuvent emmagasiner plus d’énergie qu’il ne leur est favorable. Si cette énergie n’est pas relâchée rapidement, elle peut rompre des liaisons chimiques et endommager des matériaux voire l’ADN. Cette étude examine comment une classe particulière de molécules, une « photobase », transfère un minuscule noyau d’hydrogène — un proton — depuis le liquide environnant pour se protéger en l’espace de trillionièmes de seconde. Comprendre cette danse entre la molécule et son environnement liquide pourrait aider les scientifiques à concevoir de meilleurs capteurs activés par la lumière, des catalyseurs et des revêtements protecteurs.
Un petit proton en mouvement
Au cœur du travail se trouve une molécule appelée 2-(2′-pyridyl)benzimidazole, ou PBI, dissoute dans le méthanol, un alcool simple. La PBI peut capter un proton du solvant lorsqu’elle est excité par la lumière, se comportant comme une base plus forte uniquement dans son état énergisé. Les chercheurs ont utilisé des impulsions laser extrêmement rapides pour stimuler la PBI par ultraviolet puis ont surveillé, en temps réel, comment son absorption de la lumière évoluait au fur et à mesure de sa relaxation. Ces changements subtils de couleur dans les mesures révèlent quand et comment les protons se déplacent et comment le liquide environnant réagit.
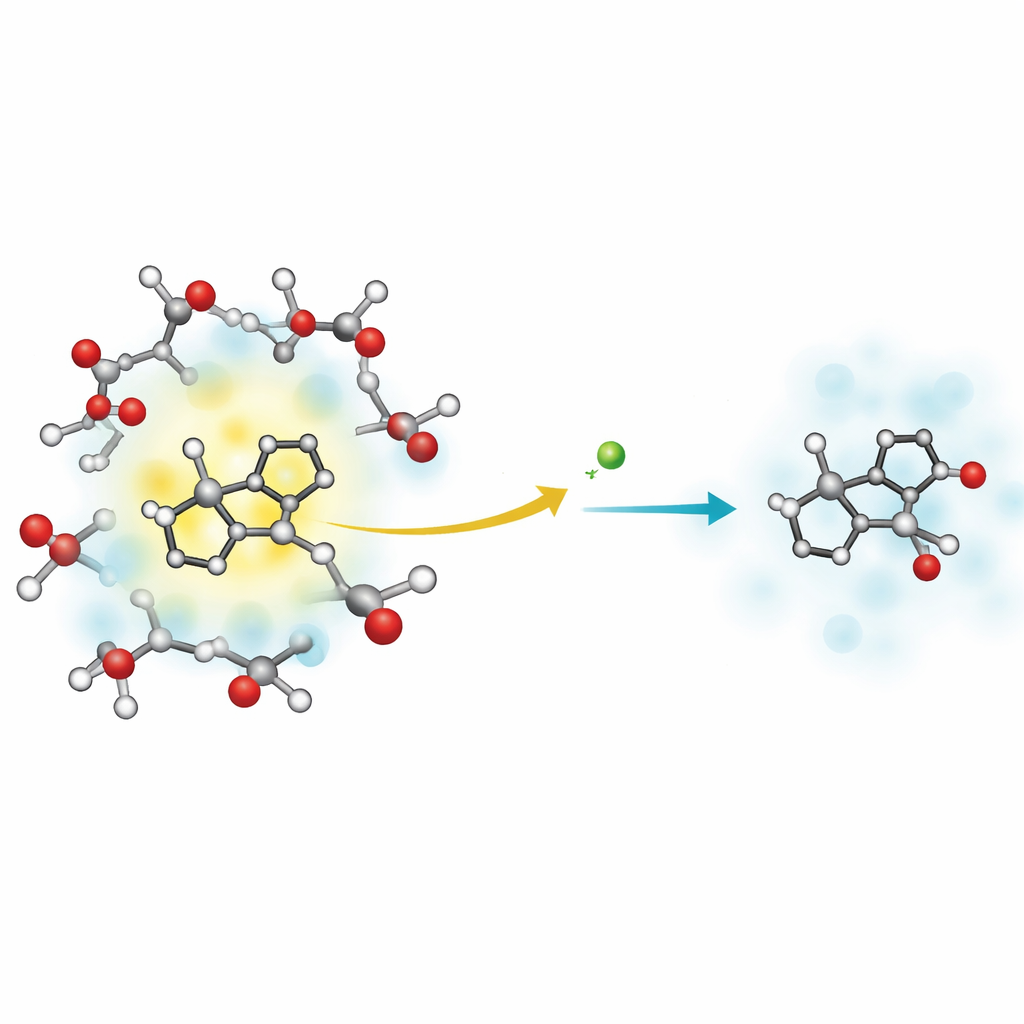
Trois étapes de libération d’énergie
Les mesures montrent que le système excité PBI–méthanol se relaxe en trois étapes distinctes. D’abord, en environ 2,2 picosecondes (deux billièmes de seconde), un proton passe d’une molécule de méthanol vers un site azoté de la PBI. Il s’agit de l’étape clé de transfert de proton du solvant au soluté, où l’environnement fait don d’un proton à la molécule excitée. Ensuite, sur environ 31 picosecondes, la PBI nouvellement protonée retombe dans son état fondamental électronique sans émettre de lumière, transférant son excès d’énergie vers des vibrations. Enfin, sur environ 186 picosecondes, cette énergie vibrationnelle s’évacue progressivement dans le méthanol environnant, ramenant la molécule et le solvant à l’équilibre thermique.
Des vibrations cachées qui guident la réaction
Pour zoomer sur les instants les plus précoces après l’impulsion lumineuse, l’équipe a enregistré les données avec des pas de temps beaucoup plus fins à l’échelle des femtosecondes (un millionième d’un milliardième de seconde). Après avoir retiré la tendance globale de décroissance, ils ont mis en évidence un motif d’oscillations faible mais régulier dans le signal — preuve que les atomes de la paire PBI–méthanol vibraient de manière coordonnée. Deux périodes vibratoires principales sont apparues : environ 117 femtosecondes et 340 femtosecondes. Des calculs ont montré qu’elles correspondent à des mouvements de basse fréquence qui torsadent et fléchissent à la fois l’ossature de la PBI et la molécule de méthanol attachée, remodelant en permanence la liaison hydrogène qui les relie. Ces mouvements modulent la distance et l’alignement entre le donneur et l’accepteur de proton, orientant effectivement le proton le long de son trajet. Les oscillations s’atténuaient en moins de 300 femtosecondes, ce qui suggère que le système passe rapidement à un paysage énergétique plus accidenté en montant vers et en franchissant la barrière réactionnelle.
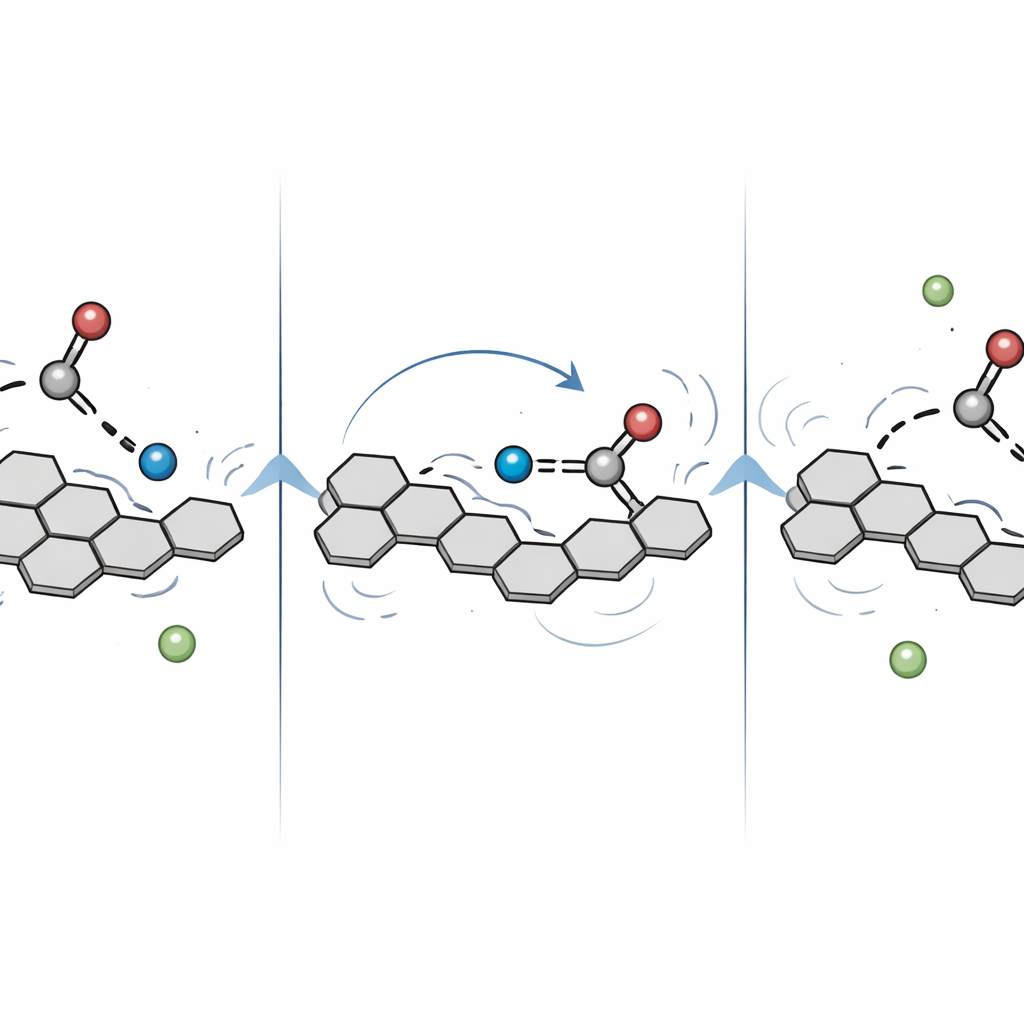
Pourquoi cette voie est importante
La modélisation par calcul a corroboré le tableau expérimental. À l’aide de méthodes de chimie quantique, les auteurs ont calculé le paysage énergétique pour plusieurs trajectoires réactionnelles possibles. La voie dans laquelle le proton se déplace directement du méthanol vers la PBI présente une barrière relativement basse et conduit à un produit plus stable qu’une route alternative où un atome d’hydrogène serait transféré différemment. Les absorptions en état excité simulées pour le produit de transfert de proton favorisé correspondaient aux spectres observés, renforçant la conclusion selon laquelle un transfert de proton direct, plutôt qu’un déplacement plus complexe d’un atome d’hydrogène, domine dans ces conditions.
Ce que cela signifie pour les matériaux actifs à la lumière
Globalement, l’étude montre que le transfert de proton du solvant au soluté dans cette photobase n’est pas un simple saut isolé, mais qu’il est imbriqué avec des vibrations coordonnées de la molécule et de son partenaire liquide. Ces mouvements ultrarapides contribuent à établir la géométrie propice au mouvement du proton et influencent la rapidité avec laquelle le système peut se débarrasser de son excès d’énergie. Pour un lecteur non spécialiste, l’idée principale est que les chimistes apprennent à observer et à comprendre comment la matière se protège de la lumière, un proton et une vibration à la fois. Des connaissances comme celles-ci pourraient orienter la conception de matériaux intelligents réactifs à la lumière — des molécules qui s’activent ou se désactivent, catalysent des réactions ou protègent des composants sensibles — en tirant parti, plutôt qu’en combattant, le mouvement incessant des atomes dans les liquides.
Citation: Jarupula, R., Mao, Y. & Yong, H. Ultrafast solvent-to-solute proton transfer mediated by intermolecular coherent vibrations. Commun Chem 9, 111 (2026). https://doi.org/10.1038/s42004-026-01917-8
Mots-clés: transfert de proton ultrarapide, photobase, cohérence vibrationnelle, spectroscopie d’absorption transitoire, interactions soluté–solvant