Clear Sky Science · fr
La protéase S9 WprP2 catalyse une coupure uniforme du peptide précurseur dans la biosynthèse des RiPP
Pourquoi de petits outils de découpe dans les cellules comptent
À l’intérieur des bactéries, des ciseaux moléculaires spécialisés coupent de longues chaînes d’acides aminés en fragments plus petits et actifs qui deviennent souvent des antibiotiques ou d’autres produits naturels utiles. Cette étude met au jour un outil de découpe jusque‑là inconnu — une protéase nommée WprP2 — qui taille son peptide cible avec une précision inhabituelle. Comprendre le fonctionnement de cette enzyme pourrait aider les scientifiques à concevoir de nouveaux peptides bioactifs et des antibiotiques de nouvelle génération.
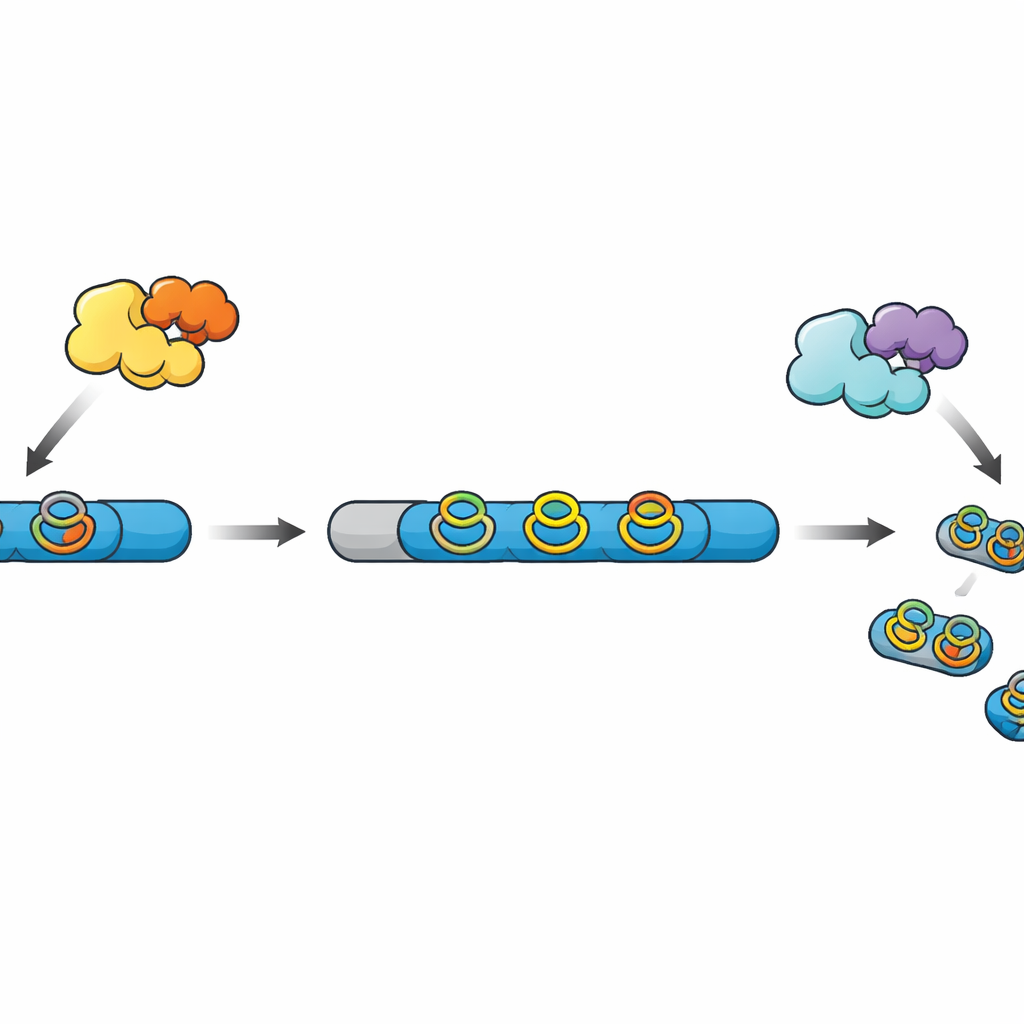
Des chaînes brutes aux mini‑médicaments finis
De nombreux produits naturels modernes à base de peptides, regroupés sous le terme RiPP, commencent comme de simples chaînes synthétisées sur le ribosome. Ces chaînes contiennent une région leader qui sert de poignée et une région cœur qui deviendra le produit final après une série de modifications chimiques. D’autres enzymes ajoutent des pontages et des anneaux qui rendent le peptide plus stable et plus actif, puis une protéase coupe la région leader et libère la molécule mature. Dans une famille de RiPP récemment découverte, des enzymes radical SAM construisent des anneaux compacts « cyclophanes » impliquant des acides aminés aromatiques, mais dans la plupart des clusters de gènes connus, la protéase correspondante manque, laissant mystérieuses les étapes finales du traitement.
À la recherche d’un enzyme partenaire manquant
Les auteurs avaient auparavant étudié une enzyme radical SAM nommée WprB1 qui installait des pontages identiques sur trois segments WPR répétés d’un peptide précurseur. Dans le nouveau travail, ils ont parcouru des génomes bactériens à la recherche de parents de cette enzyme et cherché à proximité d’éventuels gènes codant pour une protéase. Dans Streptomyces venezuelae, ils ont trouvé un cluster prometteur contenant une enzyme de pontage similaire, sa protéine auxiliaire, un peptide précurseur apparié avec trois répétitions WPR, et une protéase candidate de la famille S9, qu’ils ont nommée WprP2. Ce système constituait un banc d’essai idéal pour élucider comment le peptide est finalement coupé pour libérer les fragments actifs.
Observer le peptide être découpé
Pour sonder WprP2, l’équipe a produit le peptide précurseur dans des bactéries, avec et sans l’enzyme de pontage, l’a purifié, puis l’a mélangé avec la protéase dans des réactions in vitro contrôlées. La spectrométrie de masse a révélé que WprP2 clive d’abord la chaîne immédiatement après chaque segment WPR, puis effectue une seconde coupure à une distance fixe en amont d’une proline particulière plus loin dans la séquence. Ces deux étapes créent une série de fragments plus petits et uniformes. Fait remarquable, WprP2 a exécuté ce schéma de coupures que les anneaux cyclophanes aient déjà été installés ou non, montrant que ces anneaux ne sont pas nécessaires à la reconnaissance. Comparée à la trypsine commerciale, qui ne peut pas couper en certains sites pontés, WprP2 fonctionnait toujours, soulignant sa robustesse inhabituelle.
Décoder ce que l’enzyme reconnaît
Les chercheurs se sont ensuite demandé quelles caractéristiques du peptide WprP2 lit réellement. En modifiant systématiquement des acides aminés individuels autour des sites de coupure, ils ont constaté que changer de nombreux résidus voisins avait peu d’effet, mais que la substitution d’une arginine clé au sein du segment WPR ou de la glutamine ou de la proline au deuxième site de coupure pouvait bloquer cette étape particulière. Des expériences avec un peptide précurseur apparenté portant des résidus flanquants différents ont montré que la protéase coupait toujours après les répétitions WPR mais n’effectuait la seconde coupure que lorsqu’une paire glutamine‑proline était présente. Des modèles structurels générés par ordinateur avec AlphaFold3 ont soutenu ce tableau : dans les complexes prédits, les sites basés sur WPR et la paire glutamine‑proline s’alignaient chacun à leur tour sur le centre catalytique de l’enzyme, cohérents avec un mécanisme séquentiel en deux étapes.
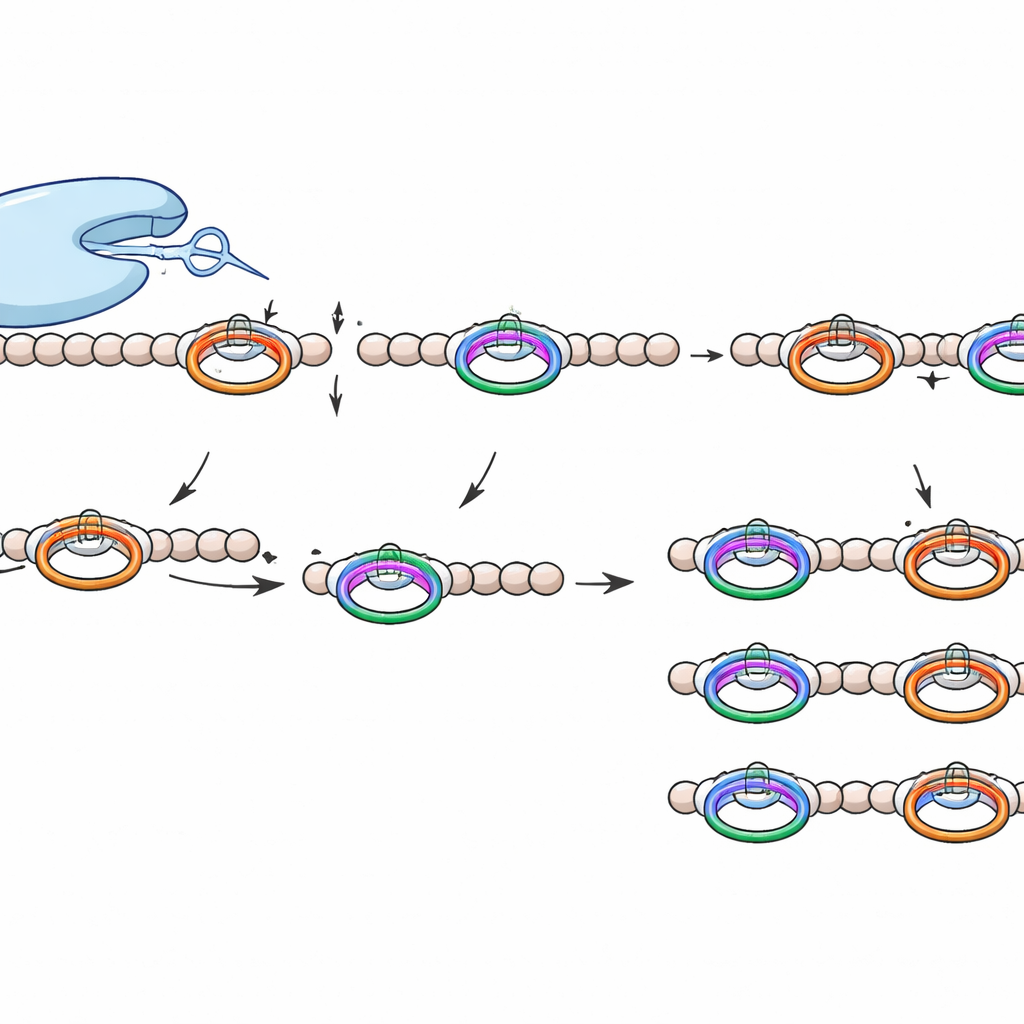
Ce qui rend cet outil de découpe spécial
WprP2 appartient à une large famille S9 de protéases qui inclut déjà des enzymes d’intérêt médical, mais elle se distingue à plusieurs égards. Elle coupe du côté N‑terminal d’une proline plutôt qu’après celle‑ci, elle agit sur un motif répété pour générer des fragments de taille uniforme sur l’ensemble de la chaîne précurseur, et elle montre une large tolérance aux acides aminés situés entre ses deux sites de reconnaissance. Cette combinaison de précision et de flexibilité n’avait pas été observée jusqu’ici chez les protéases liées aux RiPP.
Comment cette découverte pourrait être utilisée
En révélant une protéase qui reconnaît des indices de séquence simples et effectue des coupures répétées et uniformes, ce travail ajoute un nouvel outil puissant à la boîte à outils croissante de l’ingénierie peptidique. Sur le plan pratique, WprP2 pourrait être exploitée pour libérer ou remodeler des peptides conçus, y compris ceux portant des pontages complexes qui résistent aux enzymes standard comme la trypsine. Pour les non‑spécialistes, l'essentiel est que les scientifiques ont découvert une nouvelle sorte de ciseaux moléculaires qui coupe de longues chaînes peptidiques en morceaux précis et de taille égale, ouvrant la voie à une production mieux contrôlée d’éventuels antibiotiques et autres molécules bioactives.
Citation: Haedar, J.R., Khan, A.H., Ma, S. et al. S9 protease WprP2 catalyzes uniform cleavage on the precursor peptide in RiPP biosynthesis. Commun Chem 9, 108 (2026). https://doi.org/10.1038/s42004-026-01915-w
Mots-clés: Peptides RiPP, protéase à sérine, WprP2, produits naturels cyclophanes, ingénierie peptidique