Clear Sky Science · fr
Sonde d'émission induite par confinement stérique pour surveiller les conformations protéiques dans des cellules vivantes
Observer en temps réel des protéines qui changent de forme
À l'intérieur de chaque cellule vivante, les protéines modifient en permanence leur conformation pour transmettre des signaux, sonder leur environnement et accomplir des fonctions vitales. De nombreuses maladies résultent d'anomalies de ces changements de forme, mais il a été remarquablement difficile d'observer directement ces mouvements dans des cellules vivantes, notamment sur des échelles de temps très rapides comme lentes. Cet article présente une nouvelle sonde émettrice de lumière, baptisée BIOSCE, qui convertit de minuscules mouvements protéiques en éclats visibles, permettant aux chercheurs de suivre des protéines individuelles lorsqu'elles se plient, se tordent et interagissent en temps réel à l'intérieur de cellules vivantes. 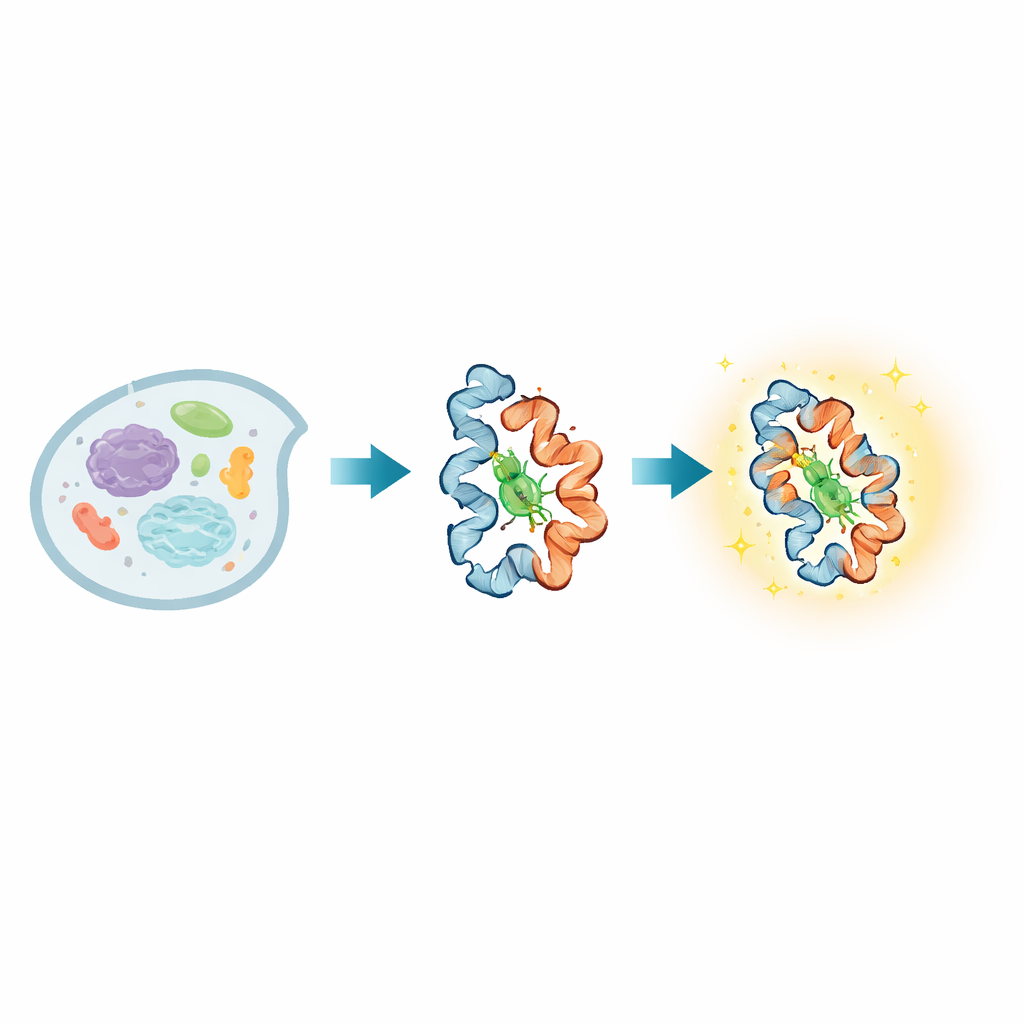
Un nouvel interrupteur lumineux pour les protéines en mouvement
Au cœur de BIOSCE se trouve une petite molécule colorante, MTPABP-Cl, qui devient plus lumineuse lorsqu'elle est comprimée. Les auteurs fixent ce colorant à une balise protéique largement utilisée, HaloTag, qui peut être fusionnée génétiquement à presque n'importe quelle protéine d'intérêt. Lorsque la protéine marquée change de conformation ou se compacte davantage avec ses voisines, elle modifie l'espace disponible pour le colorant et donc sa capacité à bouger. Dans un environnement lâche, les parties internes du colorant peuvent tourner librement et la majeure partie de la lumière absorbée est dissipée par le mouvement ; dans une poche plus serrée ces mouvements sont bloqués et le colorant libère davantage cette énergie sous forme de lumière. Cette « émission induite par confinement stérique » convertit des variations subtiles de l'encombrement local autour d'une seule protéine en un changement progressif d'intensité, plutôt qu'en un signal tout-ou-rien, rendant la sonde très sensible aux petites variations conformationnelles.
Conception et test du colorant sensible à la compression
L'équipe a d'abord conçu et synthétisé MTPABP-Cl de sorte qu'il reste terne en solution mais s'éclaire lorsqu'il est immobilisé par HaloTag ou par une protéine de fusion plus compacte. Des mesures précises ont montré que le colorant absorbe la lumière bleue et émet dans le rouge lointain, ce qui est favorable pour l'imagerie en profondeur dans les cellules et pour l'observation à long terme. Lorsqu'il est lié uniquement à HaloTag, sa sortie lumineuse augmente ; lorsque HaloTag est fusionné à une protéine partenaire qui s'enroule autour du colorant, la luminosité s'accroît encore davantage. Des simulations informatiques ont confirmé que, dans des arrangements protéiques plus compacts, le colorant subit un encombrement plus important, une surface exposée plus petite et davantage de contacts stabilisants, qui restreignent le mouvement et renforcent l'émission. Le colorant se lie également de façon rapide et spécifique à HaloTag, présente un bruit de fond très faible dans les cellules dépourvues de la balise et reste non toxique aux concentrations d'utilisation, soutenant son emploi dans des expériences en cellules vivantes. 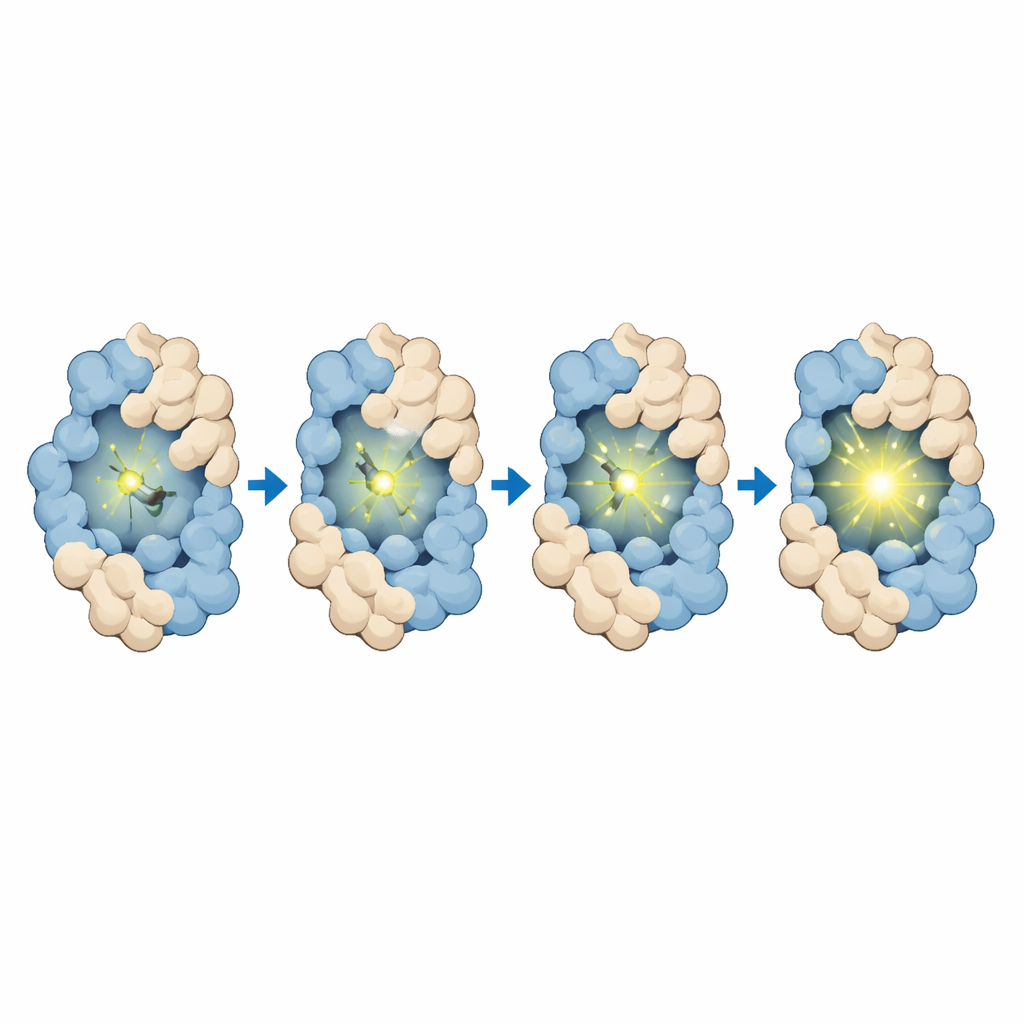
Suivre des signaux rapides et des rencontres protéiques
Pour démontrer les capacités de BIOSCE, les auteurs l'ont appliqué à plusieurs processus cellulaires bien connus. D'abord, ils ont adapté un capteur de calcium basé sur la calmoduline, une protéine qui change de conformation lorsqu'elle se lie aux ions calcium, essentiels pour la transmission nerveuse et de nombreux autres événements cellulaires. En fusionnant la calmoduline à HaloTag et en la marquant avec MTPABP-Cl, ils ont créé un indicateur chimigénétique nommé SCECaMP. Dans des cellules humaines et des cellules de type neuronal, cet indicateur s'est éclairci et est devenu plus faible en phase avec les pics de calcium déclenchés par une stimulation au potassium, avec des vitesses de réponse comparables aux protéines fluorescentes GCaMP largement utilisées. Parce que le signal BIOSCE dépend directement de l'encombrement local autour du colorant, il peut refléter fidèlement les changements structurels de la calmoduline tout en fournissant une fluorescence stable et durable adaptée à l'imagerie prolongée.
Visualiser des interactions induites par des médicaments et les dégâts toxiques
Les chercheurs ont ensuite testé si BIOSCE pouvait suivre la réunion de deux protéines provoquée par un médicament. Ils ont utilisé un système classique dans lequel la rapamycine rapproche deux partenaires, FKBP et FRB, au sein d'une voie de contrôle de la croissance. En attachant HaloTag soit à FKBP soit à FRB et en marquant avec MTPABP-Cl, ils ont observé des augmentations rapides de fluorescence à l'échelle des millisecondes lorsque la rapamycine induisait l'approche et la réorganisation de ces protéines. L'augmentation de luminosité reflétait un microenvironnement plus serré autour du colorant à mesure que les partenaires se rapprochaient. Dans un test plus complexe, ils ont étudié SNAP25, une protéine de la terminaison nerveuse cruciale pour la libération des neurotransmetteurs et la cible principale de la neurotoxine botulique A. En plaçant HaloTag de part et d'autre du site de coupure de la toxine et en marquant avec le colorant, ils ont pu suivre séparément les mouvements des fragments N-terminal et C-terminal après clivage. Le suivi de particules individuelles a révélé qu'un fragment restait ancré près de la membrane plasmique tandis que l'autre se diffusait plus librement dans le cytoplasme, et que le profil exact dépendait du moment du marquage par rapport à l'exposition à la toxine. La sonde a même rapporté des ajustements conformationnels rapides induits par le zinc dans SNAP25 durant ce processus.
Implications pour la biologie et la médecine
Dans l'ensemble, ces résultats montrent que BIOSCE est une nouvelle méthode polyvalente pour visualiser comment des protéines individuelles se déplacent, se replient et interagissent à l'intérieur de cellules vivantes sur une large gamme d'échelles temporelles. Parce que la méthode repose sur une fusion HaloTag générale et une seule petite molécule colorante, elle peut en principe être appliquée à de nombreuses protéines différentes sans redessiner entièrement le capteur à chaque fois. Le changement d'intensité continu, dépendant du confinement, permet aux chercheurs de détecter des variations structurelles subtiles plutôt que seulement de grands événements binaires. À l'avenir, les auteurs prévoient d'améliorer l'administration de la sonde et la profondeur d'imagerie afin que BIOSCE puisse être utilisé dans des tissus et des organismes entiers. Si cela réussit, cette approche pourrait devenir un outil puissant pour relier l'emplacement des protéines, leur dynamique et leur fonction en santé et en maladie, et alimenter finalement des modèles informatiques détaillés du comportement cellulaire.
Citation: Jia, H., Yang, L., Yang, Y. et al. Steric confinement-induced emission probe for monitoring protein conformations in live cells. Commun Chem 9, 109 (2026). https://doi.org/10.1038/s42004-026-01914-x
Mots-clés: dynamique conformationnelle des protéines, imagerie en cellules vivantes, biocapteurs fluorescents, sondes HaloTag, neurotoxine botulique