Clear Sky Science · fr
Diazotation directe des indoles avec le nitrite de 2-méthoxyéthyle
Transformer un gaz problématique en chimie utile
Le monoxyde d’azote est souvent perçu comme un gaz industriel problématique : toxique, difficile à manipuler et généralement considéré comme un déchet. Il est pourtant riche en azote, un élément clé de nombreux médicaments. Cette étude montre comment des chimistes peuvent dompter le monoxyde d’azote en le convertissant en un réactif liquide stable qui, à son tour, aide à construire des molécules complexes proches de candidats-médicaments. Ce travail offre un moyen de transformer un sous-produit dangereux en un outil permettant de fabriquer des composés de valeur de façon plus sûre et plus propre.
Un nouveau molecule auxiliaire pour des réactions délicates
Les chimistes s’appuient fréquemment sur des composés « diazo » — des molécules portant une paire d’atomes d’azote très réactive — pour construire des architectures carbonées complexes. Ces architectures apparaissent dans de nombreux produits pharmaceutiques, en particulier ceux dérivés des indoles, un système cyclique courant dans les produits naturels et les médicaments. Les méthodes traditionnelles pour produire des composés diazo utilisent souvent des azides explosifs ou de grandes quantités d’acides et de bases puissants, posant des problèmes de sécurité et d’environnement. Les auteurs se concentrent sur une alternative plus sûre : un liquide appelé nitrite de 2-méthoxyéthyle, ou MOE-ONO, qui peut être fabriqué directement à partir de monoxyde d’azote gazeux, d’oxygène et d’un alcool simple, ne générant que de l’eau en sous-produit.
Répliquer directement une structure de type médicament importante
L’équipe a cherché à introduire des groupes diazo directement sur les indoles, en les modifiant à une position précise du noyau sans conditions agressives. Ils ont découvert que la combinaison de MOE-ONO avec un radical organique courant, le TEMPO, et une faible quantité d’un sel métallique à base de scandium déclenche efficacement cette transformation. Comparée aux mélanges classiques de nitrite de sodium et d’acide, ou à d’autres donneurs liquides d’oxyde nitrique comme le nitrite de tert-butyle, la nouvelle combinaison donne des rendements supérieurs, beaucoup moins de sous-produits indésirables et fonctionne en des temps bien plus courts. Même des indoles qui résistaient aux méthodes plus anciennes — telles que celles portant de volumineux groupes phényl — ont pu être converties proprement avec cette approche.
Une méthode, de nombreux blocs de construction
Après optimisation de la réaction, les chercheurs ont testé l’étendue d’application de la méthode. Ils ont constaté qu’une grande variété de dérivés d’indole tolèrent ces conditions, y compris ceux portant des esters, des cétones, des amides et différents substituants autour du cycle, des groupes alkyles et méthoxy riches en électrons aux halogènes et groupes cyano. La méthode s’est également étendue au-delà des indoles à des composés apparentés comme les naphtols, formant des dérivés diazo qui nécessitaient auparavant des procédures plus longues et en plusieurs étapes. Fait notable, la réaction fonctionnait encore lorsqu’elle était menée en eau, bien que les matériaux de départ ne s’y dissolvent pas bien. Ce comportement dit « on‑water » suggère que simplement agiter le mélange dans l’eau fournit un milieu plus écologique qui aide la réaction à progresser tout en réduisant la dépendance aux solvants organiques.
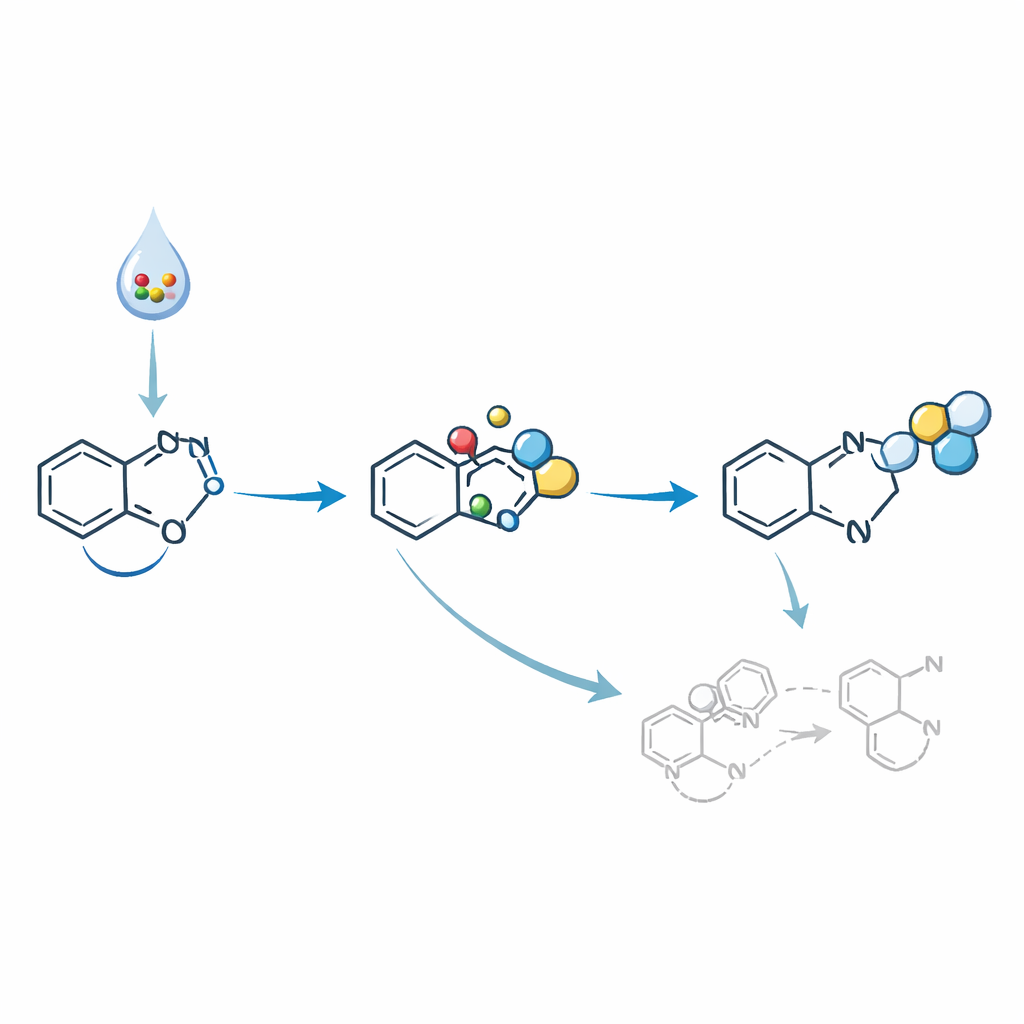
Des intermédiaires réactifs aux candidats-médicaments
Pour montrer la valeur de ces diazoindoles, les auteurs les ont transformés en molécules plus élaborées. À l’aide d’un catalyseur au rhodium, ils ont converti le groupe diazo en un intermédiaire très réactif appelé carbène, qui a ensuite formé de nouvelles liaisons pour construire des cycles cyclopropanes à des positions spécifiques de l’indole. Dans une autre séquence, ils ont assemblé un candidat modulateur pour un récepteur impliqué dans le contrôle de la glycémie, démontrant la pertinence de la méthode pour la chimie médicinale. Ils ont également montré que des réactifs de Grignard — outils classiques pour l’addition de carbone — pouvaient s’additionner de façon sélective à une position de la diazoindole tout en laissant le groupe diazo intact, ouvrant la voie à la construction étape par étape d’indoles et d’indolines fortement substituées.
Pourquoi la réaction reste sur la bonne voie
Dans les coulisses, plusieurs voies concurrentes pourraient conduire à des produits indésirables comme des nitro ou des oximes au lieu des diazo voulus. Des expériences mécanistiques suggèrent que le TEMPO aide à orienter la chimie en piégeant des radicaux nuisibles et en capturant un intermédiaire nitroso fugitif avant qu’il ne puisse se réarranger. D’autres molécules d’oxyde nitrique s’ajoutent ensuite en séquence, produisant finalement le groupe diazo et libérant des nitrates inoffensifs. Le sel de scandium semble favoriser la décomposition de MOE-ONO en espèces réactives et activer le noyau indole, améliorant encore l’efficacité. La détection de nitrate dans le mélange final soutient cette voie proposée du donneur d’oxyde nitrique au produit diazo.
Une voie sûre et durable vers des molécules complexes
Dans l’ensemble, ce travail introduit une manière pratique d’installer des groupes diazo très utiles sur les noyaux d’indole sans recourir à des réactifs explosifs ni à des conditions agressives. En utilisant un liquide stable dérivé du monoxyde d’azote gazeux, la méthode « upcycle » à la fois une émission industrielle problématique et facilite l’accès à des molécules complexes d’allure médicamenteuse. Pour les non‑spécialistes, le message clé est que la chimie ingénieuse peut transformer un gaz toxique en un bloc de construction polyvalent pour de futurs médicaments, tout en réduisant l’impact environnemental en cours de route.
Citation: Hashidoko, A., Kitanosono, T., Nakao, Y. et al. Direct diazotization of indoles with 2-Methoxyethyl nitrite. Commun Chem 9, 104 (2026). https://doi.org/10.1038/s42004-026-01910-1
Mots-clés: revalorisation de l’oxyde nitrique, diazoindoles, synthèse organique verte, médicaments à base d’indole</keyword:molecules à base d’indole> <keyword>réactifs donneurs de NO