Clear Sky Science · fr
Consommation d’échantillons minimisée pour la cristallographie sérielle résolue dans le temps appliquée au cycle redox de la NQO1 humaine
Observer les enzymes en action avec moins d’échantillons précieux
La biologie moderne s’appuie souvent sur des lasers X puissants pour voir comment les molécules de la vie se déplacent et changent de conformation, mais ces expériences consomment généralement d’énormes quantités de protéines préparées avec soin. Cette étude présente une nouvelle façon d’acheminer de minuscules cristaux de protéines vers un laser à électrons libres X de manière bien plus efficace, réduisant la quantité de matière nécessaire jusqu’à 97 %. Elle montre également que cette méthode plus économe peut capturer les premières étapes de l’activité d’une enzyme humaine d’intérêt médical, ouvrant la voie à des « films » de protéines au travail plus accessibles. 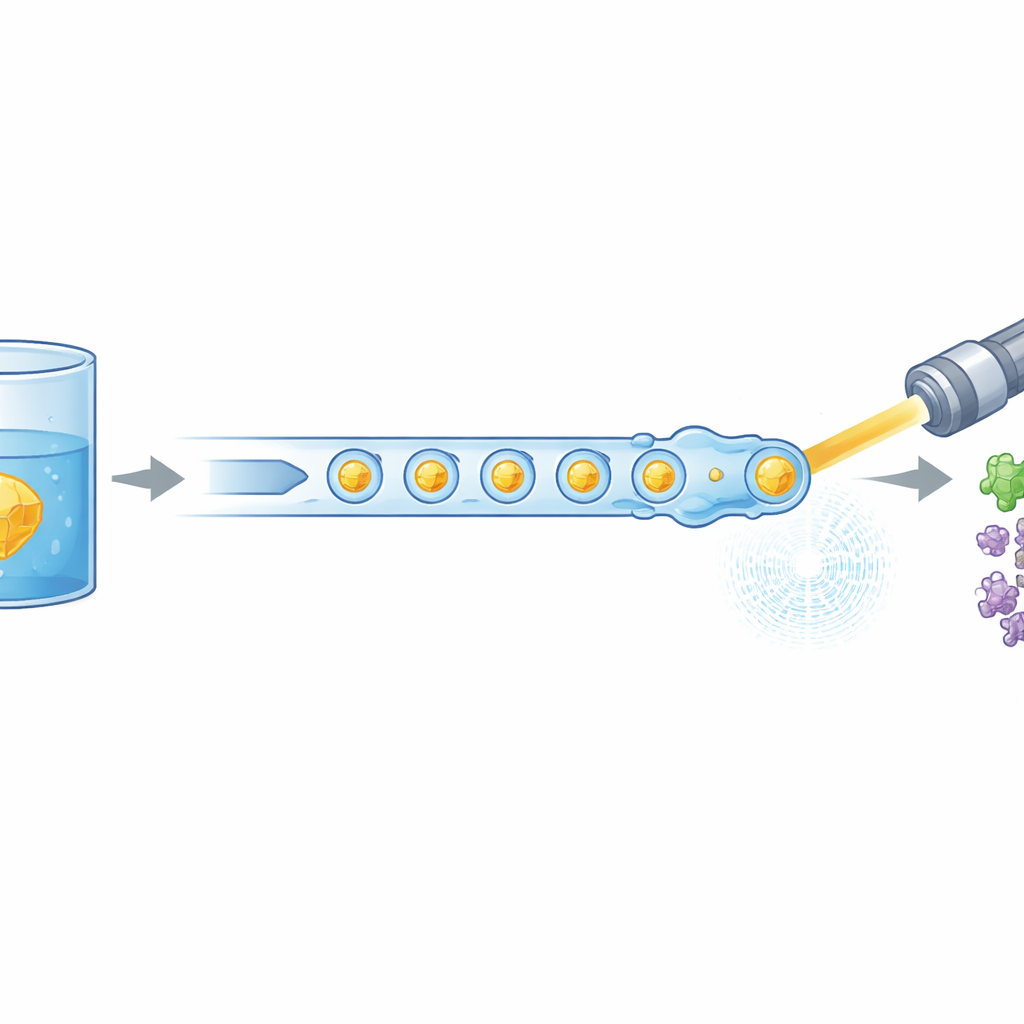
Pourquoi réaliser des films moléculaires coûte si cher
Pour comprendre comment les protéines accomplissent réellement leurs fonctions, les scientifiques se tournent de plus en plus des instantanés statiques vers des « films » temporels qui suivent les réactions en temps réel. Une approche majeure, la cristallographie sérielle résolue dans le temps, pulvérise des millions de microcristaux d’une protéine à travers un faisceau X ultra-brillant. Chaque cristal est frappé une seule fois, fournissant un aperçu sans dommages de la structure, et des milliers de ces images sont combinées pour reconstituer l’ensemble. Le problème est que chaque instant le long d’une réaction — dixième de seconde, seconde entière, etc. — nécessite un lot neuf de cristaux. Comme la préparation des protéines peut être lente et coûteuse, la consommation d’échantillons est devenue un goulot d’étranglement majeur, en particulier dans des installations de pointe comme l’European XFEL, où les impulsions X arrivent en trains rapides à des fréquences mégahertz.
Une nouvelle manière de délivrer de minuscules gouttes sur commande
Les chercheurs ont résolu ce problème en repensant la façon dont les cristaux sont délivrés au faisceau X. Plutôt qu’un flux liquide continu, ils génèrent un train soigneusement espacé de gouttelettes microscopiques, chacune contenant des cristaux de protéine, séparées par une phase huileuse. Un dispositif miniature imprimé en 3D combine deux flux — cristaux protéiques et un partenaire de réaction dissous — en de minuscules volumes mélangés, qui sont ensuite détachés en gouttelettes. Ces gouttelettes sont guidées à travers une buse focalisée par un gaz qui forme un jet étroit compatible avec le vide et la vitesse de l’XFEL. De manière cruciale, la production des gouttelettes est synchronisée électriquement avec le timing des trains d’impulsions X afin que presque chaque impulsion utile frappe une gouttelette plutôt qu’un vide liquide. 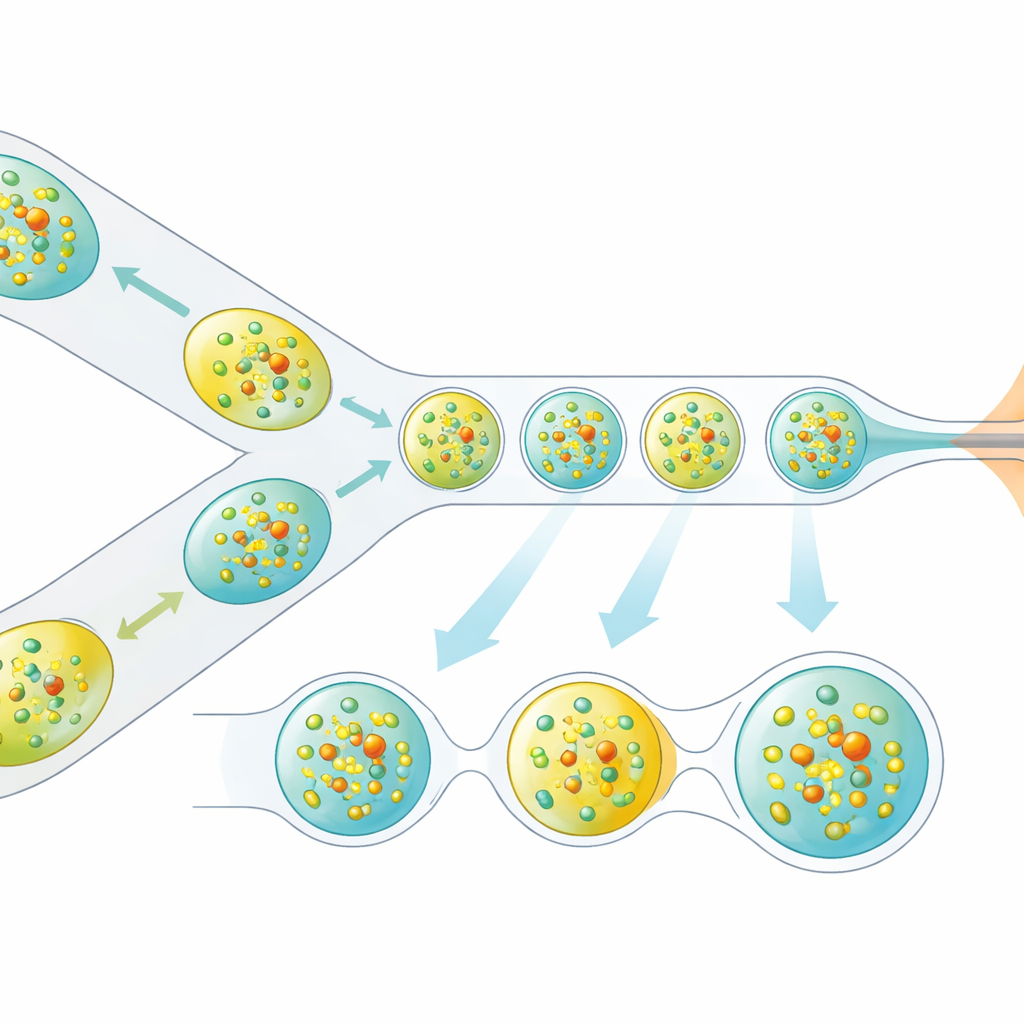
Mettre la méthode à l’épreuve avec une enzyme humaine
Pour démontrer que cette approche à base de gouttelettes fonctionne pour des questions biologiques réelles, l’équipe a étudié la NAD(P)H:quinone oxydoréductase 1 (NQO1), une enzyme humaine impliquée dans la gestion de l’équilibre redox cellulaire et liée à des pathologies. Ils ont mélangé des microcristaux de NQO1 avec son cofacteur naturel, le NADH, et sondé le système à deux temps précoces : 0,3 seconde et 1,2 seconde après le mélange. En examinant les motifs de diffraction X obtenus, ils ont reconstruit des structures tridimensionnelles de l’enzyme à chaque délai. Malgré l’utilisation d’une quantité de protéine bien moindre que dans les expériences à flux continu classiques, la qualité des données a suffi à révéler des caractéristiques subtiles de densité électronique dans les sites actifs de l’enzyme, compatibles avec des molécules de NADH commençant à se lier à faible occupation.
Ce que révèlent les premiers instantanés structuraux
Les structures montrent que peu après le mélange, tous les sites actifs dans le cristal ne se comportent pas de la même manière. À 0,3 seconde, des signes de NADH apparaissent clairement dans trois des quatre sites actifs de la maille élémentaire, et souvent sous plus d’une conformation, ce qui suggère que le cofacteur explore plusieurs positions avant de se stabiliser. À 1,2 seconde, certaines de ces caractéristiques se précisent en un mode de liaison dominant, mais l’ensemble reste celui d’une interaction flexible et seulement partiellement occupée. Ce comportement inégal et changeant concorde avec des preuves biochimiques antérieures indiquant que les deux sous-unités partenaires d’un dimère de NQO1 n’agissent pas de façon parfaitement synchronisée, mais présentent une activité en « moitié des sites », où un côté s’engage en premier tandis que l’autre reste en retard. Les données résolues dans le temps offrent ainsi un premier aperçu structural de la manière dont cette asymétrie se manifeste dans l’espace réel.
Économiser l’échantillon sans sacrifier la science
Sur le plan pratique, la méthode segmentée par gouttelettes a réduit l’usage de protéine d’environ six fois pour les mesures à 0,3 seconde et jusqu’à 97 % pour les expériences à 1,2 seconde, comparée aux jets continus traditionnels dans des conditions similaires. Pourtant elle a fourni des informations structurales fiables à température ambiante, compatibles avec la structure d’impulsions exigeante de l’European XFEL. Pour le non-spécialiste, la conclusion est que les chercheurs peuvent désormais observer des enzymes comme la NQO1 débuter leur activité en quasi-temps réel, tout en utilisant seulement des milligrammes d’échantillon précieux par point temporel. Cela rend beaucoup plus réaliste l’exploration de nombreux temps de réaction et de nombreuses protéines différentes, aidant en fin de compte à révéler comment des enzymes d’intérêt médical se déplacent, se fléchissent et coopèrent pour accomplir la chimie de la vie.
Citation: Doppler, D., Grieco, A., Koh, D. et al. Minimized sample consumption for time-resolved serial crystallography applied to the redox cycle of human NQO1. Commun Chem 9, 107 (2026). https://doi.org/10.1038/s42004-026-01908-9
Mots-clés: cristallographie sérielle, laser à électrons libres X, microfluidique de gouttelettes, dynamique enzymatique, NQO1