Clear Sky Science · fr
Les variants oncogéniques de PI3Kα révèlent un spectre conformationnel graduel avec des poches cryptiques spécifiques aux mutations
Quand un seul changement d’ADN ne suffit pas
Le cancer est souvent décrit comme une maladie des mutations, mais cette étude montre que toutes les mutations n’agissent pas isolément. Les chercheurs ont examiné une enzyme clé du contrôle de la croissance, PI3Kα, et ont découvert que lorsque deux modifications d’ADN spécifiques surviennent ensemble dans la même copie du gène, elles peuvent pousser cette protéine vers des conformations plus actives que chacune des modifications prise séparément. Cela importe parce qu’une PI3Kα hyperactive non seulement favorise les cancers, mais intervient aussi dans des syndromes de surcroissance bénins et des troubles du développement cérébral — et cela aide à expliquer pourquoi certaines tumeurs répondent mal aux traitements actuels.
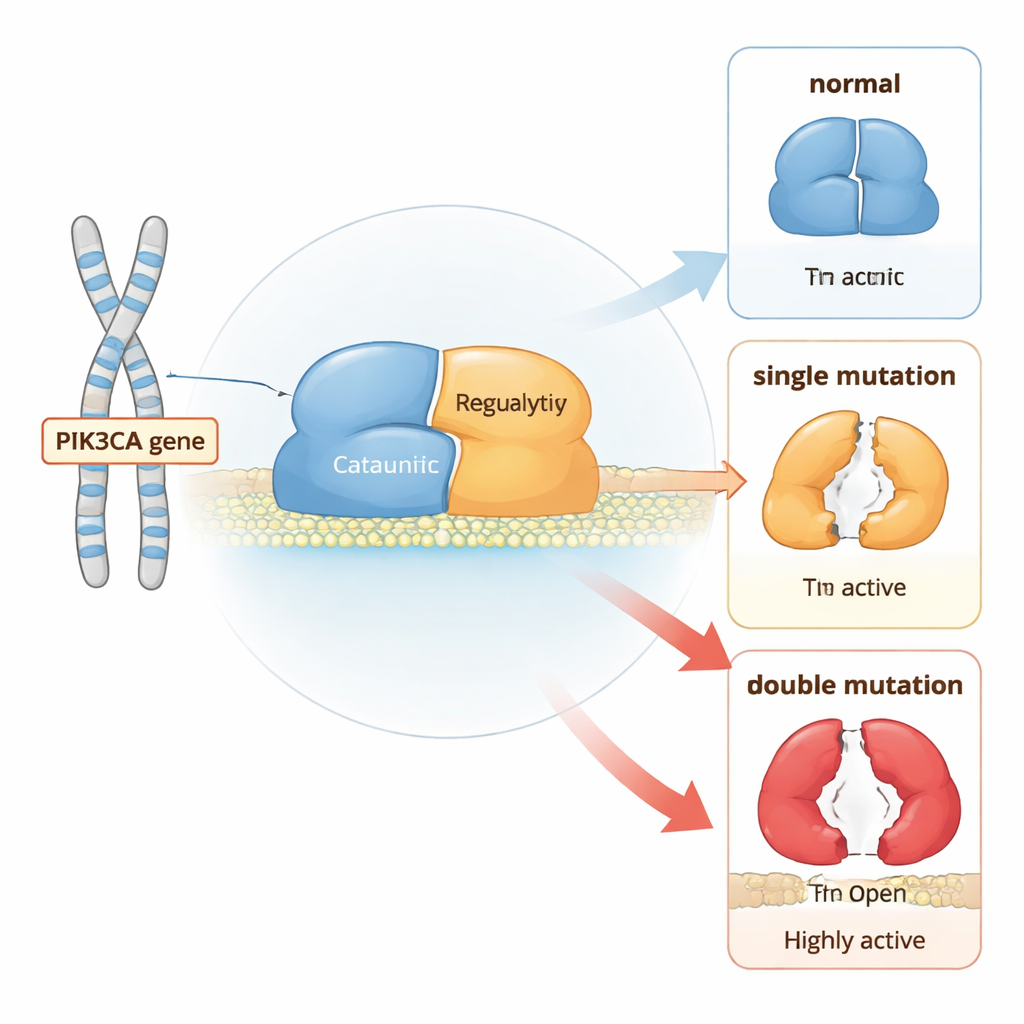
Un interrupteur moléculaire pour la croissance cellulaire
PI3Kα est une protéine en deux parties qui se situe près de la membrane cellulaire et relaie les signaux de croissance. Dans des conditions normales, elle reste majoritairement en position « arrêt » jusqu’à ce que des récepteurs à la surface cellulaire soient stimulés. Ensuite, PI3Kα se déplace vers la membrane et convertit un lipide appelé PIP2 en PIP3, qui indique à la cellule de croître et de se diviser. Pour éviter une croissance incontrôlée, plusieurs éléments de la protéine jouent le rôle de freins intégrés : une région pince le cœur catalytique, une autre maintient une boucle d’activation flexible à proximité, et une sous-unité partenaire aide à contenir l’ensemble du complexe.
Comment les mutations simples et doubles font pencher la balance
En utilisant de longues simulations informatiques à l’échelle atomique, les auteurs ont comparé la PI3Kα normale à des versions portant soit des mutations « points chauds » uniques associées au cancer, soit des combinaisons d’un point chaud avec une mutation plus faible dans la même molécule. Ils ont constaté que chaque mutation modifie la fréquence à laquelle la protéine adopte des conformations plus ouvertes et actives, mais que les mutants doubles déplacent l’équilibre bien plus loin que les simples. En particulier, certaines paires de mutations coopèrent pour desserrer les contacts qui maintiennent une pièce régulatrice (appelée nSH2) en place et pour écarter un autre segment (iSH2) de son site d’accrochage. Ce mouvement coordonné déverrouille le cœur catalytique, facilitant le déplacement de la protéine vers la membrane et le déclenchement du signal.
Aider le substrat à atteindre le site réactionnel
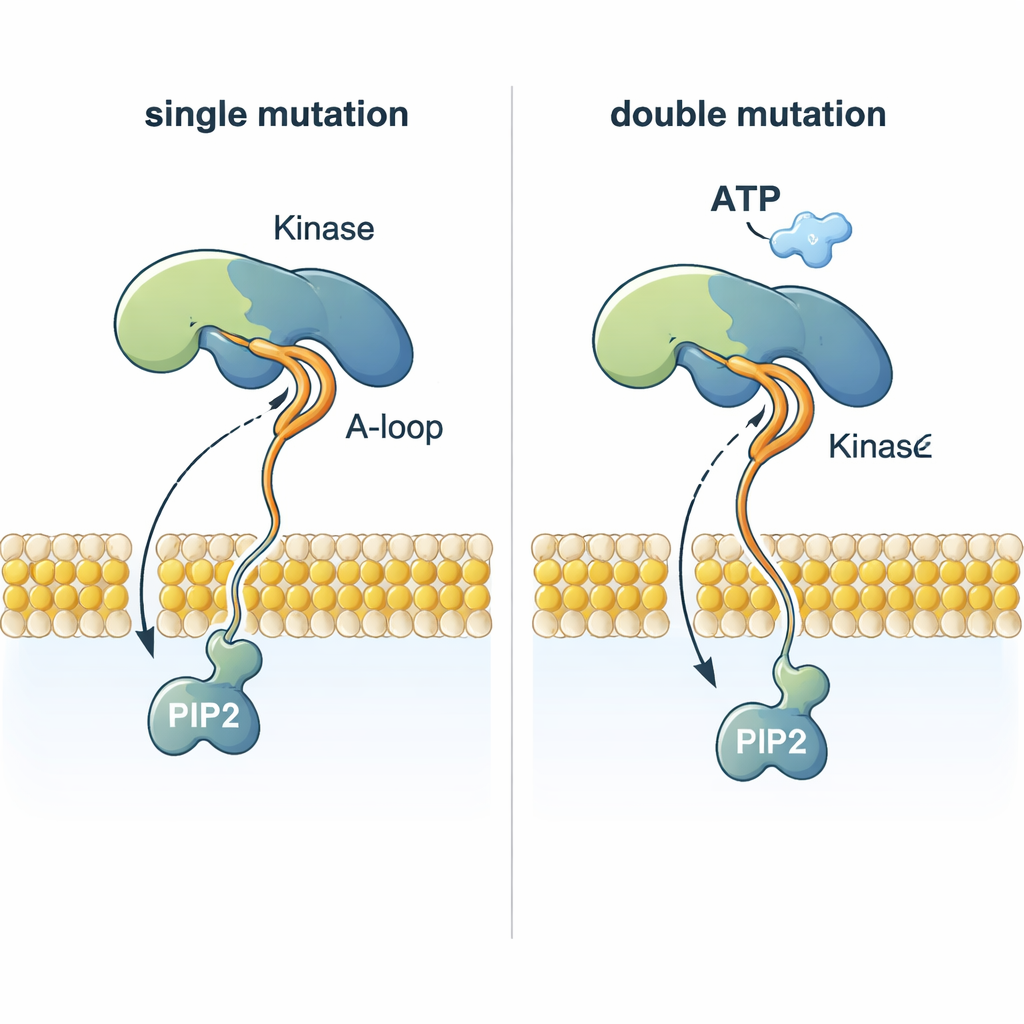
Un puzzle frappant est la manière dont PI3Kα peut transférer un groupe phosphate depuis l’ATP — qui se trouve à près de 2 nanomètres au-dessus de la membrane — vers le PIP2, ancré dans la membrane. Les simulations montrent que certaines mutations remodelent une boucle d’activation flexible de sorte qu’une région fortement chargée positivement se projette vers la membrane. Cette boucle peut saisir la tête négativement chargée du PIP2, l’extraire de la couche lipidique et la guider vers l’ATP. Les mutants doubles qui combinent une mutation favorisant l’ancrage à la membrane avec une autre qui modifie cette boucle coordonnent le PIP2 bien plus efficacement que la PI3Kα normale ou les mutants simples, offrant une explication structurale à l’agressivité accrue de tumeurs portant deux mutations de PI3Kα.
Sites cachés de liaison aux médicaments révélés par le mouvement
Parce que PI3Kα est grande et flexible, un médicament unique visant son site actif a souvent du mal à être efficace contre toutes les formes mutantes et peut provoquer des effets secondaires tels que des perturbations sévères de la glycémie. En suivant la respiration et la flexibilité de la protéine au fil du temps, les chercheurs ont découvert des poches « cryptiques » — des cavités temporaires qui ne s’ouvrent que dans certaines conformations mutantes et sont invisibles dans les structures cristallines statiques. Ces poches apparaissent à des endroits spécifiques selon la mutation, par exemple près des régions qui bougent le plus dans certains mutants doubles. Cela suggère que des médicaments allostériques soigneusement conçus, qui se lient loin du site actif, pourraient être adaptés pour verrouiller des variants mutants particuliers dans des conformations plus sûres et moins actives.
Vers des traitements combinés plus intelligents
Globalement, le travail soutient une vision « coup de poing en deux temps » de la génétique du cancer : une mutation forte en point chaud plus une partenaire plus faible dans la même molécule de PI3Kα peuvent créer un spectre graduel de conformations plus actives, souvent corrélées à des issues cliniques plus sévères. Pour la thérapie, les auteurs avancent que plutôt que de s’en remettre à un inhibiteur unique, il pourrait être plus efficace de combiner des médicaments ciblant différentes poches — l’une au niveau du site actif et une ou plusieurs allostériques qui n’existent que dans des mutants spécifiques. De tels cocktails pourraient, en principe, réduire plus précisément l’activité de PI3Kα, diminuer les effets toxiques et mieux adapter le traitement au profil exact de mutations retrouvé dans la tumeur d’un patient.
Citation: Jang, H., Yavuz, B.R., Zhang, M. et al. Oncogenic PI3Kα variants reveal graded conformational spectrum with mutation-specific cryptic pockets. Commun Chem 9, 100 (2026). https://doi.org/10.1038/s42004-026-01906-x
Mots-clés: PI3K alpha, mutations oncogéniques, inhibiteurs allostériques, dynamique moléculaire, transduction du signal