Clear Sky Science · fr
Dynamique dépendante de la séquence et de l’échelle de longueur dans les biocondensats de protéines désordonnées fortement chargées
Pourquoi de petites gouttes de protéines comptent
À l’intérieur de nos cellules, de nombreuses réactions vitales se déroulent au sein de structures molles en forme de goutte sans membrane entourante. Ces « condensats biomoléculaires » se comportent comme de petits compartiments liquides et sont souvent constitués de protéines souples et fortement chargées. Des expériences ont montré que des molécules à l’intérieur de certaines de ces gouttes peuvent se déplacer étonnamment vite, même si les gouttes, prises globalement, peuvent être assez épaisses et collantes. Cet article pose une question simple mais importante : comment l’ordre précis des charges positives et négatives le long de ces protéines contrôle-t-il la vitesse des déplacements à l’intérieur de telles gouttes ?
Construire des gouttes à partir de chaînes souples et chargées
Les auteurs se concentrent sur les protéines intrinsèquement désordonnées : de longues chaînes flexibles qui ne se replient pas en formes rigides. Bon nombre de ces chaînes portent à la fois des charges positives et négatives, disposées selon des motifs différents le long de la séquence. Grâce à des simulations informatiques à grande échelle, l’équipe a créé des gouttes modèles formées par de nombreuses copies de ces protéines, ainsi que par de l’eau et de petits ions, pour reproduire l’intérieur encombré des condensats réels. Ils ont modifié systématiquement la « blocabilité » du motif de charge, depuis des séquences où charges positives et négatives alternent jusqu’à des séquences où toutes les charges positives sont regroupées et toutes les charges négatives forment un bloc séparé.
La teneur en eau et l’écoulement fluidique façonnent le mouvement
Les simulations ont révélé que ces gouttes peuvent toujours se comporter comme de véritables liquides avec une teneur en eau très élevée : entre environ 55 % et 84 %, selon le motif de charge. Cette quantité d’eau signifie que l’écoulement du fluide, ou l’hydrodynamique, n’est pas entièrement supprimé comme le suggèreraient de nombreuses théories pour des solutions de polymères denses. En suivant comment les segments protéiques errent avec le temps, les auteurs ont observé des profils de mouvement caractéristiques de chaînes dont le déplacement est facilité par le fluide environnant, plutôt que ralenti seulement par la friction. Cette influence hydrodynamique persiste jusqu’à la taille d’une chaîne protéique entière, et au-delà, en particulier dans les gouttes formées par des séquences aux charges plus mélangées et donc plus riches en eau.
Les motifs locaux de charge contrôlent la flexibilité à micro-échelle
En regardant de plus près, les auteurs ont examiné comment de courtes sections de chaque chaîne se relâchent et se réarrangent à l’intérieur de la goutte. Différentes portions d’une même protéine, contenant le même nombre d’unités, pouvaient se mouvoir à des vitesses très différentes selon leur mélange local de charges positives et négatives. Les sections plus équilibrées en charge se détendaient plus rapidement, tandis que les segments dominés par un seul type de charge bougeaient lentement. De manière surprenante, ces différences restaient marquées alors que de simples arguments de crantage électrostatique prédiraient que les effets électrostatiques devraient être de courte portée dans de telles conditions salines et encombrées. Le travail montre que le fait que les charges soient liées le long d’une chaîne préserve des corrélations électriques de longue portée qui affectent fortement le mouvement local.
La viscosité dépend de la taille de l’échelle sondée
L’équipe s’est ensuite demandé à quel point ces gouttes semblent « épaisses » à différentes échelles de longueur. En utilisant une méthode qui relie de fines perturbations du moment cinétique du fluide à sa résistance à l’écoulement, ils ont calculé une viscosité dépendant de l’échelle de son observation. Pour toutes les séquences, le fluide apparaît plus fluide lorsqu’on le sonde à des échelles très petites et plus visqueux lorsqu’on le sonde à l’échelle de la goutte entière. Cette dépendance à la taille est particulièrement spectaculaire pour les séquences à charges en blocs : pour le motif le plus ségrégué, la viscosité macroscopique est plus de vingt fois supérieure à la viscosité locale au niveau du monomère. En revanche, les gouttes issues de séquences bien mélangées présentent un écart beaucoup plus faible. Globalement, la viscosité en vrac augmente fortement avec la concentration en protéines, conformément au comportement des solutions de polymères neutres denses, même si les protéines elles-mêmes sont fortement chargées.
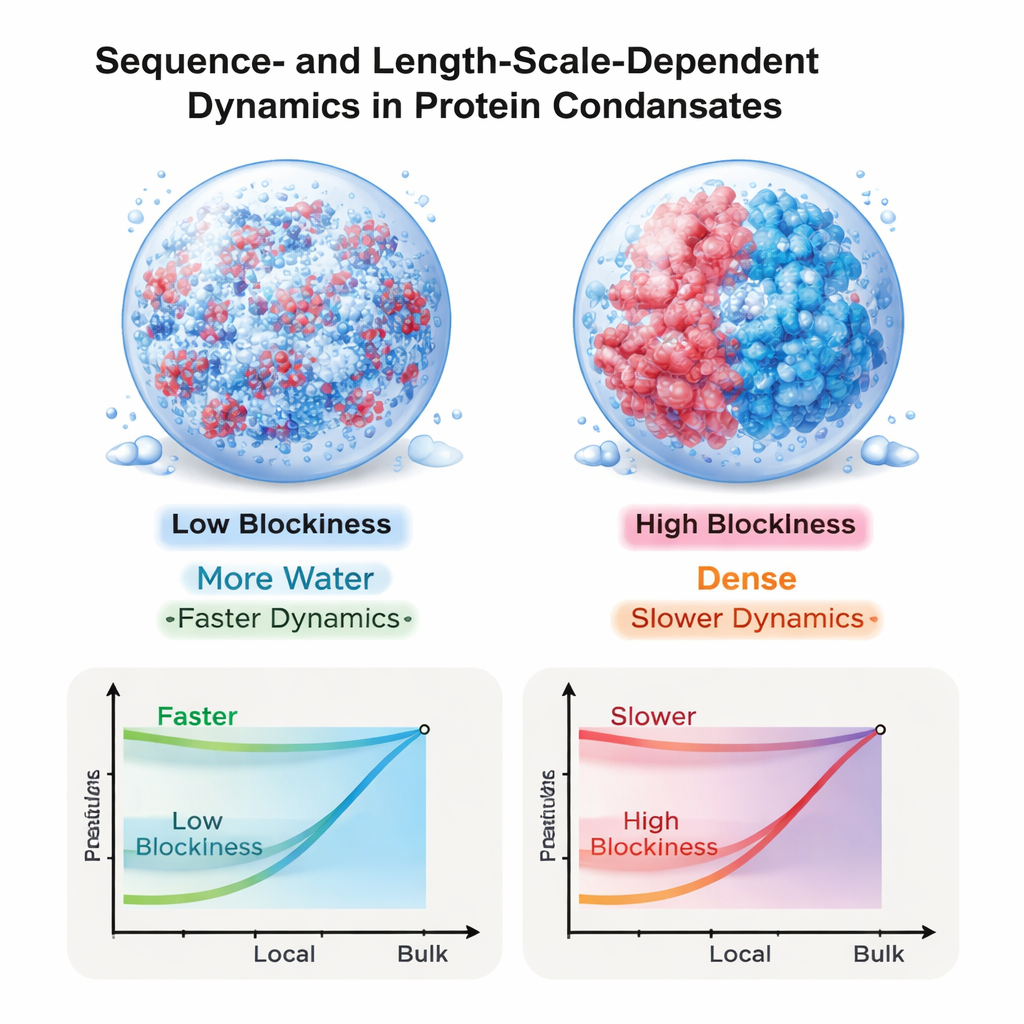
Relier les simulations à des expériences déroutantes
Ces résultats contribuent à résoudre un paradoxe apparent issu d’expériences récentes : comment de petites molécules et des segments protéiques peuvent-ils diffuser si rapidement à l’intérieur de condensats qui, mesurés globalement, paraissent extrêmement visqueux ? La réponse qui émerge de ce travail est que l’écoulement de l’eau et les interactions électrostatiques de longue portée demeurent importants dans ces gouttes, et leur impact est étroitement contrôlé par l’ordre des charges le long de chaque chaîne. Les séquences à motifs de charge en blocs produisent des gouttes denses et très visqueuses qui restent toutefois relativement fluides à l’échelle microscopique, tandis que les séquences plus mélangées donnent des environnements globalement plus mobiles. En montrant que la séquence de charges peut régler le mouvement différemment selon l’échelle, l’étude propose un principe de conception pour l’ingénierie de matériaux synthétiques à base de protéines et éclaire la manière dont les cellules peuvent programmer le comportement des condensats par la séquence détaillée de leurs protéines désordonnées.
Citation: Zhou, H., Wu, Z., Jiang, L. et al. Sequence and length-scale dependent dynamics in biocondensates of highly charged disordered proteins. Commun Chem 9, 98 (2026). https://doi.org/10.1038/s42004-026-01903-0
Mots-clés: condensats biomoléculaires, protéines intrinsèquement désordonnées, motifs de charge, dynamique des protéines, viscosité