Clear Sky Science · fr
Un flux de travail intégré pour l’élucidation de la structure des poudres nanocristallines
Pourquoi les cristaux minuscules comptent
De nombreux médicaments modernes et matériaux avancés sont fabriqués sous forme de poudres fines, et non sous forme de beaux cristaux brillants. C’est un défi pour les scientifiques, car notre meilleur outil pour voir l’arrangement atomique dans un solide — la cristallographie par rayons X — exige des cristaux grands et parfaits. Cet article présente une nouvelle stratégie pas à pas pour déterminer la structure atomique complète de poudres nano‑taille récalcitrantes, du type souvent issues de procédés de fabrication plus écologiques et économes en solvant. Comprendre ces structures peut aider à améliorer la dissolution des médicaments, leur stabilité et leur fiabilité d’action dans l’organisme.
Le défi des atomes invisibles
Les méthodes mécanochemiques, comme le broyage des réactifs dans un moulin au lieu de les dissoudre dans de grands volumes de solvant, gagnent en popularité conformément aux principes de la chimie verte. Elles peuvent générer de nouvelles formes solides de médicaments — par exemple des sels et des cocrystaux — qui ajustent des propriétés telles que la solubilité et la durée de conservation. Mais les mêmes procédés qui rendent ces méthodes attrayantes compliquent la tâche des cristallographes : ils produisent généralement seulement des cristaux nano‑ ou microscopiques, parfois mélangés à du matériau amorphe. La diffraction sur monocristal de rayons X ne peut pas traiter de tels grains minuscules, tandis que la diffraction sur poudre de rayons X est souvent mise à l’épreuve par la complexité des solides pharmaceutiques modernes.
Une boîte à outils pour voir l’invisible
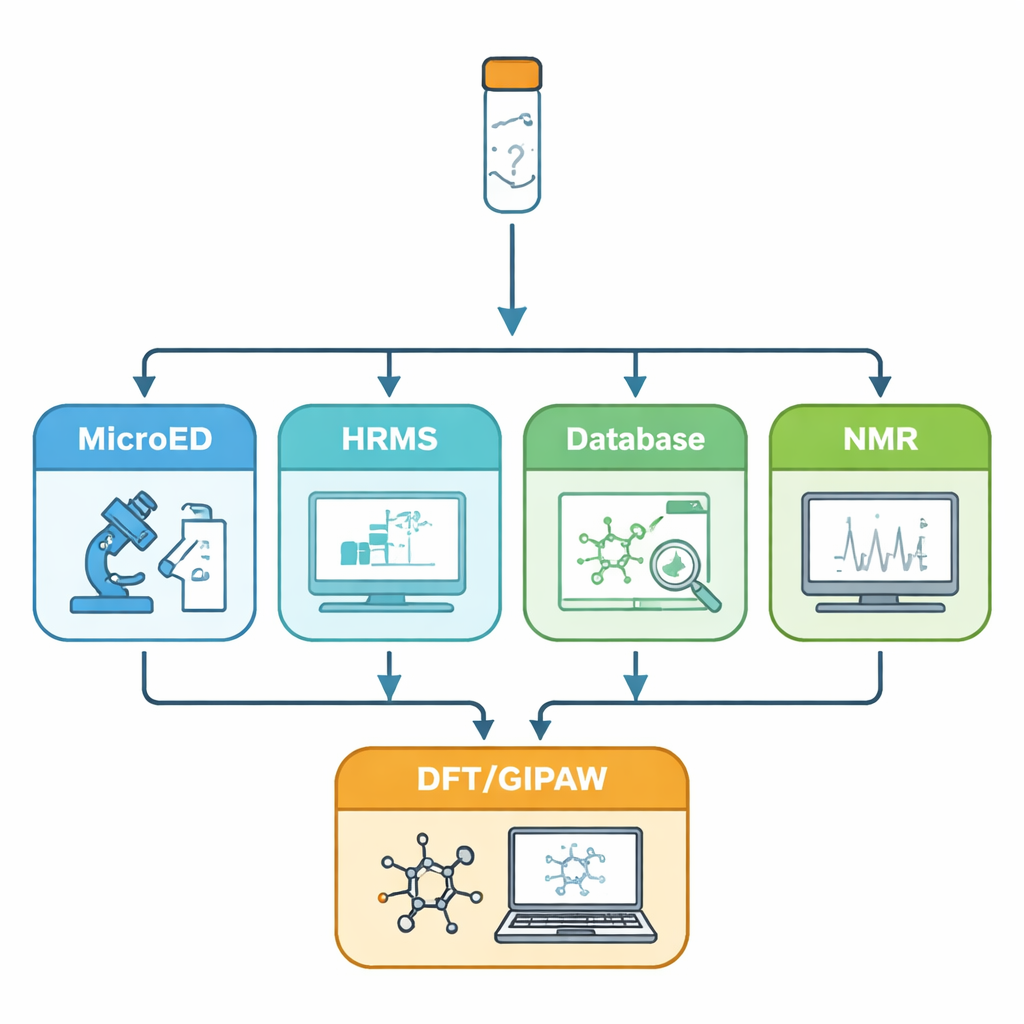
Ces dernières années, la diffraction électronique sur microcristaux (MicroED) est apparue comme une méthode puissante pour obtenir des informations à l’échelle atomique à partir de cristaux de quelques centaines de nanomètres seulement. Les électrons interagissent plus fortement avec la matière que les rayons X, de sorte que même ces cristaux minuscules peuvent fournir des motifs de diffraction nets. MicroED peut révéler l’agencement de base — ou le « squelette » — des molécules dans le solide. Toutefois, la méthode présente deux angles morts importants : les atomes d’hydrogène sont très difficiles à voir, et il peut être ardu de distinguer des atomes comme le carbone, l’azote et l’oxygène. Les auteurs pallient ces faiblesses en combinant MicroED avec une série d’outils complémentaires : la spectrométrie de masse haute résolution pour déterminer la formule moléculaire exacte, des recherches dans des bases de données pour proposer des identités moléculaires plausibles, la RMN en solution et en état solide pour confirmer quelles molécules sont réellement présentes et comment elles interagissent, et des calculs quantiques pour affiner et valider la structure finale.
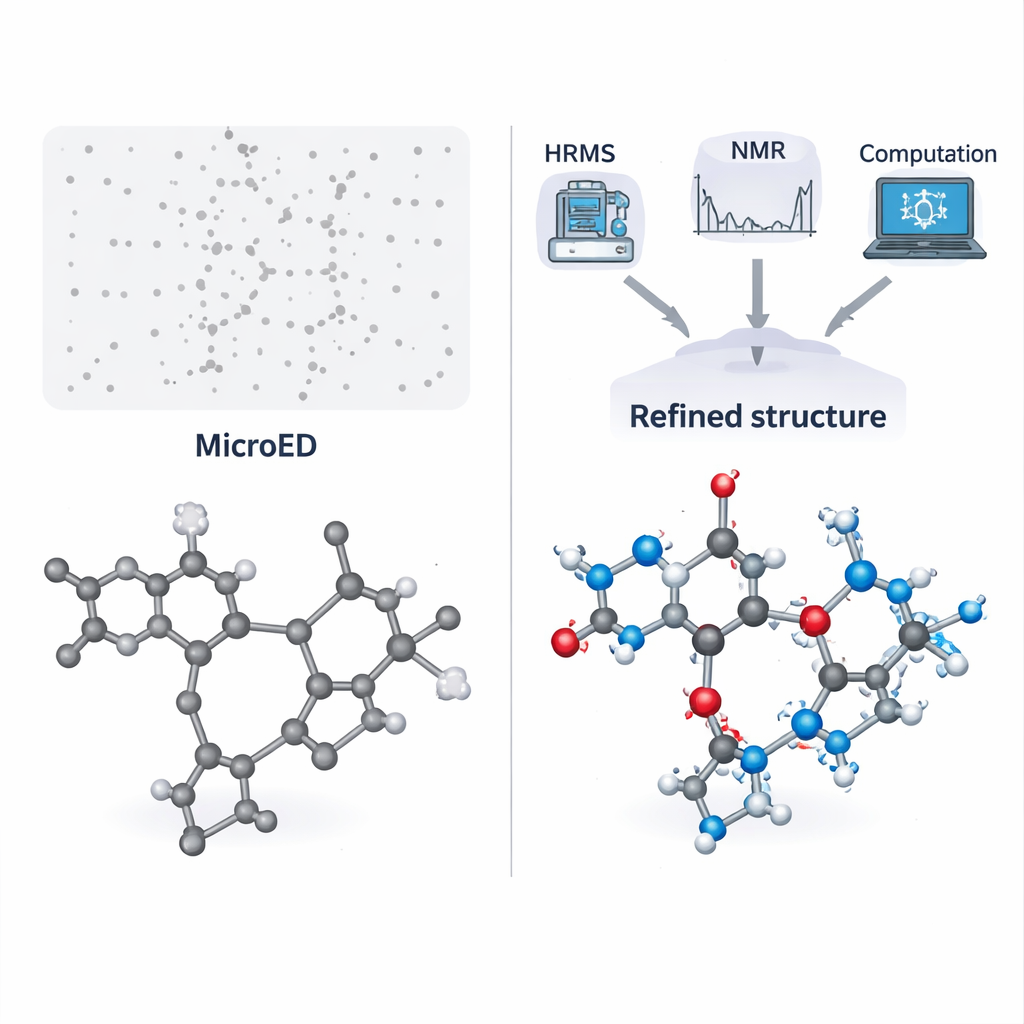
Résoudre deux énigmes réelles
L’équipe applique d’abord ce flux de travail à un sel difficile obtenu à partir de la pyridoxine (une forme de vitamine B6) et de l’antioxydant N‑acétyl‑L‑cystéine. Ce matériau ne peut être obtenu que par broyage à sec, et les tentatives répétées de faire croître des monocristaux adaptés ont échoué car le produit est visqueux. MicroED a montré que la poudre contenait deux composants moléculaires différents et a même suggéré la présence d’un atome de soufre, mais n’a pas permis d’assigner de manière fiable tous les autres atomes ni les atomes d’hydrogène. La spectrométrie de masse haute résolution a révélé deux masses moléculaires précises, utilisées ensuite pour interroger des bases de données chimiques à la recherche de structures correspondantes. En comparant ces candidats avec le squelette fourni par MicroED et en vérifiant des caractéristiques clés par RMN en solution, les auteurs ont restreint les possibilités et identifié avec confiance les deux partenaires comme la pyridoxine et la N‑acétyl‑L‑cystéine.
Du croquis grossier à l’image finale
Une fois les identités moléculaires établies, des calculs quantiques informatiques ont été utilisés pour relâcher en douceur la structure dérivée de MicroED et prédire les déplacements chimiques en RMN. Ces signaux RMN calculés ont ensuite été comparés aux données de RMN en état solide recueillies sur la poudre réelle. L’excellent accord a confirmé que les positions atomiques, y compris la plupart des hydrogènes, étaient correctes. Des expériences RMN supplémentaires se sont concentrées sur un hydrogène crucial partagé entre les deux molécules, permettant à l’équipe de mesurer avec grande précision sa distance à un atome d’azote. Cela a montré que la paire forme un véritable sel, et non un cocristal neutre — une distinction importante pour le comportement du médicament et sa classification réglementaire. Le même flux de travail a été testé sur un second composé, très différent : un petit tripeptide appelé fMLF, largement utilisé comme système modèle en RMN mais dont la structure en état solide n’avait jamais été rapportée. Là encore, l’approche intégrée a permis d’obtenir une structure entièrement validée et a même éclairé des mouvements rapides de son noyau aromatique.
Comment cela aide la science et la médecine
En traitant chaque poudre inconnue comme un « test à l’aveugle », les auteurs montrent que leur flux de travail modulaire peut partir d’informations très limitées et malgré tout aboutir à une structure atomique complète et fiable. MicroED fournit un premier croquis, la spectrométrie de masse et les bases de données identifient des molécules candidates, la RMN clarifie combien de composants sont présents et où se situent les hydrogènes, et les calculs quantiques relient le tout. Pour les chimistes et les scientifiques pharmaceutiques, cela signifie que les poudres nanocristallines complexes issues de voies de fabrication écologiques n’ont pas à rester des mystères structuraux. La méthode ouvre la voie à une caractérisation détaillée et routinière des poudres — des pigments aux formulations médicamenteuses — même lorsque la croissance de cristaux traditionnels échoue, contribuant à concevoir des matériaux plus sûrs et plus efficaces dès leur conception.
Citation: Sabena, C., Bravetti, F., Miyauchi, N. et al. An integrated workflow for the structure elucidation of nanocrystalline powders. Commun Chem 9, 97 (2026). https://doi.org/10.1038/s42004-026-01902-1
Mots-clés: MicroED, RMN en état solide, poudres nanocristallines, synthèse mécanochimique, sels pharmaceutiques