Clear Sky Science · fr
Dynamiques de la photo-oxydation du CO en CO2 sur le rutile (110)
Pourquoi observer des molécules en une trillionième de seconde est important
La vie moderne dépend de réactions chimiques qui purifient notre air et notre eau et convertissent la lumière du soleil en énergie exploitable. Bon nombre de ces réactions ont lieu sur les surfaces de solides appelés photocatalyseurs, activés par la lumière. Cette étude examine l’une de ces réactions — comment le monoxyde de carbone (CO), toxique, est transformé en dioxyde de carbone (CO2) sur une surface de dioxyde de titane — sur des échelles de temps de l’ordre du quadrillionième de seconde. Comprendre ces étapes ultrarapides peut aider les chercheurs à concevoir des matériaux plus efficaces pour le contrôle de la pollution, des surfaces autonettoyantes et des technologies solaires.
Une équipe de nettoyage activée par la lumière
Le dioxyde de titane est un matériau polyvalent que l’on trouve dans les fenêtres autonettoyantes, les revêtements purificateurs d’air et les dispositifs expérimentaux de carburants solaires. Il est peu coûteux, stable et peut utiliser la lumière pour déclencher sur sa surface des réactions de nettoyage puissantes. Mais toutes les formes de dioxyde de titane ne se comportent pas de la même manière. Deux formes courantes, appelées anatase et rutile, diffèrent par leur efficacité à piloter des réactions comme la conversion du CO en CO2. Alors que l’anatase est généralement plus active dans l’ensemble, le timing détaillé des étapes individuelles — en particulier la façon dont l’oxygène de l’air est activé — restait flou. Cette étude se concentre sur la forme rutile avec une orientation de surface spécifique, dite (110), pour déterminer à quelle vitesse le CO est oxydé une fois que la lumière frappe le matériau.
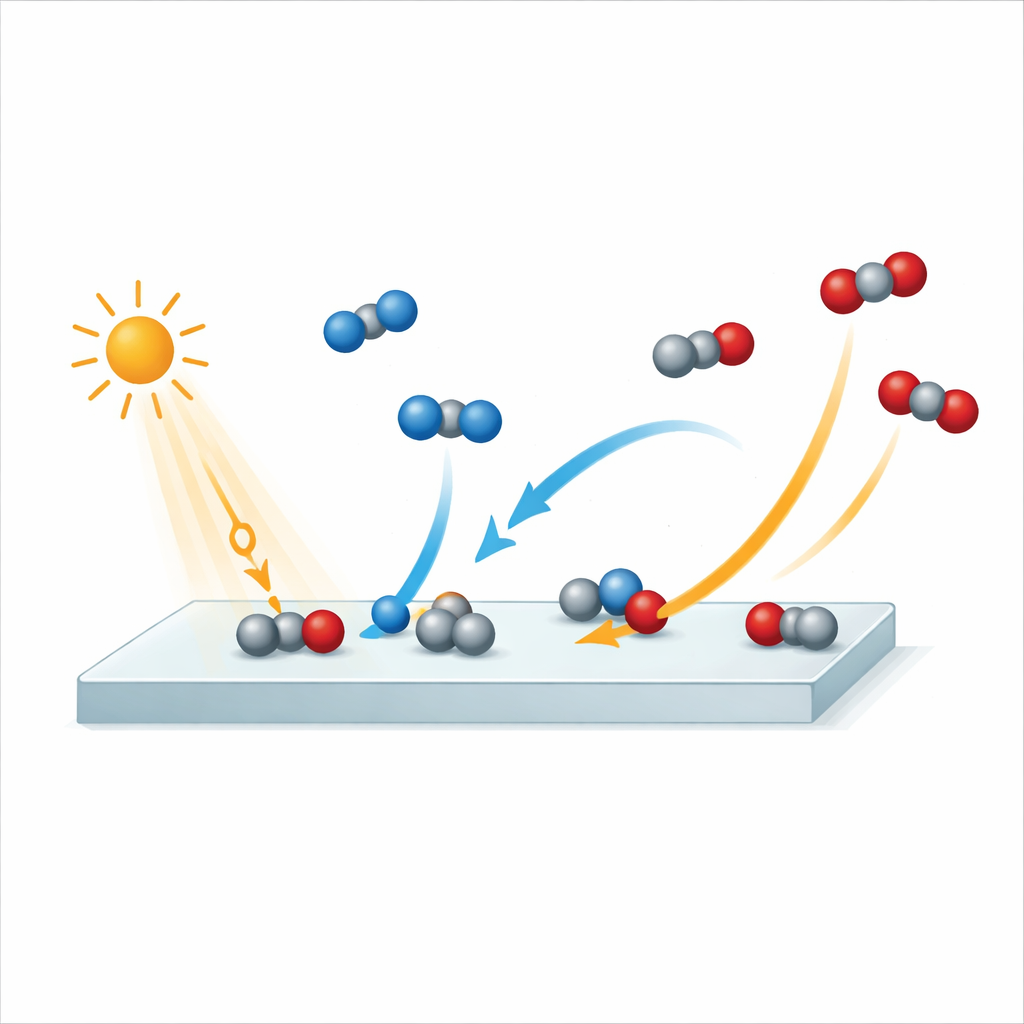
Filmer une réaction à vitesse extrême
Pour capturer ce processus, les chercheurs ont utilisé une installation à laser à électrons libres à Hambourg qui produit des éclairs de rayons X extrêmement courts. Ils ont d’abord frappé la surface de rutile par une impulsion de lumière infrarouge, jouant le rôle d’un minuscule flash photographique qui déclenche la réaction. Une impulsion de rayons X, précisément synchronisée, a ensuite sondé comment les atomes et les électrons à la surface évoluaient. En répétant cette séquence avec des délais différents entre les impulsions lumineuses et X, ils ont reconstitué une sorte de « film moléculaire » de la réaction avec une résolution temporelle d’environ 250 femtosecondes — une femtoseconde étant le millionième du milliardième de seconde. L’équipe a suivi des signaux provenant des atomes d’oxygène à la surface et dans les molécules gazeuses, ce qui leur a permis de distinguer le CO, le CO2, l’eau et l’oxyde lui-même au fur et à mesure du déroulement de la réaction.
Attraper le CO2 en moins d’un trillionième de seconde
L’observation clé est qu’un nouveau CO2 apparaît sur la surface de rutile en aussi peu que 200 à 800 femtosecondes après l’impulsion lumineuse. Cela signifie que l’oxygène provenant de molécules O2 voisines s’active, que des liaisons se rompent et que le CO est converti en CO2 en moins d’un trillionième de seconde. Après environ 0,8 picoseconde, le signal du CO2 fraîchement formé diminue à mesure que le produit se désorbe de la surface. Fait remarquable, toute cette séquence est plus rapide sur le rutile que sur l’anatase, où des travaux antérieurs avaient observé l’apparition du premier CO2 seulement après environ 1,2 à 2,8 picosecondes dans des conditions par ailleurs similaires. Même si l’anatase produit plus de CO2 au total et est considérée comme le photocatalyseur le plus performant, le rutile réalise l’étape cruciale d’oxydation plus rapidement.
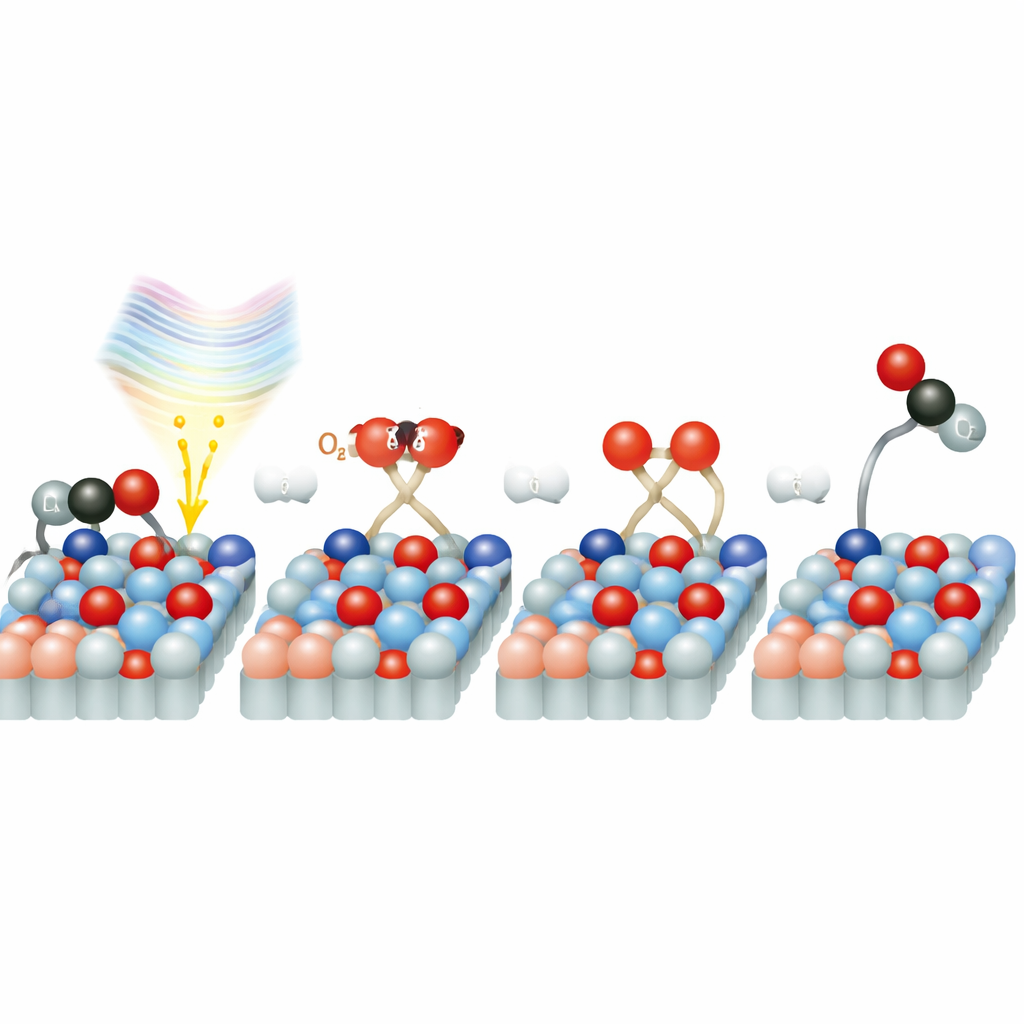
Une voie de contournement pour l’oxygène
Pourquoi la réaction est-elle si rapide sur le rutile ? Des simulations informatiques détaillées suggèrent que les molécules d’oxygène adsorbées sur la surface créent des états électroniques particuliers qui servent de pont entre le solide et l’O2. Lorsque la lumière laser de 770 nanomètres est absorbée, elle peut déplacer directement un électron du dioxyde de titane vers la molécule d’oxygène, formant une espèce d’oxygène chargée et activée. Ce « raccourci » évite la voie plus lente où les électrons voyagent d’abord à travers le volume du solide puis migrent vers la surface. Une fois activé, l’oxygène se divise rapidement et un atome d’oxygène se combine au CO pour former du CO2. L’étude montre aussi que des traces d’eau à la surface peuvent à la fois bloquer des sites réactifs et, à faibles niveaux, aider potentiellement ce transfert de charge et l’activation de l’oxygène, ajoutant une couche supplémentaire de complexité.
Relier la structure électronique à la performance réelle
Globalement, le travail montre que de petits détails dans la façon dont les électrons se déplacent entre une surface et des molécules voisines peuvent modifier drastiquement la vitesse des réactions, même entre deux matériaux étroitement apparentés. Alors que l’anatase l’emporte encore en termes de rendement photocatalytique total, le rutile présente une étape d’activation de l’oxygène plus rapide liée à cette route spéciale de transfert de charge. En associant mesures ultrarapides et simulations avancées, l’étude fournit une feuille de route pour concevoir des surfaces afin que des réactions déclenchées par la lumière se déroulent plus efficacement. À long terme, ces connaissances pourraient aider les ingénieurs à développer de meilleurs revêtements pour la purification de l’air, des surfaces antibactériennes plus efficaces et des matériaux améliorés pour la production de carburants solaires et le fractionnement de l’eau.
Citation: Gleissner, H., Wagstaffe, M., Wenthaus, L. et al. Dynamics of CO photooxidation to CO2 on rutile (110). Commun Chem 9, 127 (2026). https://doi.org/10.1038/s42004-026-01901-2
Mots-clés: photocatalyse, dioxyde de titane, spectroscopie ultrarapide, chimie de surface, oxydation du monoxyde de carbone