Clear Sky Science · fr
Développement d’un nanomodèle à points quantiques de carbone conjugués quadruplement pour une thérapie ciblée du gliome
Nouveau espoir pour des tumeurs cérébrales tenaces
Les tumeurs cérébrales de haut grade, comme le glioblastome, font partie des cancers les plus difficiles à traiter. De nombreux médicaments efficaces ailleurs dans l’organisme ne franchissent pas la barrière hémato-encéphalique ou endommagent les tissus sains en chemin. Cette étude décrit un nanoparticule « intelligente » fabriquée en laboratoire qui vise à pénétrer plus précisément dans les tumeurs cérébrales, transporter un cocktail médicamenteux puissant et le libérer directement dans le noyau des cellules tumorales, où il peut infliger le plus de dégâts au cancer tout en épargnant les cellules normales.
Un petit camion de livraison construit en carbone
Au cœur de la nouvelle approche se trouvent les points quantiques de carbone — des particules à l’échelle nanométrique fabriquées à partir de carbone, peu coûteuses à produire, compatibles avec l’eau et luminescentes sous certains types de lumière. Leurs surfaces riches en sites chimiques permettent d’y fixer plusieurs composants biologiques simultanément. Dans ce travail, les chercheurs ont créé un nanomodèle « conjugué quadruplement » : chaque point quantique de carbone a été lié chimiquement, en une seule réaction en une étape, à deux peptides de ciblage différents et à deux charges anticancéreuses. Cette conception modulaire transforme chaque point en un petit camion de livraison capable de reconnaître les cellules tumorales, de franchir les barrières cellulaires et d’acheminer les médicaments vers la bonne adresse intracellulaire.
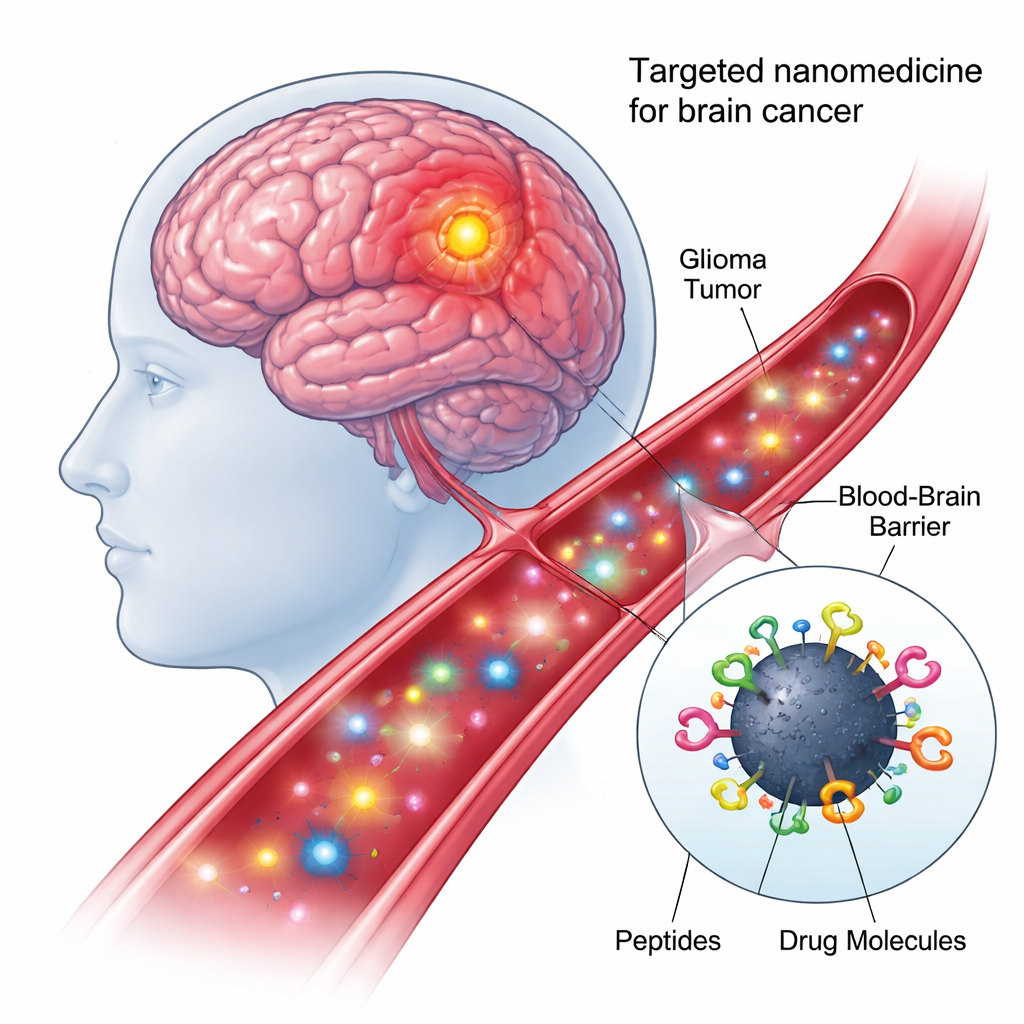
Repérer et pénétrer les bonnes cellules cérébrales
Le premier peptide sur le nanoparticule, appelé shPep-1, est conçu pour reconnaître un récepteur nommé IL13Rα2. Ce récepteur est fortement exprimé dans de nombreuses tumeurs cérébrales agressives — y compris le glioblastome adulte et pédiatrique et le gliome pontique intrinsèque diffus — mais apparaît faiblement sur les cellules cérébrales normales. En se liant à IL13Rα2, shPep-1 aide les points quantiques à se diriger vers les cellules tumorales et à y pénétrer par captation médiée par le récepteur. Le second peptide, plus long, lnPep-1, contient un signal de localisation nucléaire : une courte séquence qui aide la cargaison à traverser la membrane nucléaire et à atteindre le centre de contrôle de la cellule, où l’ADN est stocké. Ensemble, ces deux peptides confèrent au nanoparticule à la fois une préférence tumorale et la capacité d’atteindre le noyau une fois à l’intérieur.
Livrer une attaque médicamenteuse coordonnée
La charge thérapeutique consiste en deux petites molécules. La première est l’épirubicine, un médicament de chimiothérapie bien connu qui tue les cellules cancéreuses en s’insérant dans l’ADN et en bloquant des enzymes nécessaires à la réparation des cassures double brin. La seconde est un métabolite appelé 5-aminoimidazole-4-carboxamide (AIC), produit à partir du médicament contre les tumeurs cérébrales témozolomide à pH physiologique. Dans des travaux antérieurs, la même équipe a montré que la combinaison d’épirubicine et d’AIC sur un point quantique de carbone augmentait la mortalité des cellules cancéreuses par rapport à chaque médicament seul. Dans la nouvelle conception, les deux sont co-administrés sur le nanoparticule à double peptide, visant un effet synergique directement dans le noyau de la cellule tumorale.
Puissant pour les cellules tumorales, plus doux pour les cellules normales
Pour tester l’efficacité du nanomodèle, l’équipe a exposé plusieurs lignées cellulaires de gliome de haut grade — glioblastome adulte, glioblastome pédiatrique et un modèle de gliome pontique intrinsèque diffus — aux points quantiques de carbone conjugués quadruplement. Même à de très faibles concentrations (aussi basses que 50 nanomolaires), la viabilité des cellules tumorales est tombée à environ la moitié de celle des témoins non traités, et à des doses plus élevées, tous les conjugués testés ont tué la plupart des cellules tumorales. Fait important, le nanomodèle quadruple a surpassé les versions plus simples « à peptide unique », bien qu’il transportât globalement moins d’épirubicine. Testé sur des cellules musculaires lisses vasculaires non cancéreuses, il s’est montré beaucoup moins toxique : ces cellules nécessitaient environ 25 à 40 fois plus de nanoparticules pour observer une perte de viabilité similaire, ce qui suggère une fenêtre de sécurité utile portée par le ciblage tumoral plutôt que par une augmentation brute de la dose.
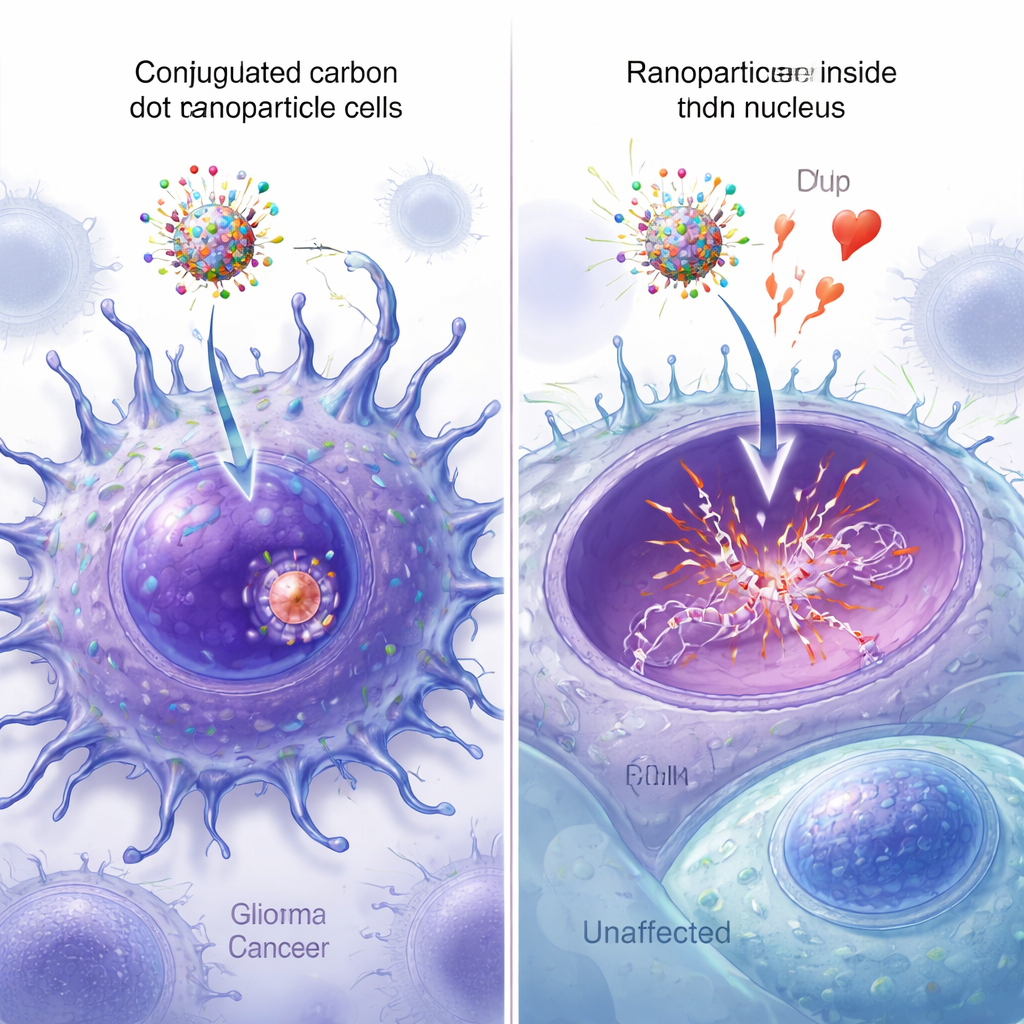
Observer les nanoparticules atteindre le noyau
Des versions fluorescentes des nanoparticules ont permis aux chercheurs d’observer l’efficacité de chaque conception pour pénétrer les cellules et atteindre le noyau. Au microscope, les points quantiques équipés des deux peptides ont montré le signal le plus intense réparti dans les cellules cancéreuses, avec un fort recouvrement entre la fluorescence verte des nanoparticules et la coloration nucléaire bleue. L’analyse d’images quantitative a confirmé que les particules à double peptide présentaient la colocalisation nucléaire la plus élevée, dépassant significativement celle des particules ne portant qu’un peptide ou aucun. Des mesures supplémentaires par spectroscopie, spectrométrie de masse et microscopie à force atomique ont vérifié que les quatre composants étaient bien attachés aux points quantiques et augmentaient modestement leur taille, sans perturber la fonction clé de liaison à l’ADN de l’épirubicine.
Ce que cela pourrait signifier pour les soins futurs des cancers cérébraux
Pour les patients, ces résultats restent une démonstration préclinique in vitro plutôt qu’une thérapie prête à l’emploi. Pourtant, ils illustrent un concept prometteur : un nanoparticule à base de carbone, petit, stable et relativement facile à fabriquer, qui peut être rapidement personnalisé avec des peptides de ciblage et des combinaisons médicamenteuses. En dirigeant les médicaments spécifiquement vers les cellules tumorales surexprimant IL13Rα2 et en les concentrant dans le noyau, de telles nanomédecines pourraient un jour permettre des doses plus faibles, moins d’effets secondaires et des stratégies de traitement plus personnalisées pour des tumeurs cérébrales hautement létales comme le glioblastome et le gliome pontique intrinsèque diffus.
Citation: Cilingir, E.K., Hettiarachchi, S.D., Rathee, P. et al. Development of a quadruple-conjugated carbon dot nanomodel for targeted glioma therapy. Commun Chem 9, 96 (2026). https://doi.org/10.1038/s42004-026-01900-3
Mots-clés: glioblastome, nanomédecine, points quantiques de carbone, transport ciblé de médicaments, tumeurs cérébrales