Clear Sky Science · fr
Un test généralisable pour l’accumulation intracellulaire visant à profiler la délivrance cytosolique de médicaments dans les cellules de mammifères
Pourquoi faire entrer des médicaments dans les cellules est important
Beaucoup des médicaments les plus prometteurs aujourd’hui — de petites molécules, de courts fragments protéiques appelés peptides, et des protéines de taille entière — sont conçus pour agir sur des cibles situées à l’intérieur de nos cellules. Mais la membrane cellulaire fait office de porte de sécurité exigeante. Un médicament peut se lier à l’extérieur d’une cellule ou rester piégé dans des sacs internes appelés endosomes sans jamais atteindre l’intérieur aqueux, le cytosol, où se trouvent de nombreuses cibles. Cet article décrit un nouveau test de laboratoire, nommé le test CHAMP, qui permet aux chercheurs de savoir non seulement si une molécule pénètre dans une cellule, mais si elle atteint réellement le cytosol, où elle peut exercer son effet.
Une nouvelle façon de suivre l’entrée des médicaments
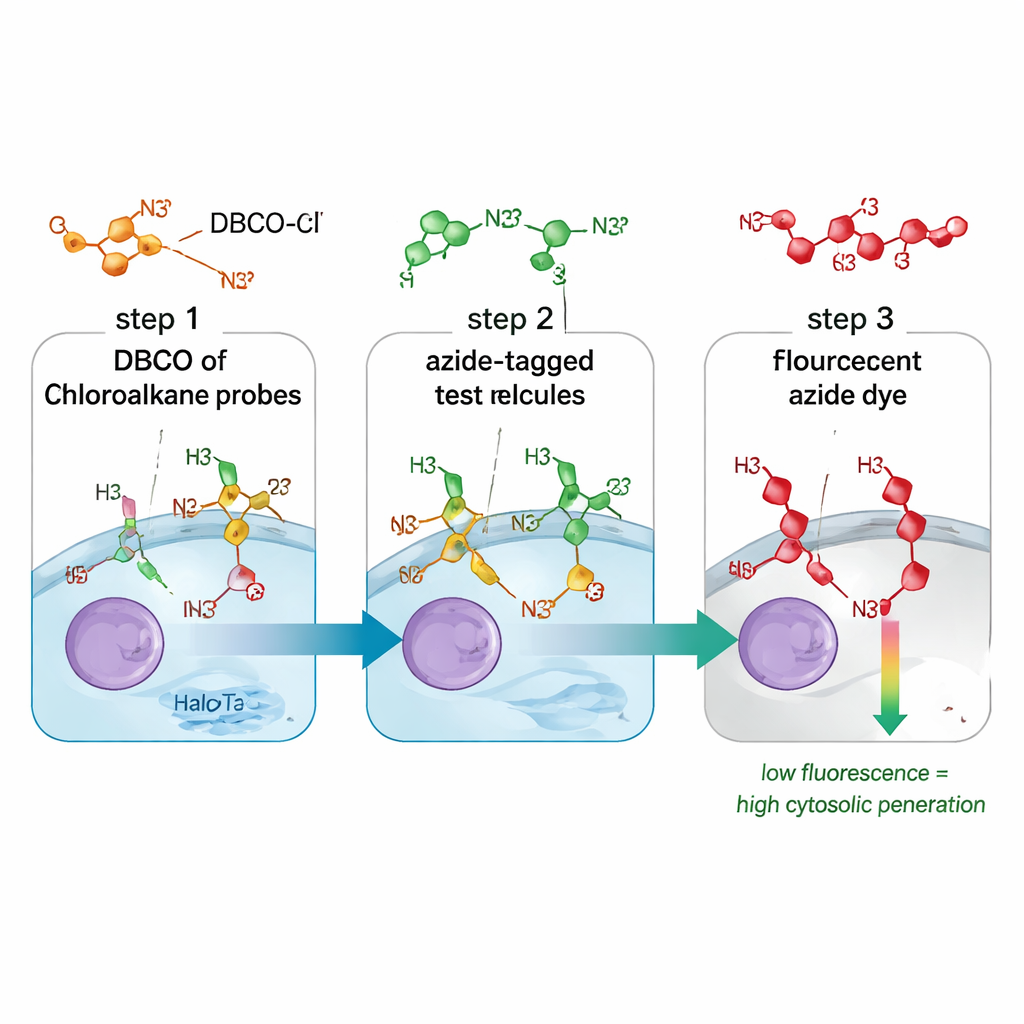
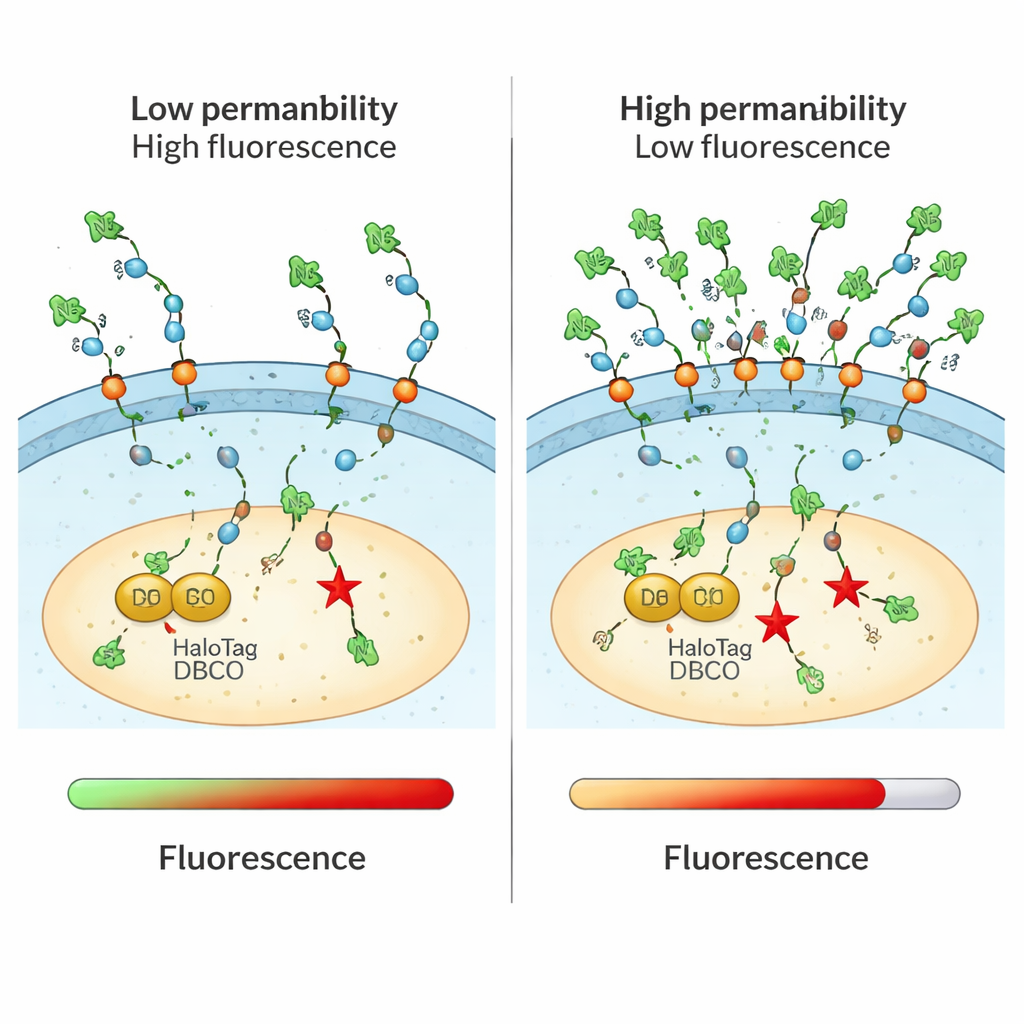
Les méthodes traditionnelles pour mesurer l’absorption des médicaments confondent souvent les molécules qui se contentent de toucher la surface cellulaire, celles qui restent dans les endosomes, et celles qui atteignent effectivement le cytosol. Elles reposent parfois aussi sur des étiquettes fluorescentes volumineuses qui modifient le comportement d’une molécule. Le test CHAMP résout ces deux problèmes en combinant une « poignée » chimique minuscule appelée azide avec un marqueur protéique nommé HaloTag, conçu pour flotter librement dans le cytosol de cellules humaines en culture. D’abord, on traite les cellules avec une molécule de liaison qui fixe le DBCO, une forme contrainte d’alkyne, sur HaloTag. Ensuite, les chercheurs ajoutent leur composé testé, portant la petite étiquette azide. Ce n’est que si ce composé traverse la membrane cellulaire et pénètre dans le cytosol que l’azide et le DBCO peuvent se « click-er » dans une réaction chimique hautement sélective. Une dernière sonde fluorescente azide révèle combien de sites DBCO restent disponibles : des cellules peu lumineuses signifient que le composé testé est entré et a occupé la plupart des sites ; des cellules lumineuses indiquent un faible accès cytosolique.
Du concept à un test opérationnel
Les auteurs ont d’abord confirmé que HaloTag était correctement produit et localisé dans le cytosol de cellules HeLa humaines en utilisant une sonde chloroalkane standard et l’imagerie. Ils ont ensuite optimisé chaque étape du CHAMP : la quantité de lien DBCO à ajouter, la durée d’incubation, et la sonde fluorescente azide offrant un signal fort et spécifique sans nuire aux cellules. La cytométrie en flux — un instrument mesurant la fluorescence de milliers de cellules individuelles — a montré que le test était rapide, robuste et ajustable. Fait crucial, l’équipe a démontré que la fluorescence provenait réellement de réactions spécifiques aux sites HaloTag plutôt que d’un dépôt non spécifique de sondes sur des composants cellulaires, et que la petite étiquette azide n’altérait pas de façon visible la façon dont les molécules entraient dans les cellules.
Ce que le test révèle sur les petites molécules et les peptides
Avec CHAMP en main, les chercheurs l’ont mis à l’épreuve sur des centaines de petites molécules marquées par un azide et ont fait varier systématiquement des caractéristiques comme la charge, la taille et la flexibilité. Ils ont observé, par exemple, que transformer un acide carboxylique chargé négativement en une amide neutre augmentait l’accumulation cytosolique, et que le degré et la position de la méthylation de certains atomes d’azote modifiaient l’aptitude des composés à pénétrer. En comparant les réactions sur billes libres versus sur cellules vivantes, ils ont pu séparer la réactivité chimique intrinsèque de la barrière imposée par la membrane elle-même. L’équipe a également appliqué CHAMP à un panel d’antibiotiques courants, montrant que certains atteignaient le cytosol bien mieux que d’autres — information cruciale pour traiter des bactéries qui se cachent à l’intérieur des cellules hôtes.
Peptides et protéines surchargés traversant la barrière
Le test s’est avéré particulièrement puissant pour étudier des molécules de plus grande taille et fortement chargées, difficiles à suivre par d’autres méthodes. Les auteurs ont examiné des peptides pénétrant les cellules composés de multiples résidus d’arginine et confirmé une tendance claire : des chaînes plus longues et plus chargées positivement délivraient davantage de matière dans le cytosol, jusqu’à un certain point. Ils ont étudié comment l’inversion de la chiralité de certains acides aminés affectait l’entrée, constatant que des versions en image miroir s’accumulaient parfois mieux, suggérant des interactions chirales subtiles avec la membrane. CHAMP a aussi montré que des protéines « surchargées » — conçues pour porter de nombreuses charges positives — pouvaient atteindre le cytosol plus efficacement que leurs homologues normales, soutenant leur potentiel en tant que vecteurs pour de grosses cargaisons thérapeutiques.
Règles de conception pour les futurs médicaments intracellulaires
En testant systématiquement des petites molécules, des peptides, des macrocycles peptidiques et des squelettes modifiés, l’étude a mis au jour des principes généraux de conception. Les peptides macrocycliques, dont l’épine dorsale est fermée en anneau, avaient tendance à atteindre le cytosol plus facilement que des versions linéaires et flexibles. Des groupes N‑méthyle placés avec soin sur l’épine dorsale peptidique augmentaient modestement l’entrée, mais un excès pouvait être contre‑productif. Ces relations structure‑perméation, révélées avec un test standardisé unique, offrent des indications pratiques pour les chimistes cherchant à concevoir des molécules qui non seulement se lient à leurs cibles, mais peuvent aussi réellement les atteindre à l’intérieur des cellules.
Comment cela aide le développement de médicaments
En termes simples, le test CHAMP est un compteur de trafic finement réglé à la porte d’entrée et dans le couloir intérieur de la cellule. Il indique aux scientifiques quels médicaments expérimentaux franchissent réellement la membrane et atteignent le cytosol, sans être induits en erreur par des molécules coincées à la surface ou dans des compartiments internes. Parce qu’il fonctionne avec une grande variété de formes et de tailles moléculaires et n’utilise qu’une petite étiquette azide, CHAMP peut être intégré dans des pipelines de découverte à haut débit. Avec le temps, cela devrait accélérer la conception de traitements plus efficaces pour des maladies où les cibles les plus importantes sont enfermées à l’intérieur de nos cellules.
Citation: Bhandari, S., Ongwae, G.M., Dash, R. et al. A generalizable assay for intracellular accumulation to profile cytosolic drug delivery in mammalian cells. Commun Chem 9, 94 (2026). https://doi.org/10.1038/s42004-026-01898-8
Mots-clés: transport intracellulaire de médicaments, perméabilité de la membrane cellulaire, accumulation cytosolique, peptides pénétrant les cellules, chimie click bioorthogonale