Clear Sky Science · fr
Déshydrochloruration assistée par hydrogène du 1,1,1,2-tétrafluoro-2-chloropropane en 2,3,3,3-tétrafluoropropène sur Pd-Ag/nano-MgF2 avec des sites Pd isolés optimisés
Des fluides frigorigènes plus propres pour un monde qui se réchauffe
Les climatiseurs et les réfrigérateurs nous apportent du confort, mais nombre des substances qui les font fonctionner sont de puissants gaz à effet de serre. Cette étude s’attaque à un enjeu crucial : produire l’un des réfrigérants de nouvelle génération les plus importants, le HFO‑1234yf, de manière plus efficace et avec une empreinte carbone réduite. En concevant un catalyseur plus intelligent — essentiellement une machine chimique microscopique — les auteurs montrent une voie pour synthétiser ce réfrigérant à faible potentiel de réchauffement à des températures plus basses et avec beaucoup moins de sous-produits indésirables.
Pourquoi améliorer la chimie des réfrigérants
Les hydrofluorocarbures (HFC) traditionnels, comme le HFC‑134a utilisé dans les climatiseurs automobiles, retiennent la chaleur dans l’atmosphère des milliers de fois plus efficacement que le dioxyde de carbone. Des accords internationaux tels que l’amendement de Kigali en prévoient la réduction, poussant l’industrie vers les hydrofluorooléfines (HFO), qui offrent des performances similaires mais avec un potentiel de réchauffement global beaucoup plus faible (souvent inférieur à 10). Le HFO‑1234yf est le principal candidat de remplacement, mais les méthodes industrielles actuelles pour le produire reposent sur des étapes à haute température, énergivores, qui raccourcissent aussi la durée de vie des catalyseurs et augmentent les déchets. Une voie plus douce et plus sélective vers le HFO‑1234yf pourrait donc réduire à la fois les émissions et les coûts d’exploitation.
Une voie plus douce vers une molécule clé
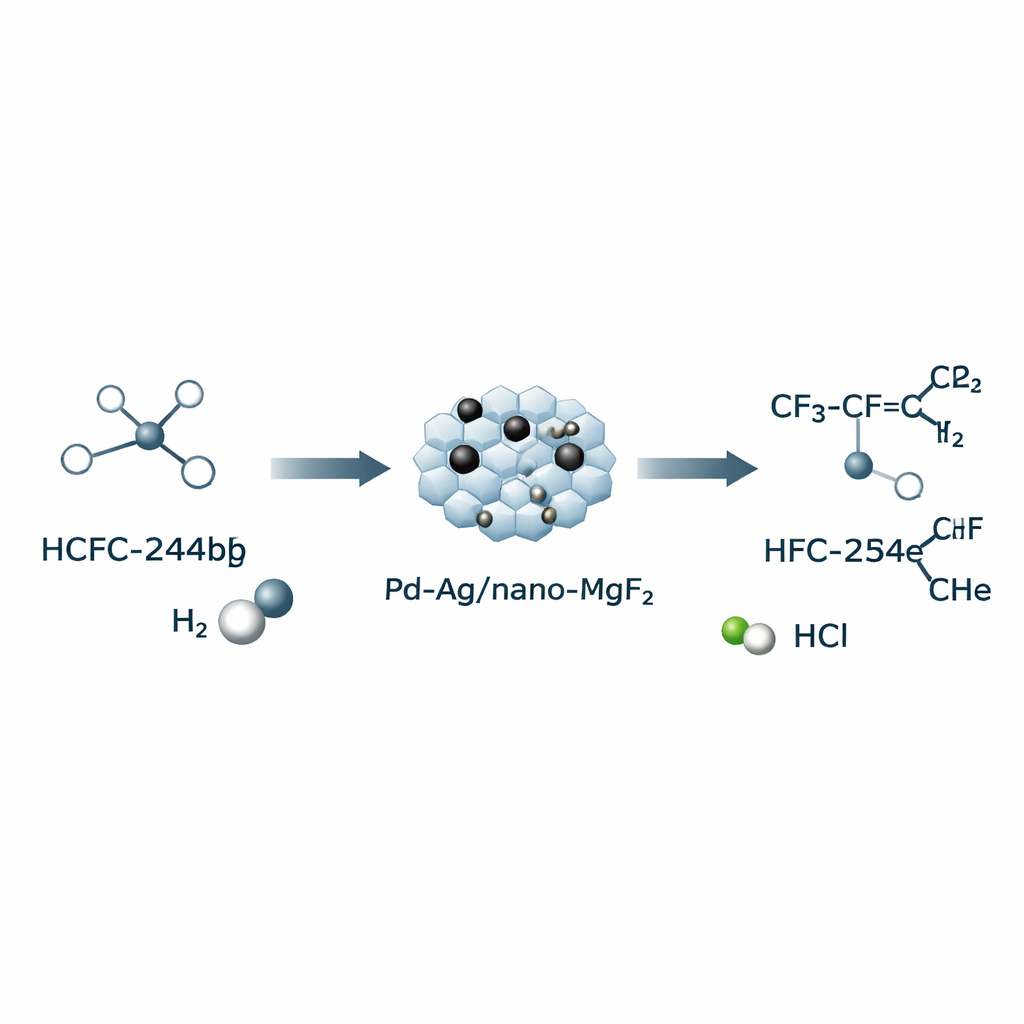
Les auteurs se concentrent sur la conversion d’un composé apparenté, le HCFC‑244bb, en HFO‑1234yf par élimination d’acide chlorhydrique (HCl) aidée par de l’hydrogène gazeux. Cette « déshydrochloruration assistée par hydrogène » permet à la réaction d’avoir lieu à une température relativement modérée de 270 °C — bien en dessous des 600–800 °C souvent nécessaires pour des méthodes purement thermiques. L’élément central du procédé est un catalyseur solide sur mesure : de petites particules creuses de fluorure de magnésium (nano‑MgF₂) décorées de palladium (Pd) et d’argent (Ag). En modifiant l’ordre d’introduction du Pd et de l’Ag lors de la préparation, l’équipe peut contrôler le degré de mélange des deux métaux — formant des alliages de nature différente — et la manière dont les sites actifs de Pd apparaissent finalement en surface pendant la réaction.
Transformer des amas métalliques en atomes isolés
Au cours des premières heures d’opération, les catalyseurs présentent une « période d’induction » : la conversion du HCFC‑244bb diminue lentement, tandis que la sélectivité vers le HFO‑1234yf désiré augmente régulièrement. Une microscopie, une spectroscopie et des mesures de surface attentives expliquent pourquoi. Au fur et à mesure de la réaction, l’acide chlorhydrique formé in situ chlorure les particules métalliques, fragmentant les plus gros agrégats de Pd et les reformant en atomes de Pd isolés ancrés à la surface du nano‑MgF₂. Les catalyseurs qui commencent avec un degré d’alliage Pd–Ag plus élevé — obtenu lorsque le Pd est ajouté en premier, puis l’Ag — subissent la restructuration la plus étendue et aboutissent à la plus grande densité de sites Pd monoatomiques. Ce matériau optimisé convertit environ 60 % du HCFC‑244bb et oriente près de 82 % du produit vers le HFO‑1234yf, tout en supprimant fortement l’hydrogénation plus profonde vers un composé saturé indésirable, le HFC‑254eb.
Comment le comportement de l’hydrogène contrôle le résultat
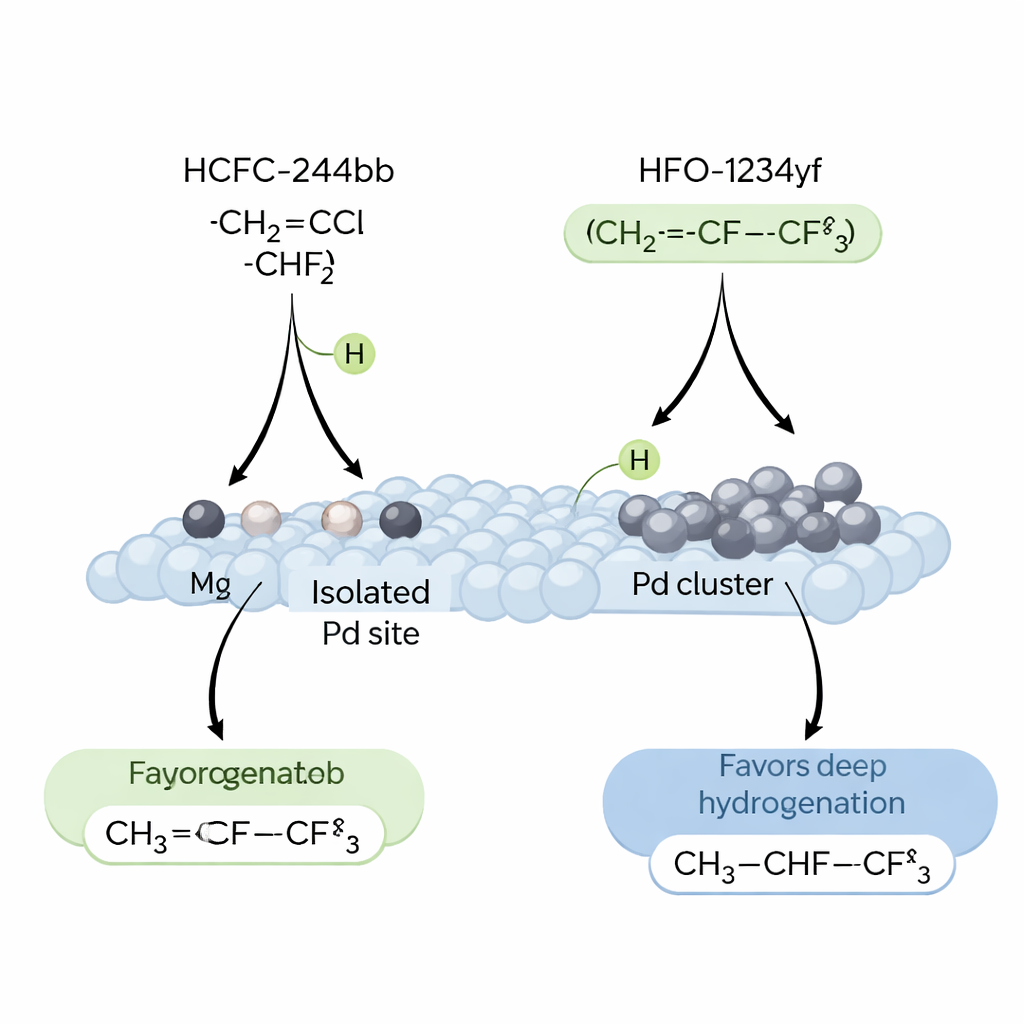
Pour comprendre pourquoi les atomes de Pd isolés sont si performants, les chercheurs ont étudié comment l’hydrogène, la molécule réactante et le produit interagissent avec différentes surfaces catalytiques. Ils ont constaté que le HCFC‑244bb et l’hydrogène préfèrent tous deux s’adsorber sur le Pd plutôt que sur l’Ag, mais que la force et la nature de la liaison de l’hydrogène sont déterminantes. Les gros agrégats de Pd ont tendance à créer un « débordement » d’hydrogène qui reste fortement lié à haute température et favorise la sur‑hydrogénation, transformant le précieux HFO‑1234yf en produits saturés moins utiles. En revanche, les sites Pd monoatomiques retiennent l’hydrogène dans une forme plus réactive mais moins persistante, idéale pour éliminer proprement le HCl et former la double liaison carbone–carbone souhaitée. Des simulations par théorie de la fonctionnelle de la densité viennent étayer ces observations, montrant que ces environnements Pd–fluorure isolés facilitent l’extraction d’hydrogène des intermédiaires clés sur la voie du HFO‑1234yf, tout en rendant les étapes secondaires d’hydrogénation énergétiquement moins favorables.
Du regard en laboratoire à un refroidissement plus vert
En termes pratiques, le meilleur catalyseur Pd–Ag/nano‑MgF₂ fournit des taux de formation de HFO‑1234yf des dizaines de fois supérieurs à ceux des premiers catalyseurs solides qui reposaient sur des déshydrochlorurations sévères à haute température. Ce travail montre que contrôler les atomes métalliques un par un — et pas seulement sous forme de nanoparticules — peut orienter fortement les voies réactionnelles, améliorant à la fois l’efficacité et la sélectivité. Pour les non‑spécialistes, le message clé est que de meilleurs designs catalytiques peuvent se traduire directement par une production plus propre des réfrigérants modernes. Cela aide, à son tour, le monde à atteindre ses objectifs climatiques tout en maintenant nos bâtiments, véhicules et approvisionnements alimentaires au frais.
Citation: Yang, C., Mao, W., Dong, X. et al. Hydrogen-assisted dehydrochlorination of 1,1,1,2-tetrafluoro-2-chloropropane to 2,3,3,3-tetrafluoropropene over Pd-Ag/nano-MgF2 with optimized Pd isolated sites. Commun Chem 9, 93 (2026). https://doi.org/10.1038/s42004-026-01896-w
Mots-clés: réfrigérants, catalyse, palladium-argent, gaz à effet de serre, hydrofluorooléfines