Clear Sky Science · fr
Activation de l’ADNzyme par surface métallique pour une clivage efficace de l’ADN
Des métaux qui font que l’ADN se coupe lui-même
La plupart d’entre nous considèrent le métal comme quelque chose de solide et inerte — utile pour les pièces, les casseroles ou les fils, mais pas pour de la chimie dans un verre d’eau. Cette étude renverse cette intuition en montrant que de simples morceaux de métal peuvent activer de minuscules catalyseurs à base d’ADN, appelés ADNzymes, avec rien d’autre que de l’eau pure et l’air. Le travail révèle une manière inattendue par laquelle des matériaux quotidiens comme le cuivre et d’autres métaux peuvent piloter des réactions de type biologique à leur surface, suggérant de nouveaux outils pour les capteurs, la médecine et même la chimie des origines de la vie. 
Qu’est-ce que des ciseaux à ADN ?
Les ADNzymes sont de courts brins d’ADN qui se replient en formes capables d’accélérer des réactions chimiques spécifiques, un peu comme le font les enzymes protéiques. De nombreux ADNzymes connus agissent comme des ciseaux moléculaires qui coupent d’autres brins d’ADN ou d’ARN, mais ils nécessitent presque toujours des ions métalliques dissous — comme le cuivre, le zinc ou le magnésium — en solution pour fonctionner. Un ADNzyme particulier, appelé PL, est un brin auto‑clivant qui dépend normalement des ions cuivre et de certains auxiliaires tels que la vitamine C ou le peroxyde d’hydrogène. Ces auxiliaires participent à des réactions rédox (transfert d’électrons) qui génèrent des espèces réactives de l’oxygène très agressives, lesquelles attaquent ensuite et rompent l’échafaudage de l’ADN à des positions précises.
Quand un fil de cuivre devient un cofacteur
En explorant un montage électrochimique pour contrôler l’activité de PL, les chercheurs ont remarqué quelque chose de surprenant : tremper simplement un fil de cuivre nu dans une solution contenant PL et de l’eau doublement distillée conduisait à un clivage efficace de l’ADN, sans ions cuivre ajoutés, sans tampons ni sels. La surface de cuivre à elle seule égalait ou surpassait les mélanges traditionnels d’ions cuivre plus vitamine C ou peroxyde d’hydrogène, et elle coupait l’ADN exactement au même site. Des tests complémentaires ont montré que de nombreux objets en cuivre — feuilles, entonnoirs, casseroles et même des pièces de monnaie de différentes devises — pouvaient déclencher le clivage par PL, l’étendue de la réaction dépendant de la surface métallique en contact avec la goutte. Un cuivre fraîchement poli fonctionnait légèrement moins bien que du cuivre vieillissant et oxydé, ce qui suggère qu’une fine couche formée par l’exposition à l’air pourrait en fait favoriser la réaction.
Quelles surfaces fonctionnent — et pourquoi
Pour vérifier si ce phénomène était propre au cuivre, l’équipe a testé 24 métaux et 10 matériaux non métalliques. Ils ont constaté que seuls certains métaux, comme le cuivre, le tantale et le vanadium, activaient fortement PL, tandis que le verre, le plastique, le bois et d’autres non‑métaux ne faisaient rien. Les mesures ont montré que de faibles quantités d’ions métalliques se dissolvaient dans l’eau à partir des surfaces actives, mais ces ions seuls étaient trop faibles pour expliquer le clivage intense observé. L’ingrédient manquant s’est révélé être de l’oxygène réactif dérivé de l’air dissous. À l’aide de piégeurs chimiques et d’enzymes, les auteurs ont montré que le superoxyde — une forme énergique d’oxygène avec un électron supplémentaire — est essentiel. Lorsque l’oxygène dissous était éliminé par dégazage au diazote, l’activité de PL disparaissait presque ; laisser l’oxygène revenir restaurait le clivage. Dans l’ensemble, les données étayent un cycle dans lequel la surface métallique et ses ions lessivés convertissent l’oxygène dissous en superoxyde et en peroxyde d’hydrogène à l’interface solide‑liquide, et ces espèces entraînent ensuite la scission de l’ADN. 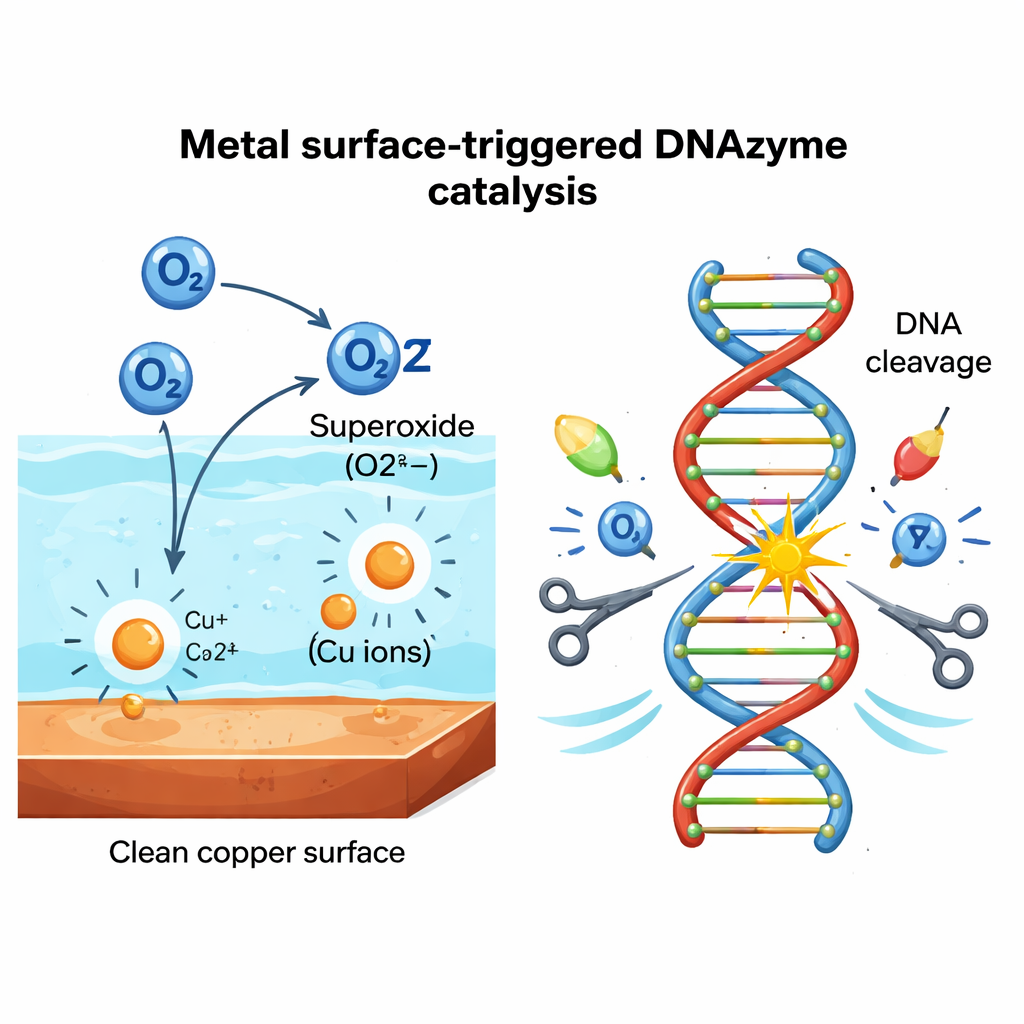
Auxiliaires, bloqueurs et autres ADNzymes
La chimie déclenchée en surface pouvait être modulée à la hausse ou à la baisse avec des molécules bien connues. Les chélateurs comme l’EDTA, qui captent les ions métalliques, ralentissaient la réaction. La catalase, une enzyme qui décompose le peroxyde d’hydrogène, et des colorants qui éliminent le superoxyde réduisaient également le clivage de l’ADN, confirmant le rôle de ces espèces réactives de l’oxygène. En revanche, de petites molécules telles que la vitamine C, le glutathion et la catéchol augmentaient l’activité en alimentant le cycle rédox qui produit le superoxyde près de la surface métallique. Fait remarquable, l’effet n’était pas unique à PL : d’autres ADNzymes coupant l’ADN ou l’ARN, notamment F‑8, Ag10c et I‑R3, ont aussi été activés par les métaux massifs correspondants (par exemple, l’argent métallique pour un ADNzyme dépendant de l’argent et le zinc métallique pour un ADNzyme dépendant du zinc). Cela suggère que la catalyse d’ADN « activée par surface métallique » pourrait être un phénomène large plutôt qu’une curiosité isolée.
Pourquoi cela importe au‑delà du laboratoire
Pour les non‑spécialistes, le message central est que des surfaces métalliques solides peuvent agir comme des partenaires chimiques invisibles pour des catalyseurs à base d’ADN, utilisant seulement l’air et l’eau pour générer les espèces réactives nécessaires au clivage de l’ADN. Au lieu de devoir dissoudre des quantités précises d’ions métalliques, on peut simplement toucher une surface métallique appropriée à une solution d’ADN et laisser l’interface faire le travail. Cela ouvre des possibilités pour des capteurs peu coûteux signalant la présence d’objets métalliques, des outils pour surveiller ou éliminer des radicaux d’oxygène nocifs dans les cellules, et de nouvelles façons d’étudier comment des réactions de type vivant pourraient se produire sur des surfaces minérales ou métalliques. En bref, votre pièce en cuivre n’est pas seulement de la monnaie — elle peut aussi être une minuscule usine chimique pour des ciseaux à ADN.
Citation: Jiang, F., Dong, Y., Yu, W. et al. Metal surface-triggered DNAzyme catalysis for efficient DNA cleavage. Commun Chem 9, 91 (2026). https://doi.org/10.1038/s42004-026-01893-z
Mots-clés: ADNzyme, catalyse en surface métallique, espèces réactives de l’oxygène, chimie d’interface du cuivre, clivage de l’ADN