Clear Sky Science · fr
Croissance contrôlée de cristaux spherulitiques à partir de mélanges salins
Pourquoi les cristaux de sel peuvent ressembler à des fleurs
La plupart d’entre nous imaginent les cristaux comme des formes nettes et facettées, mais dans la nature ils poussent souvent en sphères spectaculaires qui rappellent des fleurs ou des boules de neige. Ces « sphérulites » apparaissent dans les roches volcaniques, les calculs rénaux et même dans certaines maladies liées à des protéines mal repliées. Cet article explore comment un minéral courant, le sulfate de sodium — le même sel utilisé dans des détergents et certains matériaux de construction — peut être amené à former de tels cristaux sphériques complexes, et ce que cela révèle sur la façon dont des structures élaborées s’auto-assemblent à partir d’ingrédients simples.
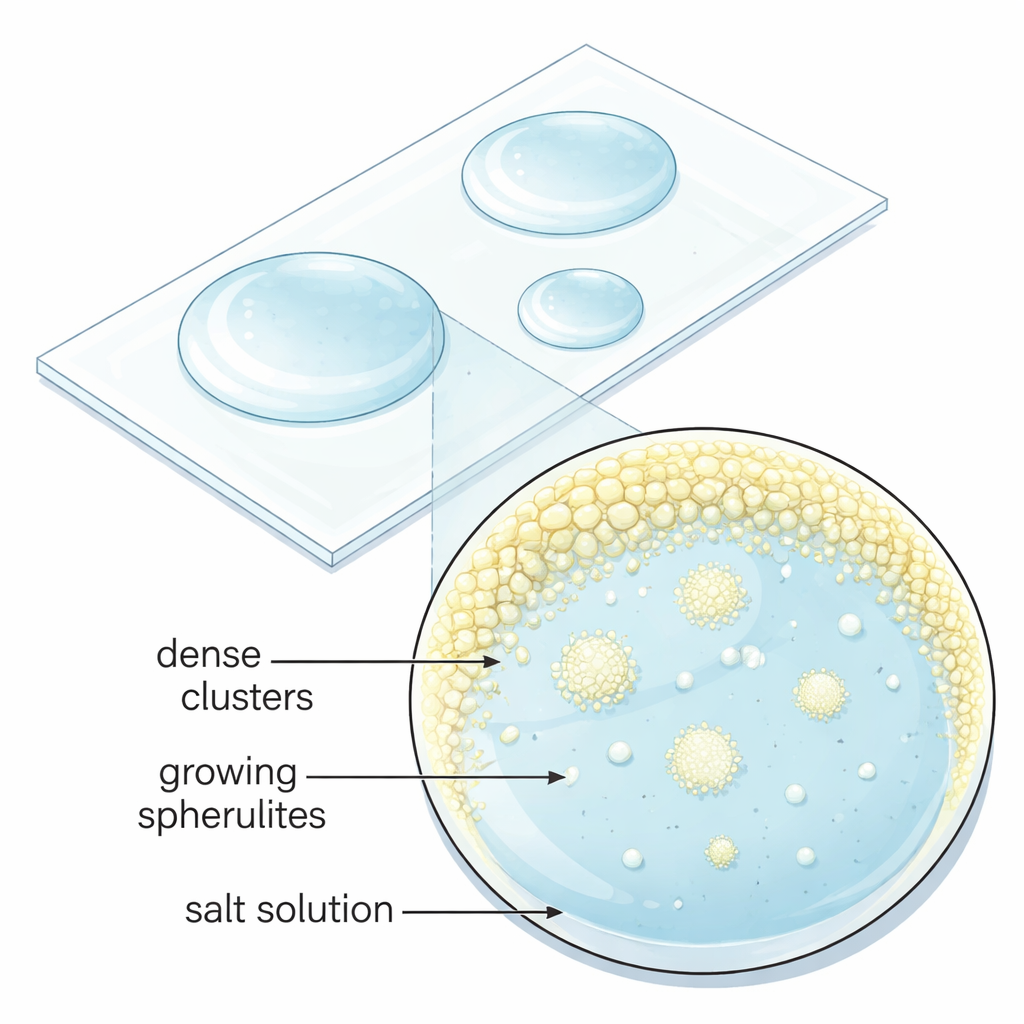
Des sels simples aux sphères sculptées
Les chercheurs ont cherché à comprendre quand et comment le sulfate de sodium croît en sphérulites plutôt qu’en cristaux blocaux ordinaires. Ils ont préparé de minuscules gouttelettes d’eau contenant des mélanges de sulfate de sodium et d’autres sulfates dont les ions métalliques portent deux charges positives, comme le magnésium ou le fer. À mesure que ces gouttelettes picolitre à microlitre s’évaporaient lentement sur des lames de verre à température ambiante, les sels dissous se concentraient de plus en plus jusqu’à l’apparition des cristaux. En faisant varier systématiquement le rapport de mélange, ils ont identifié des « zones de prédilection » de composition où le sulfate de sodium produisait systématiquement des cristaux sphériques à texture radiale. En dehors de ces plages, la même solution donnait soit des grains facettés réguliers, soit un solide informe de type gel, montrant que les formes sphériques nécessitent des conditions finement ajustées.
De minuscules poches liquides qui initient les sphères cristallines
Au microscope, l’équipe a observé que les sphérulites n’apparaissaient pas directement à partir d’une solution claire. L’évaporation créait d’abord de petits agrégats liquides denses enrichis en ions dissous près du bord de la gouttelette. Ces poches de l’ordre du micron persistaient pendant des minutes avant de donner soudainement naissance à de nombreuses sphérulites en une fois. Des images électroniques à haute résolution des structures séchées ont révélé que chaque sphérulite est constituée d’innombrables cristaux de sulfate de sodium à l’échelle nanométrique, orientés à peu près vers l’extérieur, qui se fusionnent ensuite. Ce comportement contredit le portrait classique de la croissance cristalline, où un seul nucléus stable croît de manière continue, et indique plutôt une voie en plusieurs étapes « non classique » dans laquelle des gouttelettes denses et des nanoparticules s’assemblent et se réorganisent avant d’aboutir à la forme solide finale.
Quand l’eau salée devient consistante comme du beurre de cacahuète
Un élément crucial de l’histoire est la viscosité que prend la solution à mesure que l’eau s’évapore. En suivant la vitesse d’expansion des sphérulites et en mesurant directement les propriétés d’écoulement de solutions salines apparentées, les auteurs montrent que les solutions mixtes sodium–magnésium ou sodium–fer deviennent extraordinairement visqueuses — jusqu’à environ 100 fois plus épaisses que le miel — précisément au moment où les sphérulites commencent à se former. Cette consistance proche du « beurre de cacahuète » ralentit tellement le mouvement des ions que c’est la diffusion, et non la chimie de surface, qui limite la vitesse de croissance des cristaux. Dans cet environnement visqueux, d’innombrables petits agrégats et nanocristaux se forment et ont le temps de s’agréger en agrégats sphériques plutôt que de croître en quelques gros cristaux bien formés. Les ions métalliques divalents sont déterminants : ils lient fortement l’eau et forment des chaînes ou réseaux courts, ce qui augmente la viscosité et favorise l’apparition d’un fond amorphe, de type gel, autour des sphérulites en croissance.
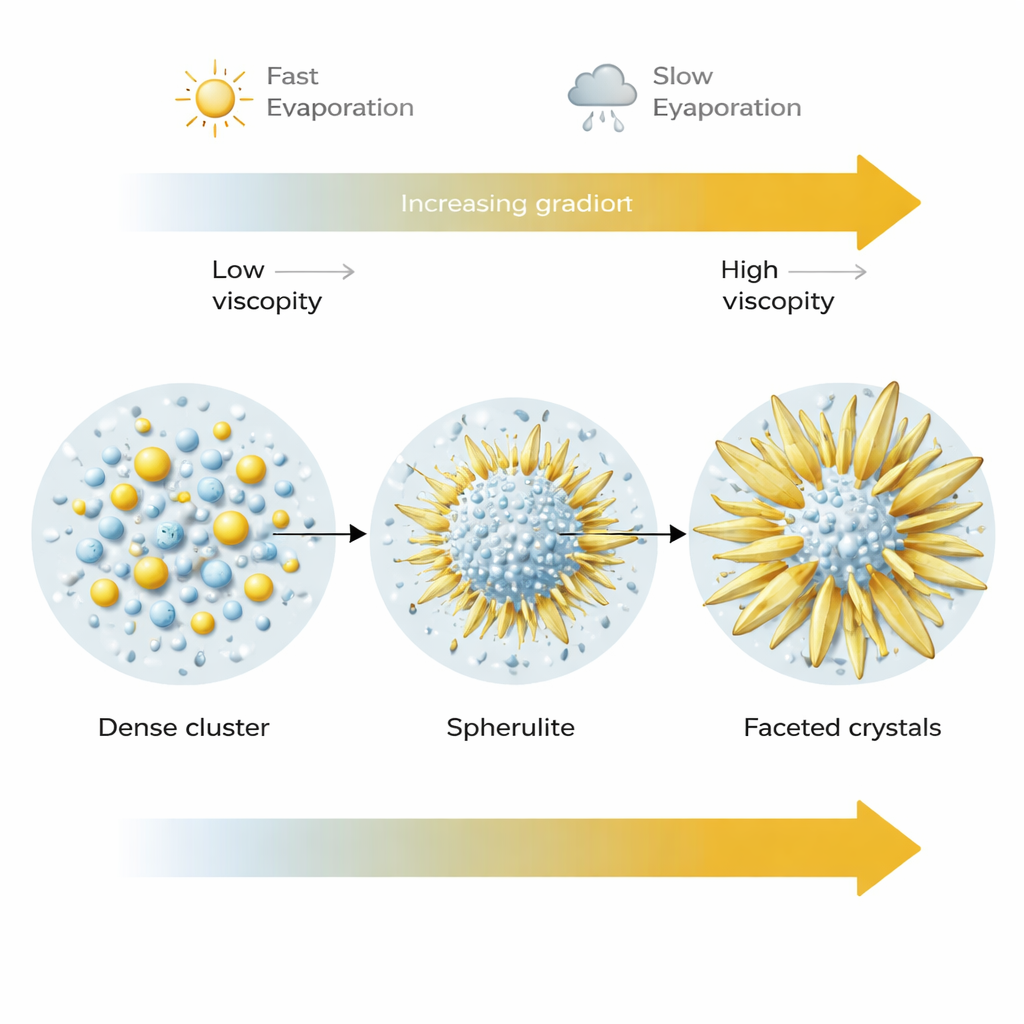
Comment la vitesse de séchage remodèle les cristaux finaux
La vitesse d’évaporation s’est révélée un autre réglage puissant. À un séchage plus rapide (humidité plus basse), de nombreuses sphérulites ont nucléés mais sont restées relativement petites, verrouillées dans leur forme sphérique métastable alors que le fluide environnant épaississait rapidement. À un séchage plus lent (humidité plus élevée), ces mêmes sphères initiales disposaient de plus de temps et d’un meilleur accès aux ions dissous. Leurs petits éléments constitutifs pouvaient se réarranger et fusionner en cristaux plus grands, plus lisses et plus facettés, produisant souvent des excroissances en lame qui finissaient par se convertir en la forme thermodynamiquement stable du sulfate de sodium. Autrement dit, les structures sphériques agissent comme une étape transitoire dans un parcours de croissance qui peut aboutir à des formes très différentes selon la rapidité du séchage et la facilité de déplacement des matériaux à l’intérieur de la solution.
Pourquoi cela compte au-delà de la beauté des cristaux
Concrètement, l’étude montre que de belles sphères salines en forme de fleur surgissent lorsque des mélanges concentrés de sels simples deviennent assez épais pour ralentir tout, mais pas au point d’arrêter complètement la croissance. Dans ces conditions « idéales », des poches liquides denses et des nuées de petits cristaux s’auto-assemblent en agrégats sphériques qui peuvent ensuite évoluer vers des grains facettés plus stables. Comprendre et contrôler cet équilibre délicat entre composition, viscosité et évaporation ouvre la voie à la conception de textures cristallines sur mesure pour des applications allant de matériaux de construction plus résistants et de meilleurs produits pharmaceutiques à de meilleurs modèles de la formation cristalline en géologie et en biologie.
Citation: Heeremans, T., Lépinay, S., Le Dizès Castell, R. et al. Controlled spherulitic crystal growth from salt mixtures. Commun Chem 9, 90 (2026). https://doi.org/10.1038/s42004-026-01892-0
Mots-clés: sphérulites, sulfate de sodium, croissance cristalline, nucléation non classique, solutions salines