Clear Sky Science · fr
Première structure cristalline d’un adduit formé lors de la réaction d’un composé de vanadium avec la transferrine sérique humaine
Pourquoi une protéine sanguine et un médicament métallique comptent
De nombreux médicaments expérimentaux contiennent des atomes métalliques susceptibles d’aider à traiter des maladies allant du diabète au cancer. Mais une fois ces médicaments à base de métaux dans le sang, ils doivent s’attacher aux protéines de transport naturelles de l’organisme. Cette étude examine comment l’une de ces protéines, la transferrine sérique humaine — le principal transporteur du fer dans notre sang — interagit avec un composé prometteur de vanadium, éclairant la façon dont les médicaments métalliques sont transportés dans l’organisme et comment ils pourraient être optimisés pour des thérapies plus sûres et plus efficaces.
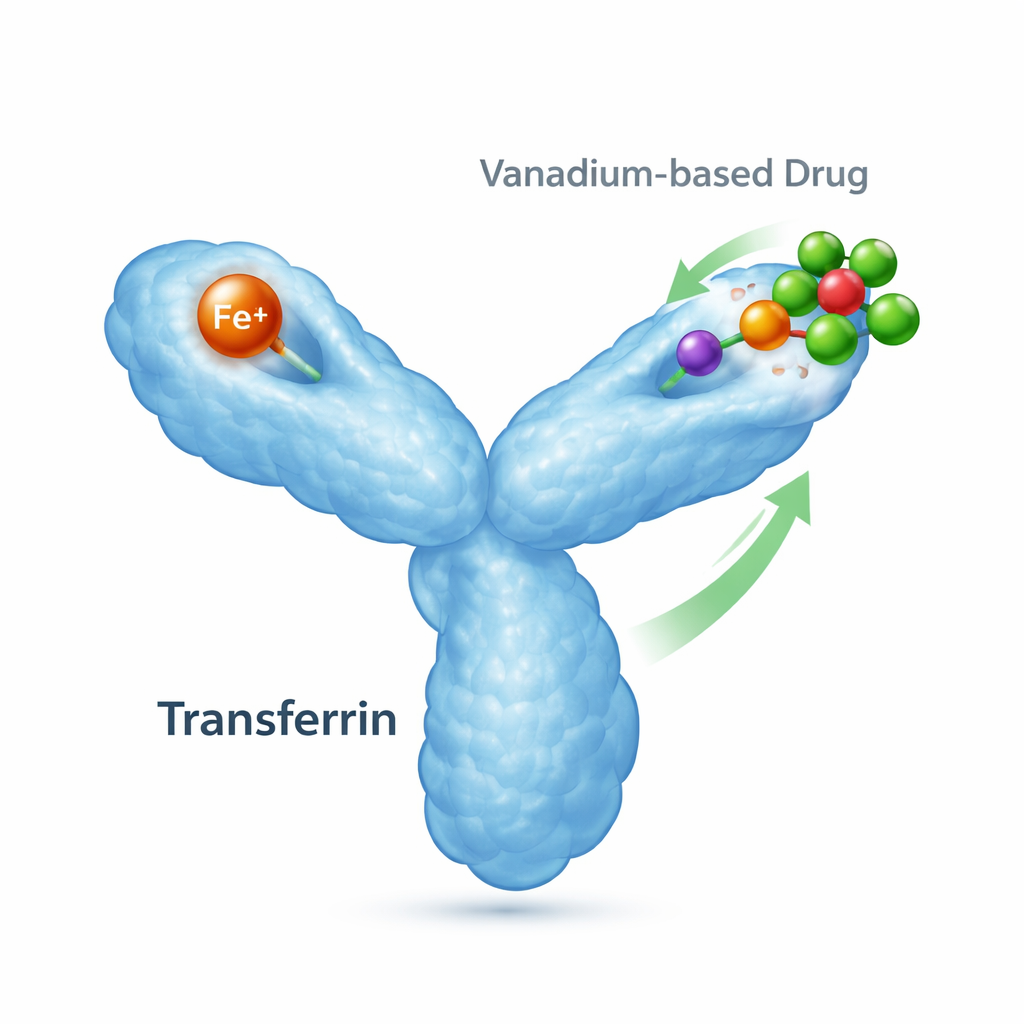
Le coursier du fer de l’organisme et ses missions secondaires
La transferrine est une protéine de 80 kilodaltons dont la fonction principale est de capturer le fer et de le livrer aux cellules qui en ont besoin. Elle possède deux « lobes », chacun capable de lier un ion fer, et elle change de conformation selon la présence du fer. Quand le fer se lie, un lobe se referme ; sans fer, il reste ouvert. Des récepteurs spécialisés à la surface des cellules reconnaissent ces formes chargées en fer et les internalisent, faisant de la transferrine un élément central de l’équilibre du fer et de la santé cellulaire. Cependant, la transferrine peut aussi lier d’autres métaux, y compris issus de traitements médicaux, ce qui signifie qu’elle peut influencer où les médicaments métalliques se déplacent et comment ils agissent.
Un instantané structural du vanadium sur la transferrine
Les chercheurs se sont intéressés à un candidat-médicament au vanadium bien étudié, le bis(acétylacétonato)oxovanadium(IV), souvent noté [VIVO(acac)₂]. Des travaux antérieurs avaient montré que ce composé, ou des espèces dérivées de celui-ci en milieu aqueux, peut se fixer à la transferrine, mais personne n’avait observé précisément comment. En utilisant la cristallographie aux rayons X, l’équipe a obtenu des structures à haute résolution de la transferrine portant du fer uniquement dans son lobe C-terminal (la forme « FeC »), avant et après exposition au médicament au vanadium. Dans les cristaux traités au vanadium, ils n’ont pas observé la molécule originale, mais un fragment transformé à base de vanadium et d’oxygène lié dans le lobe N-terminal dépourvu de fer. Cela leur a fourni la première image structurelle directe d’un fragment de vanadium attaché à la transferrine humaine.
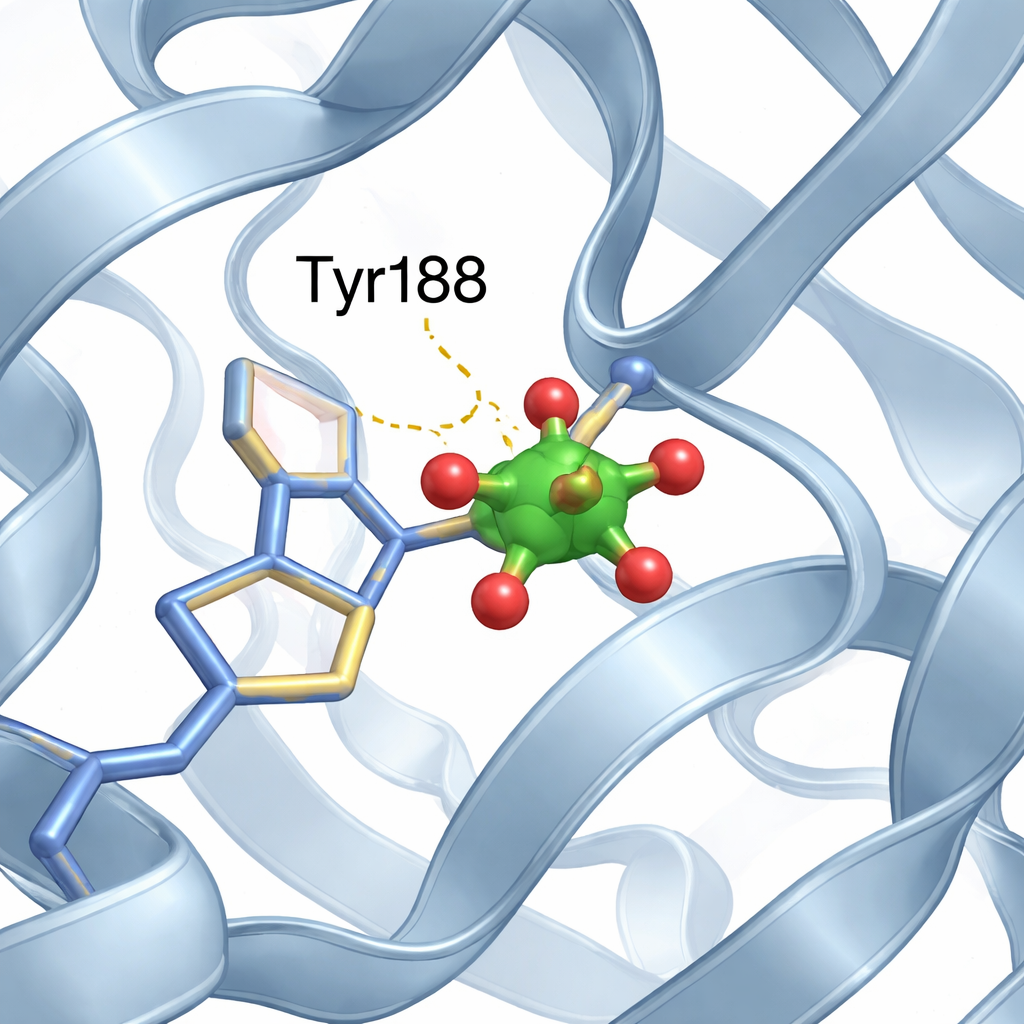
Un petit agrégat de vanadium trouve sa place
Dans le site à fer du lobe N, l’équipe a identifié un petit agrégat composé de deux atomes de vanadium et d’atomes d’oxygène, mieux décrit comme une unité « divanadate » modifiée. Une des positions d’oxygène de l’agrégat est remplacée par l’oxygène d’un acide aminé spécifique, la tyrosine 188 (Tyr188), formant une liaison directe entre la protéine et l’agrégat métallique. Des interactions supplémentaires, plus douces, comme des liaisons hydrogène provenant de segments protéiques voisins, stabilisent encore l’agrégat en place. Il est important de noter que, malgré la présence de cet invité métallique dans une poche de liaison au fer, la protéine conserve son arrangement usuel avec le lobe N ouvert et le lobe C fermé, presque identique à la structure sans vanadium.
Comment la transferrine remodèle la chimie du vanadium
En solution, aux pH et concentrations utilisés pour la cristallisation, l’espèce à deux vanadium observée dans le cristal est normalement minoritaire ; des agrégats vanadium–oxygène plus grands tendent à dominer. Des mesures spectroscopiques et des calculs de spéciation théorique suggèrent que le médicament initial au vanadium s’oxyde lentement et se décompose dans l’eau, produisant de simples ions vanadate qui s’assemblent ensuite en une variété d’agrégats. La structure cristalline indique que la transferrine stabilise sélectivement ce petit fragment de type divanadate plutôt que les agrégats plus volumineux, « choisissant » essentiellement une forme chimique au sein d’un mélange de solution encombré en fournissant un site de liaison ajusté autour de Tyr188 et un réseau de liaisons hydrogène favorable.
Conserver sa poignée de main avec le récepteur cellulaire
Comme la transferrine doit se lier à un récepteur à la surface des cellules pour délivrer le fer, les chercheurs se sont demandé si la fixation de cet agrégat de vanadium perturberait cette poignée de main cruciale. À l’aide d’électrophorèse non dénaturante et d’une technique sensible appelée interférométrie en biocouche, ils ont mesuré l’affinité de la transferrine traitée au vanadium pour le récepteur de la transferrine en comparaison avec la forme non traitée contenant uniquement du fer. Les deux se comportaient presque de manière identique, avec une liaison très forte dans la gamme des centaines à dizaines de nanomoles basses. Cela confirme que l’agrégat de vanadium, bien qu’encastré dans le lobe N, n’altère pas de manière significative la conformation de la transferrine au niveau de l’interface avec le récepteur, et ne devrait donc pas empêcher la reconnaissance de la protéine par les cellules.
Ce que cela signifie pour les médicaments à base de métaux
Pour les non-spécialistes, la conclusion est que cette étude fournit un instantané moléculaire de la manière dont un dérivé de médicament au vanadium se fixe au principal transporteur de fer de l’organisme sans compromettre sa fonction normale. La transferrine peut capturer un petit agrégat vanadium–oxygène spécifique dans un site de liaison au fer, tout en conservant sa conformation globale et sa capacité à lier son récepteur. Cela aide à expliquer comment les médicaments au vanadium peuvent circuler attachés à la transferrine et souligne que différentes protéines peuvent favoriser des tailles d’agrégats de vanadium différentes. Ces informations sont essentielles pour concevoir des thérapies métalliques plus intelligentes dont le comportement dans le sang — quelles formes elles adoptent, où elles vont et combien de temps elles persistent — peut être prédit et contrôlé.
Citation: Banneville, AS., Lucignano, R., Paolillo, M. et al. First crystal structure of an adduct formed upon reaction of a vanadium compound with human serum transferrin. Commun Chem 9, 89 (2026). https://doi.org/10.1038/s42004-026-01891-1
Mots-clés: médicaments à base de vanadium, transferrine sérique humaine, thérapeutiques à base de métaux, liaison protéine–métal, biologie structurale