Clear Sky Science · fr
Le lactame permet des réarrangements boronates à distance vers des liaisons C═N
Un nouveau raccourci pour construire des molécules de type médicament
Les chimistes recherchent en permanence des méthodes plus rapides et plus propres pour assembler les molécules complexes présentes dans les médicaments et les matériaux avancés. Cette étude présente un raccourci astucieux : une structure cyclique courante, appelée lactame, peut guider temporairement une réaction puis s’effacer discrètement — permettant de transformer des ingrédients simples et facilement disponibles en blocs de construction précieux pour la pharmacie sans recourir à des métaux coûteux ni à des étapes de préparation élaborées.
Transformer un assistant discret en guide temporaire
De nombreux médicaments modernes et matériaux fonctionnels reposent sur des réactions d’acides boroniques, une famille de composés contenant du bore appréciée pour sa fiabilité et sa douceur. Classiquement, pour amener les acides boroniques à former de nouvelles liaisons avec des liaisons double carbone‑azote (C=N), les chimistes doivent préinstaller des « groupes directeurs » spéciaux sur les réactifs. Ces groupes servent de poignées pour orienter la réaction, mais coûtent du temps, de l’argent et des étapes supplémentaires — et fonctionnent souvent seulement avec des partenaires très réactifs. Les auteurs ont remarqué que les lactames, homologues cycliques de l’amide familière des protéines, pouvaient jouer le rôle de guides temporaires intégrés. En coordonnant l’atome de bore, l’oxygène du lactame contribue à former un centre boroné fortement organisé à quatre liaisons qui peut transférer un fragment attaché vers une position distante le long de la molécule, permettant la formation de nouvelles liaisons carbone‑azote sans groupe directeur permanent.
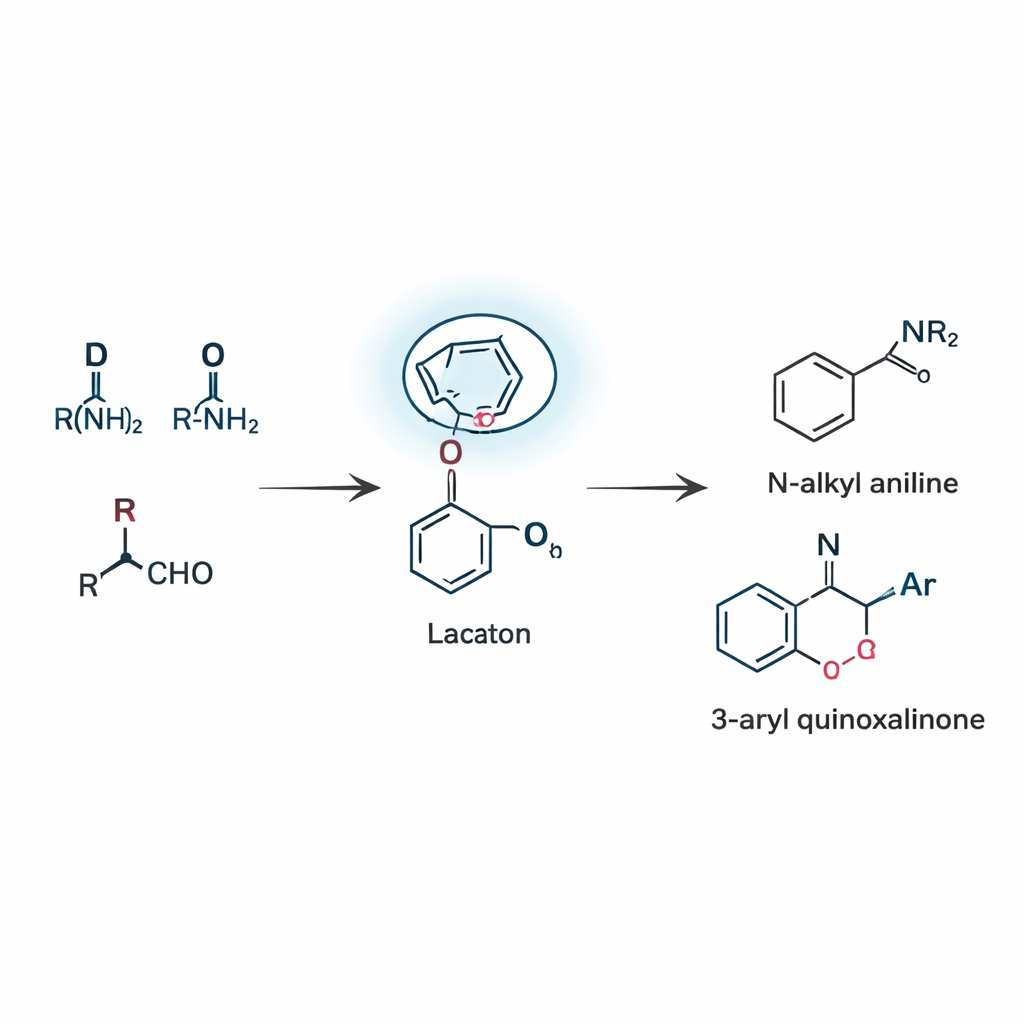
Construire deux familles de produits utiles en une stratégie
En exploitant ce concept, l’équipe a développé deux réactions apparentées reposant toutes deux sur ce réarrangement dirigé par le lactame, appelé réarrangement boronate à distance. Dans la première, trois éléments simples — un aldéhyde, une amine et un acide boronique — se combinent pour former des N‑alkyl anilines, un motif central que l’on retrouve dans d’innombrables candidats‑médicaments et colorants. La réaction se déroule via un rare déplacement 1,5, dans lequel un groupe aryle lié au bore saute par dessus cinq atomes pour atteindre la liaison C=N. En ajustant soigneusement le catalyseur, le solvant et la température, les chercheurs ont obtenu des rendements respectables et ont montré que de nombreux substituants différents, y compris des halogènes, des groupes alkyles et des hétérocycles, sont tolérés. Dans le second mode réactionnel, la même idée directrice est appliquée aux quinoxalinones, une classe d’anneaux riches en azote courante en chimie médicinale. Ici, la réaction n’utilise aucun catalyseur métallique ajouté et produit néanmoins efficacement des 3‑aryl quinoxalinones, grâce à la capacité du lactame à engager le bore et à stabiliser l’intermédiaire clé.
Conditions vertes et modification en fin de chaîne des médicaments
Au‑delà de la démonstration d’un large champ d’application, les auteurs montrent que cette stratégie est pratique pour des molécules réelles. Parce que le réarrangement 1,4 sur les quinoxalinones se déroule en l’absence de métal dans un solvant alcoolique spécialisé, il évite le recours à des métaux de transition coûteux ou toxiques. L’équipe a appliqué la méthode à des fragments complexes dérivés de médicaments commercialisés tels que l’ibuprofène et d’autres thérapeutiques contenant le squelette quinoxalinone. Dans chaque cas, la réaction a introduit de nouveaux groupes aryles à une position spécifique sans perturber d’autres caractéristiques sensibles. Ce type de « fonctionnalisation en fin d’étape » permet aux chimistes d’orner rapidement des cœurs médicamenteux existants de nouvelles chaînes latérales, accélérant la recherche d’améliorations en puissance, sécurité ou propriétés physiques.
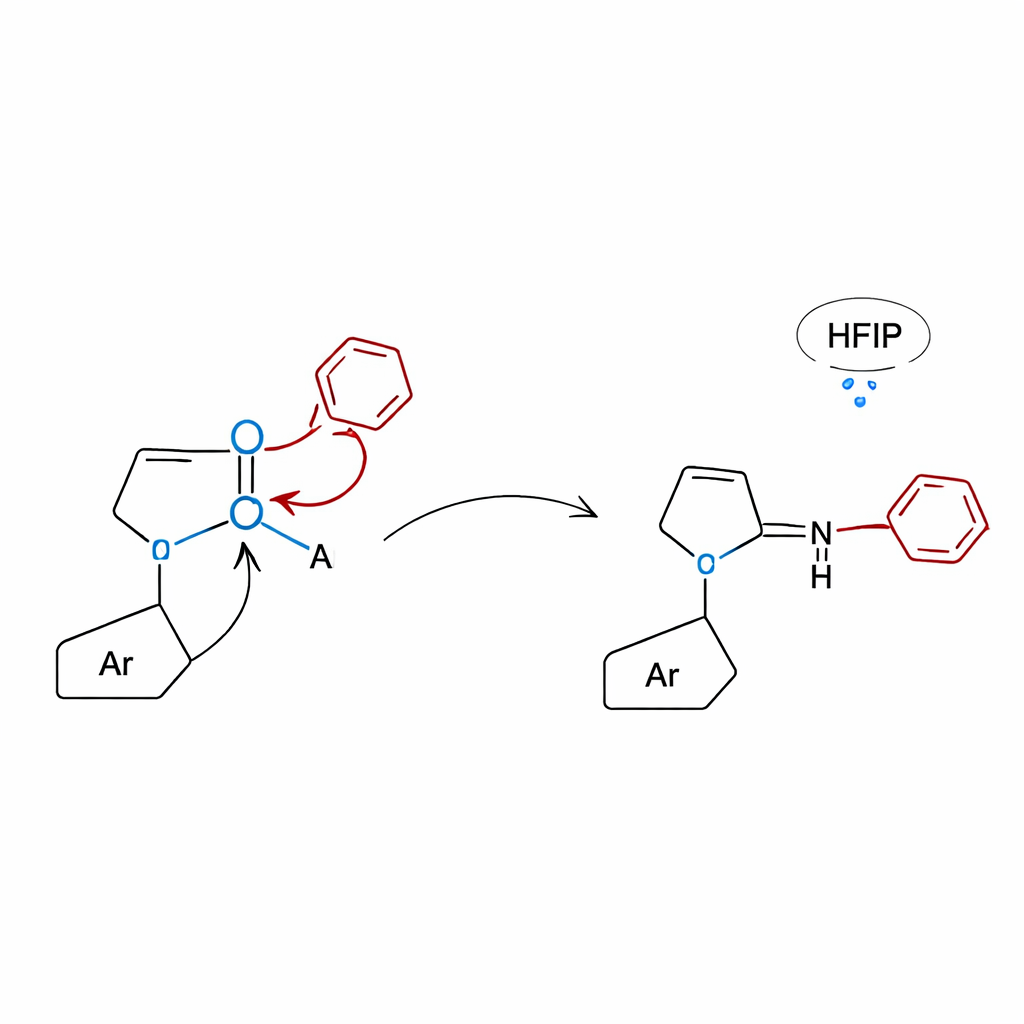
Regarder sous le capot avec la théorie et des tests de contrôle
Pour comprendre pourquoi l’approche par le lactame fonctionne si bien, les chercheurs ont combiné des expériences de contrôle soigneusement conçues avec des simulations informatiques. Lorsque des molécules dépourvues du motif lactame ont été testées, les réactions se sont pratiquement arrêtées, confirmant que l’anneau lactame est essentiel pour activer l’acide boronique et orienter le réarrangement. Des calculs de chimie quantique ont révélé que l’oxygène du lactame se lie au bore pour former une structure compacte à quatre liaisons à partir de laquelle le groupe aryle peut migrer soit sur cinq atomes (déplacement 1,5) pour donner des N‑alkyl anilines, soit sur quatre atomes (déplacement 1,4) pour donner des 3‑aryl quinoxalinones. Dans le cas des quinoxalinones, le réseau de liaisons hydrogène fourni par le solvant HFIP abaisse en outre la barrière énergétique, aidant la réaction à se dérouler sous des conditions thermiques relativement douces sans catalyseur ajouté.
Pourquoi cela importe pour les médicaments de demain
Dans l’ensemble, ce travail montre qu’un simple anneau lactame peut agir comme un guide dynamique et recyclable qui débloque des schémas de formation de liaisons jusqu’ici inaccessibles en chimie des acides boroniques. Pour le non‑spécialiste, le message clé est que les chimistes disposent désormais d’un moyen plus direct et efficace pour transformer des blocs de construction basiques en deux classes importantes de molécules azotées qui sous-tendent de nombreux médicaments. Parce que la méthode évite les métaux précieux, tolère une large gamme de groupes fonctionnels et fonctionne sur des structures avancées de type médicament, elle est bien placée pour aider à rationaliser la conception et l’optimisation des futurs produits pharmaceutiques et, potentiellement, de nouveaux produits agrochimiques également.
Citation: Lei, J., Xu, J., Li, X. et al. Lactam enables remote boronate rearrangements to C═N bonds. Commun Chem 9, 88 (2026). https://doi.org/10.1038/s42004-026-01890-2
Mots-clés: acides boroniques, chimie des lactames, formation de liaisons C–N, quinoxalinones, chimie médicinale