Clear Sky Science · fr
Découverte d'enzymes par inférence d’orthologues pour diversifier le squelette anti‑cancer de l’évodiamine
Transformer les molécules végétales en meilleurs médicaments
Beaucoup des médicaments actuels trouvent leur origine dans des molécules de défense produites par les plantes. Ces composés naturels montrent souvent des effets puissants contre le cancer, les infections ou la douleur, mais ils sont rarement des « médicaments parfaits ». Les chimistes aimeraient pouvoir modifier leurs structures de façon précise pour les rendre plus sûrs et plus efficaces, or ces molécules sont souvent si complexes que même de petits changements sont difficiles. Cette étude montre comment les chercheurs peuvent employer des enzymes végétales comme de minuscules outils moléculaires pour réaliser des modifications ciblées sur un composé anticancéreux appelé évodiamine, ouvrant potentiellement de nouvelles voies vers des thérapies améliorées.
Pourquoi cette molécule végétale compte
L’évodiamine est un composé naturel présent dans les fruits d’un arbre utilisé en médecine traditionnelle chinoise. Elle appartient à une famille de molécules cycliques qui forment déjà la base de médicaments importants contre le cancer, l’hypertension et les infections. L’évodiamine elle‑même a montré des propriétés anticancéreuses, anti‑inflammatoires, analgésiques et antimicrobiennes, et certaines de ses versions modifiées semblent particulièrement prometteuses comme candidats anticancéreux multi‑cibles. Le défi consiste à accrocher de nouvelles « poignées » chimiques, comme des groupes contenant de l’oxygène, à des positions très spécifiques sur ce squelette encombré, sans recourir à des réactifs agressifs ni à des synthèses en plusieurs étapes.
Laisser les enzymes faire la chimie difficile
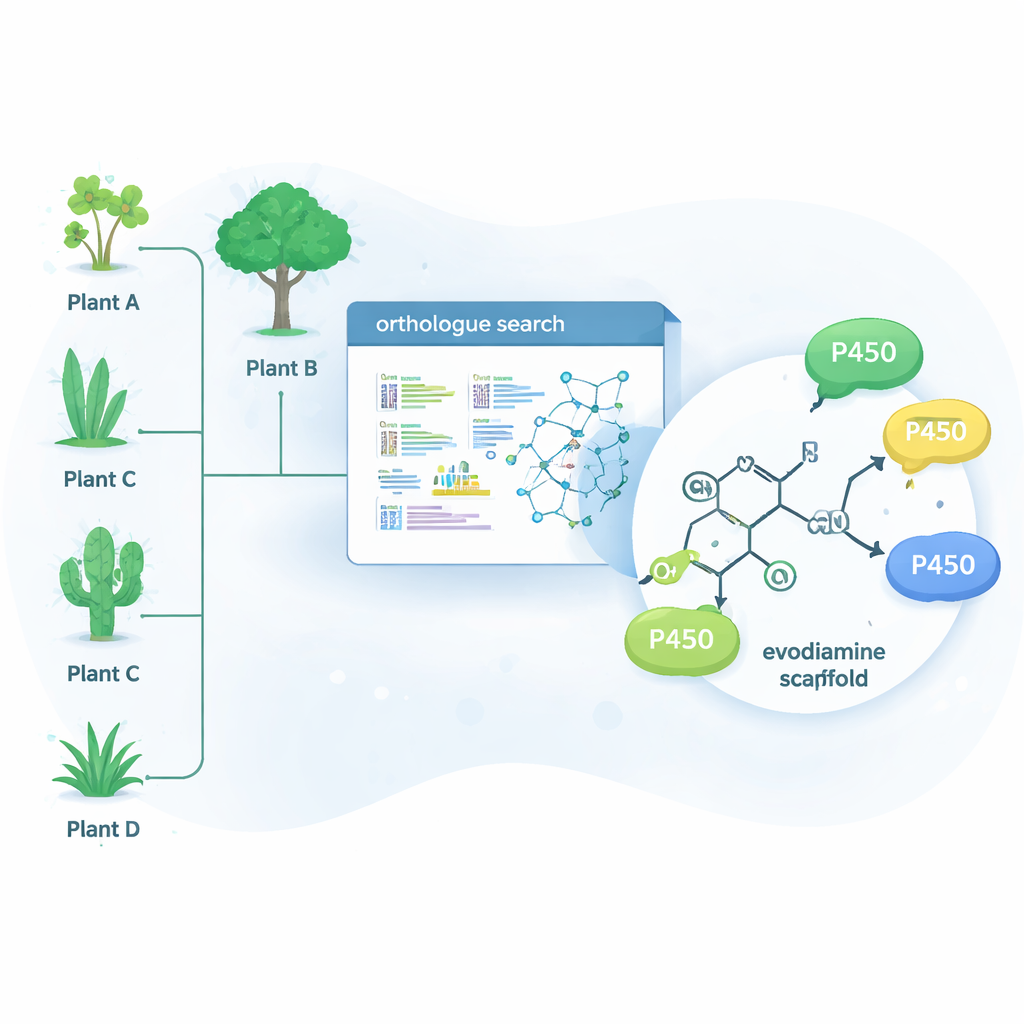
La nature a déjà résolu beaucoup de ces problèmes difficiles grâce aux enzymes — des protéines qui catalysent des réactions spécifiques. Une grande famille d’enzymes, les cytochromes P450, excelle à introduire de l’oxygène sur des liaisons carbone–hydrogène autrement peu réactives. Cette étape unique peut modifier profondément le comportement d’une molécule in vivo et constitue aussi un point de départ pour d’autres transformations chimiques. Plutôt que de chercher uniquement dans les plantes qui produisent naturellement l’évodiamine, les auteurs ont utilisé un outil bioinformatique appelé OrthoFinder pour scanner les données génétiques de 15 plantes productrices d’alcaloïdes. Ils ont recherché des P450 proches, des « orthologues », d’enzymes connues pour modifier des alcaloïdes, en raisonnant que des parents de ces enzymes pourraient également pouvoir ajuster des molécules apparentées de type médicament.
Découvrir de nouvelles enzymes dans des plantes inattendues
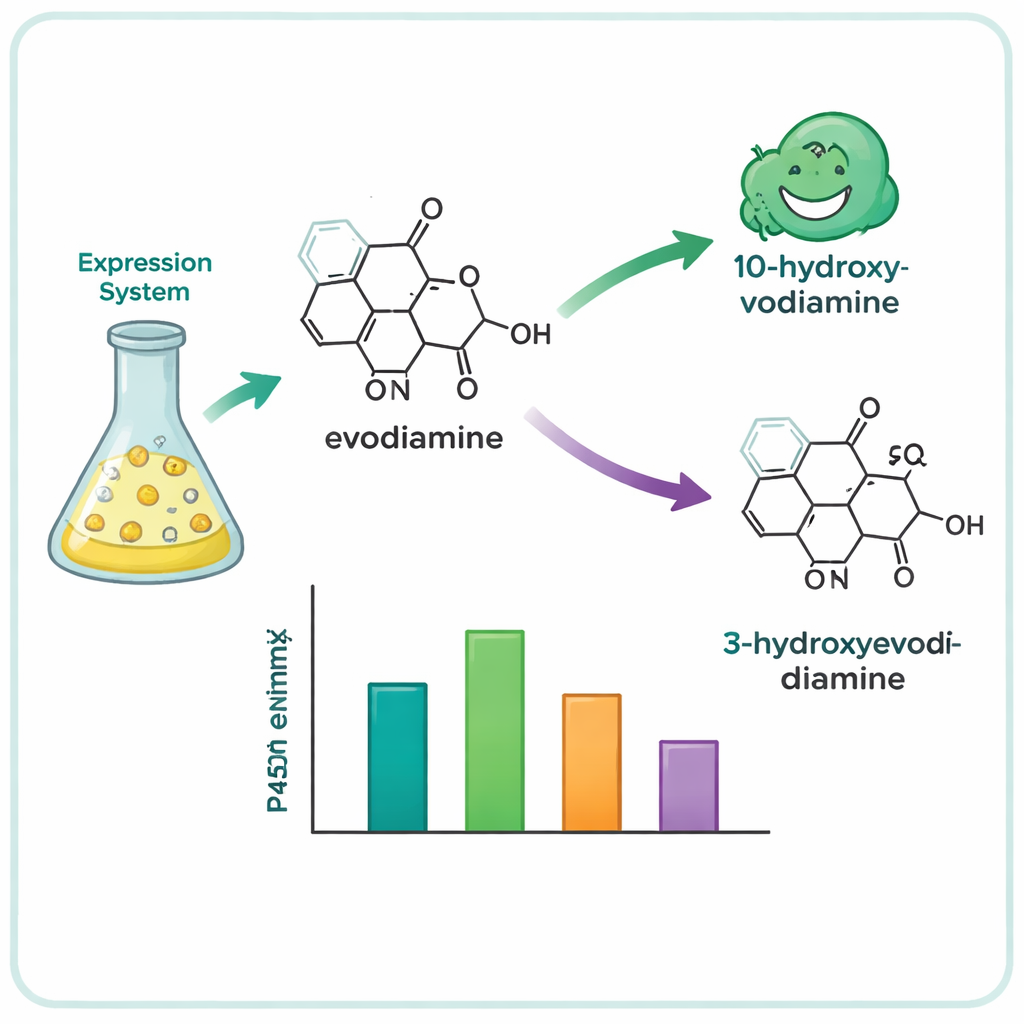
À partir de centaines de gènes candidats, l’équipe a réduit la liste à 15 P450 prometteurs et les a exprimés dans des cellules de levure, qui ont servi de petites usines enzymatiques. Ils ont ensuite nourri ces levures avec une collection de molécules végétales complexes et analysé lesquelles étaient chimiquement modifiées. Quatre enzymes — trois issues de l’arbre Camptotheca acuminata et une de l’arbuste Tabernaemontana elegans — se sont révélées actives sur l’évodiamine, bien qu’aucune de ces plantes ne soit connue pour la produire. Ces enzymes ont inséré sélectivement un atome d’oxygène à l’une de deux positions du système de cycles de l’évodiamine, générant deux produits principaux : la 10‑hydroxévodiamine et la 3‑hydroxévodiamine. Ces versions oxygénées sont plus faciles à transformer ensuite en candidats médicamenteux hydrosolubles ou plus puissants, en utilisant une chimie plus douce que les voies synthétiques traditionnelles.
Un coup d’œil à l’intérieur de la boîte à outils moléculaire
Pour comprendre pourquoi ces enzymes proches se comportaient différemment, les chercheurs ont construit des modèles tridimensionnels de l’enzyme la plus active et de ses parentes en utilisant des outils modernes de prédiction de structures protéiques. Ils ont ensuite effectué des simulations de « docking » pour voir comment l’évodiamine pouvait se placer dans la poche active de ces enzymes, près du centre contenant du fer du P450 où la réaction a lieu. Les modèles ont mis en évidence plusieurs acides aminés volumineux et hydrophobes — en particulier des phénylalanines — positionnés près des cycles aromatiques de l’évodiamine. En mutant soigneusement ces positions, l’équipe a montré que modifier la taille et la forme de cette poche pouvait affaiblir l’activité, altérer l’adéquation du substrat, ou même inverser le site d’oxygénation privilégié d’un cycle de la molécule à un autre. Dans un cas, une seule mutation a fait basculer la préférence de l’enzyme de la production de l’hydroxy‑10 vers la production de l’hydroxy‑3.
Ce que cela signifie pour les médicaments de demain
Pour les non‑spécialistes, la conclusion principale est que les auteurs ont démontré une feuille de route pratique pour découvrir et affiner des enzymes végétales capables d’effectuer des modifications précises, « chirurgicales », sur des molécules complexes de type médicament. En combinant un criblage génétique à grande échelle avec des tests enzymatiques et de la modélisation structurale, ils ont identifié un ensemble de biocatalyseurs capables de remanier sélectivement le squelette de l’évodiamine à des positions difficiles d’accès par la chimie standard. Cela offre non seulement une manière plus propre et plus durable de produire des versions avancées de l’évodiamine — comme des candidats anticancéreux hydrosolubles — mais montre aussi que des enzymes utiles peuvent être trouvées chez des plantes qui ne fabriquent pas elles‑mêmes le composé ciblé. La même stratégie pourrait désormais être appliquée à de nombreux autres produits naturels, accélérant la conception de médicaments dérivés des plantes de nouvelle génération.
Citation: Kwan, B.D., Kim, T., Nguyen, H.H. et al. Orthologue inference-based enzyme mining for diversification of the anti-cancer evodiamine scaffold. Commun Chem 9, 73 (2026). https://doi.org/10.1038/s42004-025-01876-6
Mots-clés: évodiamine, enzymes végétales, cytochrome P450, biocatalyse, découverte de médicaments