Clear Sky Science · fr
La mutation du syndrome PACS1 perturbe le transport de cargaison médié par la dynéine via HDAC6 et BICD2
Pourquoi c’est important pour le développement cérébral
Le syndrome PACS1 est une maladie génétique rare provoquant un retard intellectuel, des crises épileptiques et des traits faciaux caractéristiques. Les familles et les cliniciens connaissent les symptômes, mais jusqu’à récemment on ignorait ce qui dysfonctionnait exactement à l’intérieur des cellules des patients. Cette étude lève le voile sur ce mystère en montrant comment un changement d’une seule lettre dans le gène PACS1 bouleverse le système de transport interne de la cellule, en particulier dans les neurones, et comment cela relie le syndrome PACS1 à une famille plus large de maladies du « trafic » du système nerveux. 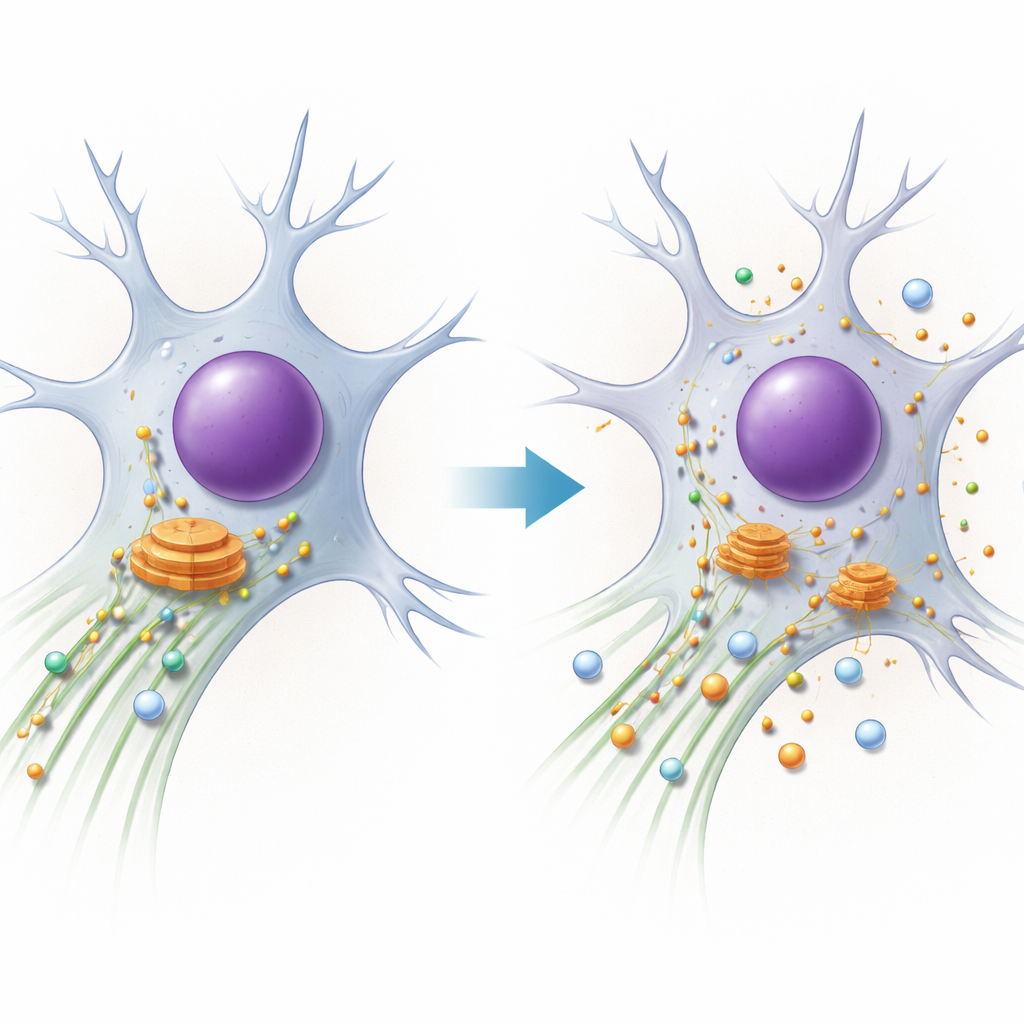
Les voies de livraison de la cellule
Chaque cellule dépend de voies microscopiques constituées de tubes protéiques appelés microtubules. Des moteurs moléculaires circulent le long de ces rails en transportant des cargaisons — enzymes, compartiments membranaires — vers les endroits où elles sont nécessaires. Un moteur, la dynéine, assure les « retours » longue distance en tirant les cargaisons de la périphérie vers le centre de la cellule, où se trouve un important centre de tri, l’appareil de Golgi. Les auteurs se concentrent sur PACS1, une protéine qui aide à sélectionner quelles cargaisons empruntent la dynéine et qui module aussi l’état des rails via une autre protéine, HDAC6, qui contrôle un marquage chimique (acétylation) des microtubules. Les neurones, avec leurs prolongements très longs, sont particulièrement sensibles aux petites défaillances de ce système.
Un coordinateur mutant qui s’accroche trop
Le syndrome PACS1 est causé par la mutation récurrente R203W dans PACS1. L’équipe a découvert que PACS1, normal et mutant, se lie physiquement à la chaîne lourde de la dynéine, mais que la forme mutante s’attache plus fortement. En utilisant des cellules de peau de patients et des lignées cellulaires modifiées, ils ont montré que cette sur‑engagement produit le même effet que la perte partielle de la fonction de la dynéine : le Golgi se fragmente en mini‑empilements dispersés, et une enzyme importante, la furine, normalement localisée du côté trans du Golgi, est redirigée vers d’autres compartiments. En disséquant la structure de PACS1, ils ont identifié un court « patch » en feuillet bêta qui contacte spécifiquement la dynéine. Lorsqu’ils ont modifié ce patch sans perturber les autres fonctions de PACS1, la furine a de nouveau perdu sa localisation correcte, confirmant que la poignée dynéine–PACS1 est cruciale pour le placement approprié des cargaisons. 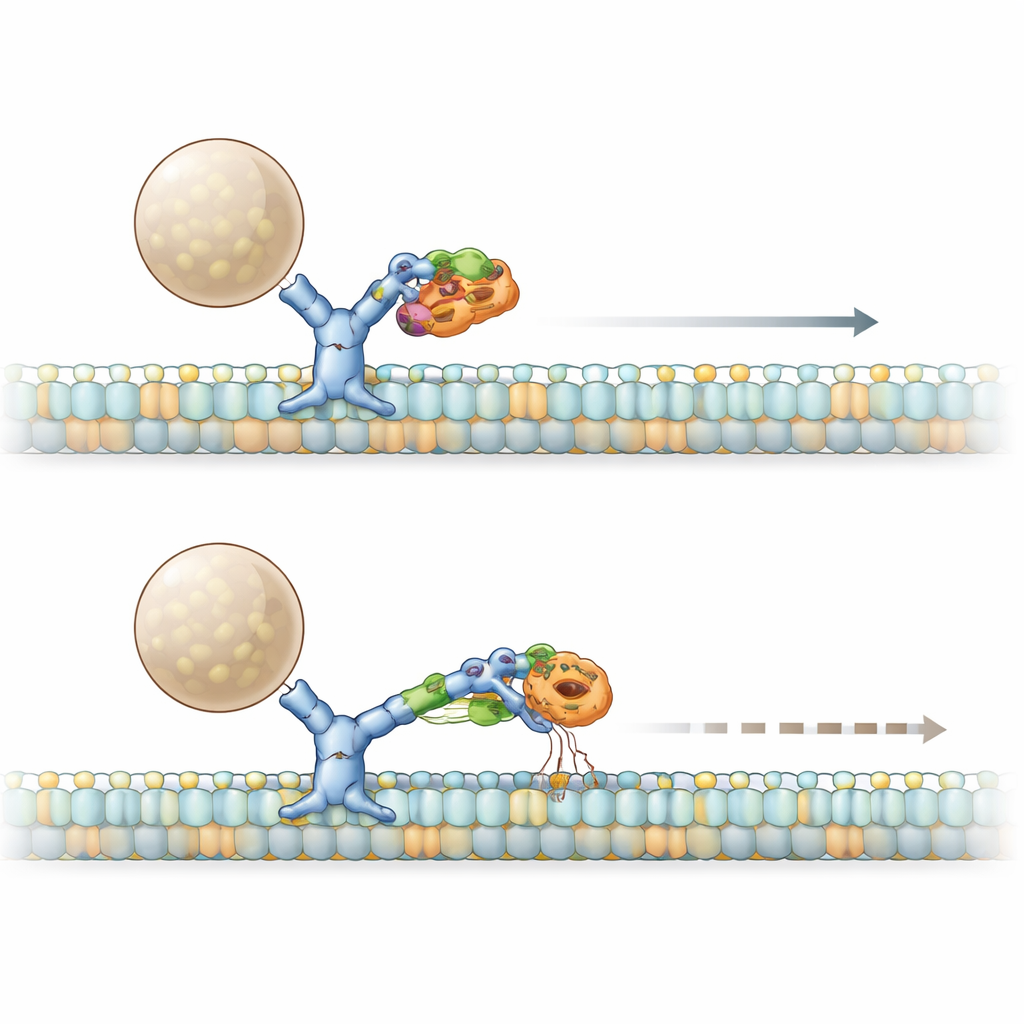
Comment une alliance de trois protéines bloque le moteur
L’histoire s’épaissit avec deux acteurs supplémentaires : HDAC6 et un adaptateur nommé BICD2, qui aide à assembler les complexes dynéine actifs. La PACS1 mutante augmente non seulement l’activité de HDAC6, réduisant l’acétylation des microtubules, mais forme aussi un complexe agrandi avec HDAC6 et BICD2. Des tests biochimiques ont révélé qu’ensemble, la PACS1 mutante et HDAC6 arrachent BICD2 à la dynéine tout en laissant intacte son association avec un moteur orienté vers l’avant (kinesine). Dans des cellules vivantes, une cargaison artificielle qui se déplaçait normalement rapidement grâce à la dynéine ralentissait, et moins de cargaisons se mouvaient du tout en présence de PACS1 mutante. Bloquer l’activité de HDAC6 a restauré à la fois la vitesse et le nombre de particules en mouvement, montrant que l’assemblage mutant PACS1–HDAC6–BICD2 agit comme un frein sur la capacité de la dynéine à initier et maintenir le transport.
Rétablir le trafic avec un assistant naturel de la dynéine
Les chercheurs ont ensuite testé si la dynéine pouvait être « réactivée » malgré le complexe mutant. Ils se sont tournés vers Lis1, un cofacteur connu de la dynéine qui stabilise les assemblages moteurs actifs. Dans les cellules de patients, les niveaux de Lis1 étaient légèrement réduits. Lorsque l’équipe a ajouté du Lis1 en excès, deux éléments se sont améliorés : le Golgi s’est re‑rassemblé près du centre cellulaire, et les lysosomes, une autre classe d’organites qui s’étaient déplacés vers l’extérieur, sont revenus en place. Dans le même essai de motilité, Lis1 a augmenté à la fois la fréquence et la vitesse des mouvements des cargaisons entraînées par la dynéine en présence de PACS1 mutante. Ces résultats montrent que le problème n’est pas l’absence de dynéine, mais son enlisement dans un état faiblement actif — un état qui peut être partiellement corrigé soit en atténuant HDAC6, soit en renforçant l’activation de la dynéine.
Relier un syndrome rare à un ensemble plus large de troubles
En combinant analyse structurale, biologie cellulaire et imagerie en direct, les auteurs proposent un modèle clair : PACS1 relie normalement des cargaisons sélectionnées à la dynéine et ajuste la performance du moteur via HDAC6 et l’acétylation des microtubules. La mutation R203W expose une surface d’interaction de PACS1, recrutant excessivement HDAC6 et BICD2 dans un complexe qui compromet la capacité de la dynéine à s’accrocher aux microtubules et à se déplacer efficacement. Le résultat est un mauvais positionnement généralisé du Golgi, des lysosomes et d’autres cargaisons, en particulier dans les neurones où le transport sur longue distance est vital. Ce mécanisme aide à expliquer pourquoi diminuer PACS1 ou HDAC6 par des thérapies antisens corrige les défauts cérébraux dans des modèles murins et est désormais exploré chez les patients. Plus largement, il place le syndrome PACS1 dans le spectre croissant des troubles du trafic sur microtubules, aux côtés de pathologies causées par des mutations de la dynéine, de BICD2 et d’autres facteurs de transport.
Citation: Yang, Y., Thomas, L., Chen, K. et al. PACS1 syndrome mutation disrupts dynein-mediated cargo transport via HDAC6 and BICD2. Commun Biol 9, 450 (2026). https://doi.org/10.1038/s42003-026-09924-0
Mots-clés: sindrome PACS1, transport par dynéine, trafic sur microtubules, organisation du Golgi, développement neuronal