Clear Sky Science · fr
La protéine sécrétée CLCF1 améliore la maladie hépatique cholestatique en inhibant la synthèse hépatique des acides biliaires et en favorisant leur excrétion
Pourquoi cette recherche est importante pour la santé du foie
Les maladies hépatiques cholestatiques sont des affections dans lesquelles la bile, un liquide digestif produit par le foie, ne s’écoule plus correctement et s’accumule, intoxiquant progressivement le foie de l’intérieur. Les traitements actuels ne bénéficient qu’à une fraction des patients, et beaucoup finissent par nécessiter une transplantation hépatique. Cette étude met au jour une protéine produite naturellement, nommée CLCF1, que l’organisme semble activer comme un mécanisme de défense lors de la cholestase. Comprendre le fonctionnement de cette protéine pourrait ouvrir la voie à de nouveaux traitements protégeant le foie en réduisant à la fois la production de composants biliaires nocifs et en aidant l’organisme à les éliminer plus efficacement.
Un assistant caché dans les foies malades
Les chercheurs ont commencé par examiner des tissus hépatiques de patients atteints de cholangite biliaire primitive et de cholangite sclérosante primitive, deux formes majeures et chroniques de cholestase. Ils ont comparé des personnes au stade précoce de la maladie à celles présentant une cholestase plus avancée, et ont aussi analysé des jeux de données génétiques publics existants. À travers ces sources humaines indépendantes, une protéine sécrétée s’est distinguée : CLCF1 figurait systématiquement parmi les gènes les plus fortement augmentés dans les foies cholestatiques. Des niveaux plus élevés de CLCF1 corrélaient avec des marqueurs sanguins plus mauvais de la gravité de la maladie, ce qui suggère que le foie augmente la production de cette protéine à mesure que le stress et l’accumulation de bile s’aggravent. Chez des patients en phase précoce traités par l’acide ursodésoxycholique, ceux qui répondaient bien au traitement avaient tendance à présenter davantage de CLCF1 dans leur foie, laissant penser que cette protéine pourrait marquer un foie plus adaptable et sensible au traitement.
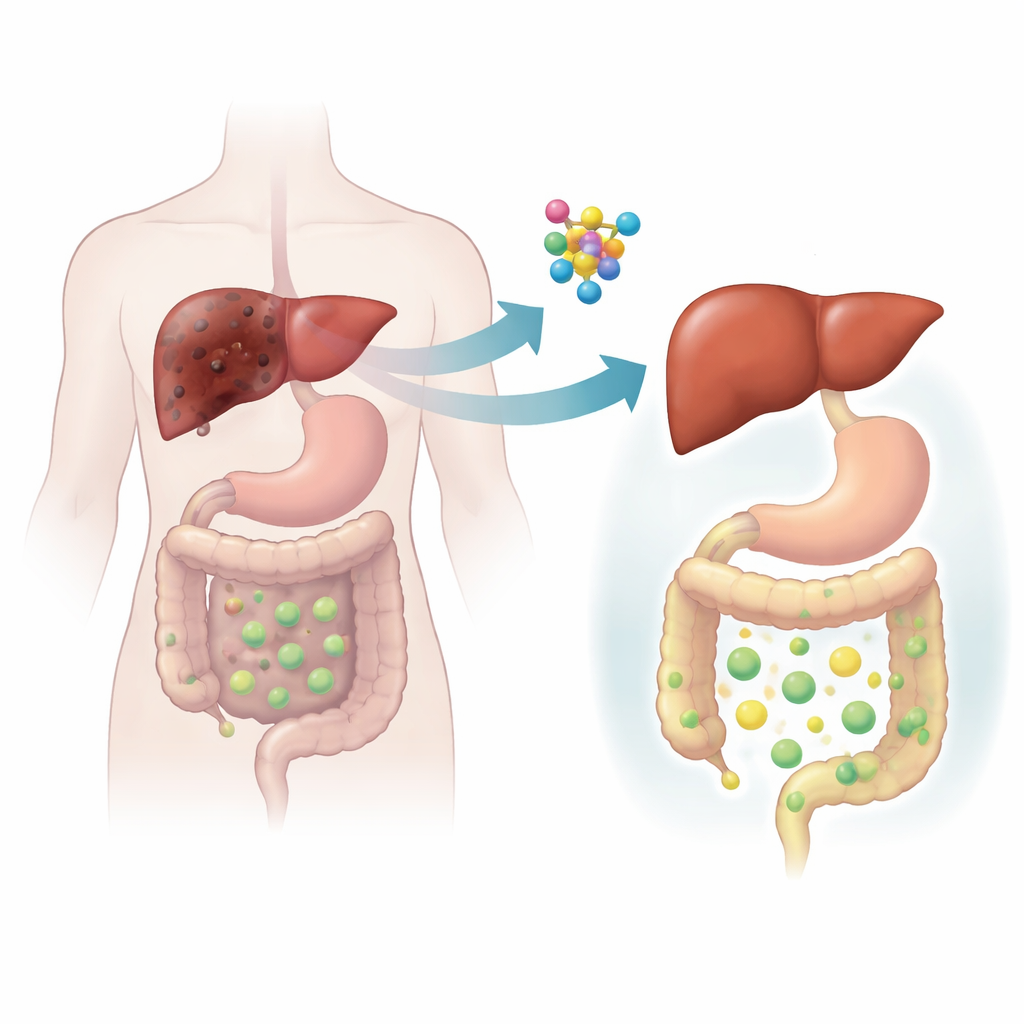
Tester CLCF1 dans des modèles animaux
Pour aller au-delà des corrélations humaines, l’équipe a utilisé des souris et a eu recours à des manipulations génétiques et alimentaires pour reproduire la maladie hépatique cholestatique. Dans deux modèles murins différents, la cholestase augmentait fortement la production hépatique de Clcf1, reflétant les observations humaines. Lorsque les scientifiques ont supprimé de façon ciblée le récepteur de CLCF1 dans les cellules hépatiques, les lésions cholestatiques se sont considérablement aggravées : prolifération des canaux biliaires, nécrose du tissu hépatique, inflammation accrue, accumulation de tissu cicatriciel et accumulation d’acides biliaires toxiques. L’expérience inverse est plus encourageante. Lorsque l’équipe a utilisé un virus inoffensif pour augmenter les niveaux de Clcf1 uniquement dans le foie, les souris ont été protégées : leur foie paraissait en meilleure santé, les analyses sanguines se sont améliorées, la fibrose a été réduite et la quantité d’acides biliaires piégés dans le foie a chuté nettement.
Réduire le robinet et ouvrir l’évacuation
Comment CLCF1 réduit-il si efficacement la surcharge en acides biliaires ? Les chercheurs ont identifié deux actions complémentaires. D’abord, CLCF1 a calmé directement la machinerie hépatique de synthèse de la bile. Dans plusieurs modèles murins et dans des cellules hépatiques en culture, un excès de CLCF1 a systématiquement arrêté des enzymes clés qui convertissent le cholestérol en acides biliaires, réduisant ainsi la production de nouvelle bile. Cela s’est produit sans activer le régulateur nucléaire habituel du foie pour le contrôle des bileux, le récepteur FXR, ce qui suggère que CLCF1 utilise une voie alternative à l’intérieur des cellules hépatiques pour freiner la synthèse biliaire. Ensuite, CLCF1 a influencé la manière dont la bile est traitée en aval dans l’organisme. Il a modifié la communauté microbienne intestinale en faveur de bactéries particulièrement efficaces pour métaboliser les acides biliaires et a augmenté la quantité d’acides biliaires éliminés dans les selles, agissant comme une évacuation renforcée.
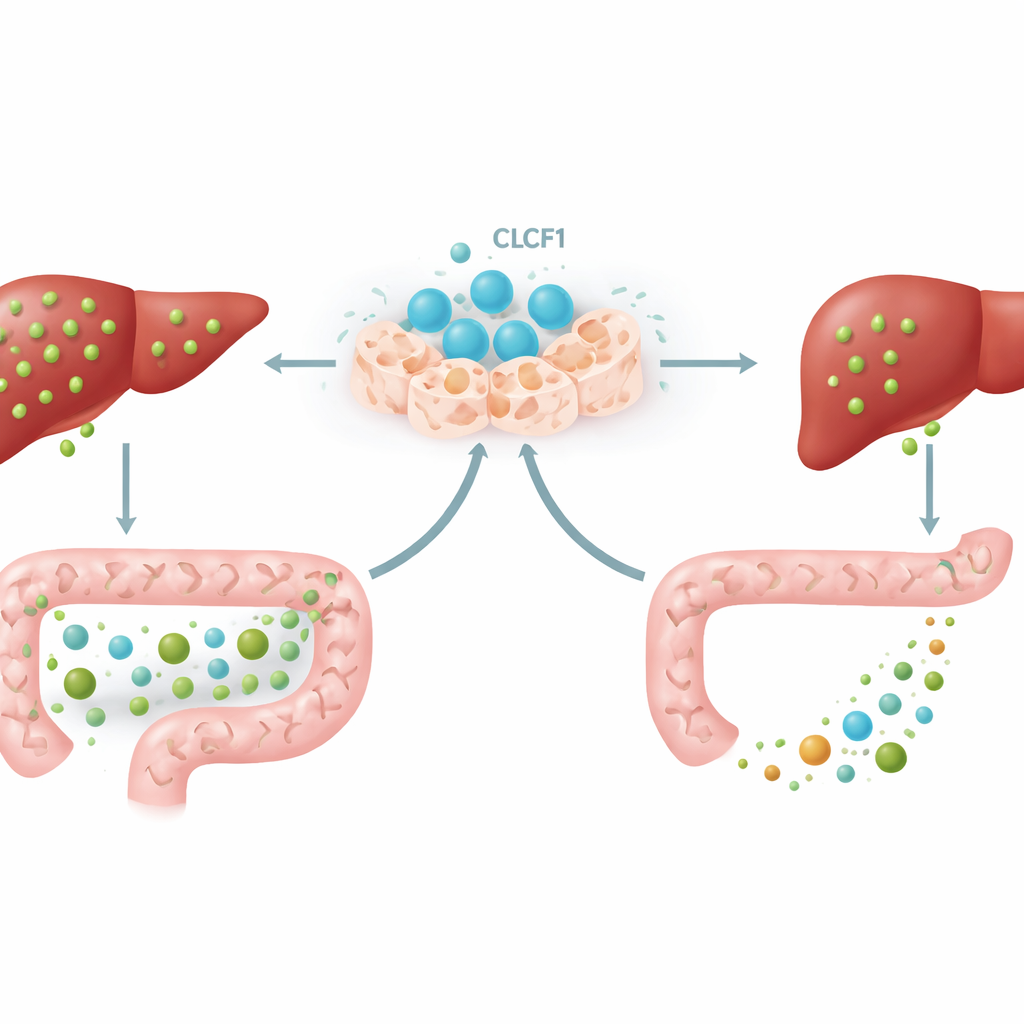
La conversation intestin–foie
Un élément clé du mécanisme impliquait une boucle de signalisation entre l’intestin et le foie. Certains acides biliaires présents dans l’intestin activent un capteur appelé FXR dans les cellules intestinales, qui libèrent alors une hormone messagère connue sous le nom de FGF15 chez la souris. Cette hormone voyage par le sang jusqu’au foie et indique à celui-ci de ralentir la production d’acides biliaires. Avec un excès de CLCF1, les souris accumulaient dans leurs intestins des types d’acides biliaires spécifiques — en particulier des formes connues pour être de puissants activateurs de FXR. En conséquence, l’activation intestinale de FXR a augmenté, les niveaux de FGF15 ont augmenté à la fois dans l’intestin et dans le foie, et le foie a encore davantage réduit sa production d’acides biliaires. Lorsque les scientifiques ont bloqué FXR intestinal avec un médicament limité à l’intestin, une grande partie de l’effet protecteur de CLCF1 a disparu, démontrant que cette conversation intestin–foie est une composante essentielle de l’action de la protéine.
Ce que cela pourrait signifier pour les traitements futurs
Ensemble, ces résultats décrivent CLCF1 comme une soupape de sécurité intrinsèque pour la maladie hépatique cholestatique. La protéine réduit les niveaux d’acides biliaires des deux côtés : elle ralentit leur création dans le foie et favorise leur élimination par l’intestin, aidée par des microbes intestinaux favorables et un signal hormonal de rétrocontrôle. Contrairement aux médicaments existants qui activent FXR dans tout l’organisme et peuvent provoquer des effets indésirables tels que démangeaisons et anomalies des lipides sanguins, CLCF1 semble orienter le contrôle des acides biliaires de façon plus douce et sélective, notamment via l’intestin. Bien que ces travaux restent limités aux souris et aux échantillons de laboratoire, ils suggèrent que renforcer CLCF1 ou imiter ses voies pourrait constituer la base de nouvelles thérapies — et que la mesure de cette protéine, ou des acides biliaires qu’elle enrichit dans l’intestin, pourrait aider à identifier les patients susceptibles d’en tirer le plus grand bénéfice.
Citation: Liu, M., Su, Y., Hu, Y. et al. The secretory protein, CLCF1, improves cholestatic liver disease by inhibiting hepatic bile acid synthesis and promoting bile acid excretion. Commun Biol 9, 370 (2026). https://doi.org/10.1038/s42003-026-09847-w
Mots-clés: maladie hépatique cholestatique, acides biliaires, axe intestin–foie, CLCF1, microbiote intestinal