Clear Sky Science · fr
Le système de sécrétion de type VI d’Acinetobacter : mécanismes, biologie et potentiel thérapeutique
Armes cachées des germes hospitaliers
Beaucoup savent que certains germes hospitaliers résistent aux antibiotiques, mais moins comprennent que ces microbes se livrent aussi à de violentes batailles entre eux. Cette revue examine une « lance à ressort » microscopique présente chez Acinetobacter, un groupe de bactéries qui inclut le redoutable germe hospitalier Acinetobacter baumannii. Comprendre comment fonctionne cette arme intégrée, quand elle est activée et comment elle facilite l’installation d’infections pourrait ouvrir de nouvelles voies pour diagnostiquer et neutraliser des infections résistantes et potentiellement mortelles.
Une machine de survie, pas seulement un dard toxique
Les espèces d’Acinetobacter vivent dans le sol, l’eau et sur notre peau, mais certaines sont devenues des pathogènes hospitaliers très efficaces. Un outil clé de leur arsenal est le système de sécrétion de type VI, ou T6SS, une minuscule machine contractile ancrée dans l’enveloppe cellulaire. Lorsqu’il est déclenché, il projette une pointe semblable à une aiguille chargée de protéines toxiques dans les cellules voisines, tuant souvent les bactéries concurrentes sur le coup. Contrairement à certains autres germes qui possèdent plusieurs variantes de ce système, les Acinetobacter pathogènes n’ont généralement qu’un seul T6SS, mais ils ont réaménagé cette plate‑forme unique pour servir à de multiples usages, de l’élimination des rivaux à la structuration des infections.
Matériel reconstruit : une plateforme de lancement inhabituelle
La plupart des bactéries construisent leur T6SS autour d’un ensemble standard de composants, mais Acinetobacter a remodelé plusieurs pièces clés. Il lui manque un ancrage de la membrane externe commun appelé TssJ et il compte à la place sur un trio d’aides spécialisées : TsmK forme une base dans la membrane interne, TslA stabilise une longue protéine « tunnel » (TssM) traversant la paroi cellulaire, et TagX coupe localement la paroi pour laisser passer l’arme. De plus, une protéine de pointe particulière, VgrG1, doit avoir une forme presque parfaite pour que le système puisse se déclencher : des changements d’un seul acide aminé peuvent le rendre non fonctionnel. Ensemble, ces ajustements montrent comment l’évolution peut remplacer des pièces manquantes par de nouvelles solutions tout en préservant le principe fondamental du tir.
Commandes intelligentes : quand le mode d’attaque a du sens
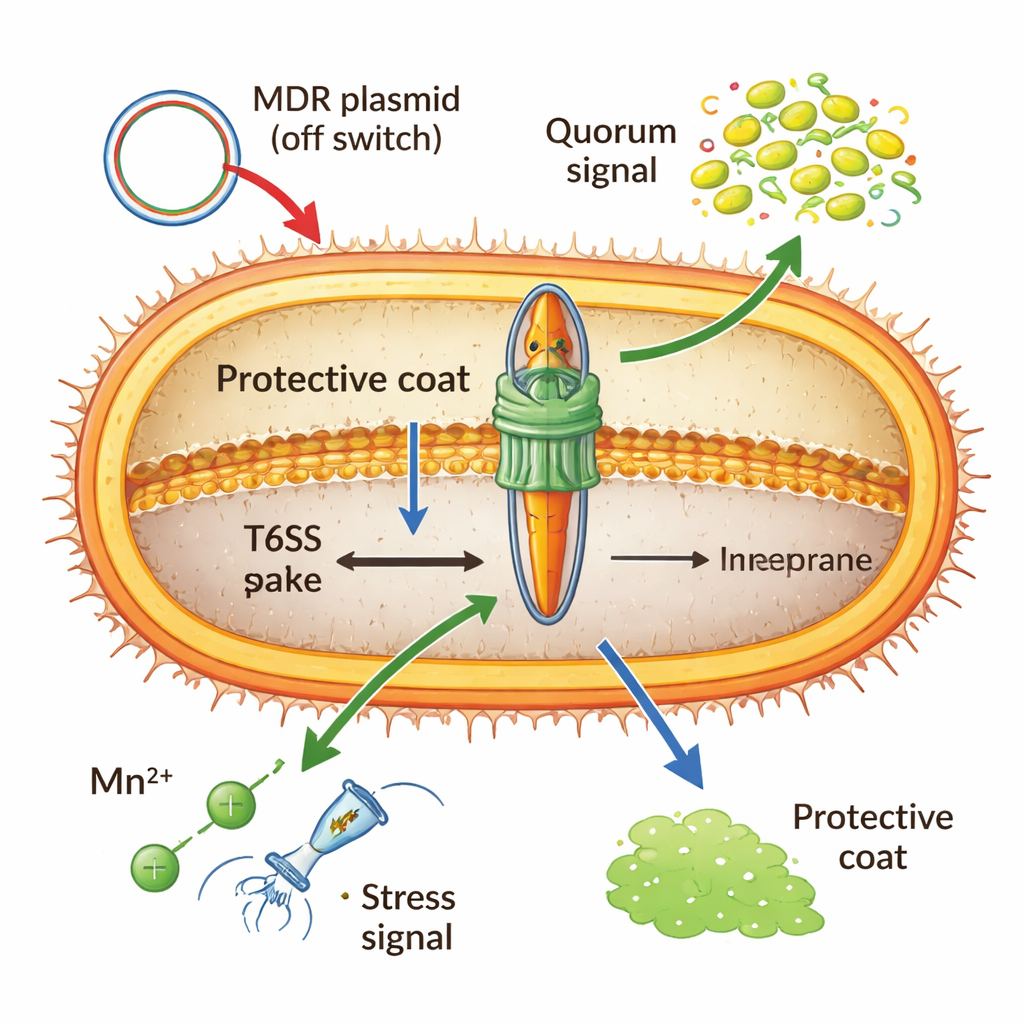
Construire et tirer cette nanomachine coûte cher, aussi Acinetobacter la maintient‑il sous contrôle strict. Une protéine globale de liaison à l’ADN (H‑NS) et des répresseurs spéciaux portés par des plasmides multirésistants peuvent verrouiller le système en position « off », notamment lorsque des gènes de résistance sont échangés entre cellules. À forte densité cellulaire, des signaux chimiques de « quorum » peuvent l’activer, préparant les bactéries à la compétition rapprochée. Les ions métalliques jouent aussi un rôle : en situation de stress oxydatif, le manganèse importé active un petit ARN qui provoque la destruction des messages clés du T6SS, réduisant l’armement pour favoriser la survie à l’intérieur de l’hôte. Même la capsule — un manteau extérieur sucré — agit à la fois comme bouclier et comme frein, bloquant les attaques entrantes mais atténuant aussi physiquement les tirs d’Acinetobacter.
Une trousse d’outils diverse de coups microscopiques
Lorsque Acinetobacter appuie sur la gâchette, il peut délivrer une large gamme de toxines. Certaines enzymes dégradent la paroi résistante des rivaux ; d’autres érodent discrètement les membranes cellulaires, et d’autres encore coupent l’ADN à l’intérieur des cellules cibles. Chaque toxine est associée à une protéine « d’immunité » correspondante qui protège l’attaquant des tirs amis. Une toxine coupeuse d’ADN, désormais appelée TafE, peut même tuer des champignons, suggérant des escarmouches inter‑règnes dans des lieux comme l’intestin ou les poumons. Des études génomiques indiquent qu’Acinetobacter code de nombreuses autres toxines encore non caractérisées, souvent empaquetées dans de grands protéines Rhs qui servent de transporteurs modulaires. Plutôt que de compter sur un seul coup, ces bactéries semblent utiliser des attaques en couches qui endommagent plusieurs structures essentielles à la fois.
Façonner les infections, les gènes et les traitements futurs
Les données provenant d’isolats de patients et de modèles animaux suggèrent qu’un T6SS actif s’accompagne souvent de maladies plus graves, d’une inflammation plus marquée et d’une meilleure survie des bactéries au sein des hôtes. En tuant les microbes voisins, le système libère aussi de l’ADN que les cellules d’Acinetobacter compétentes peuvent absorber, accélérant la diffusion de traits comme la résistance aux antibiotiques. Pourtant, maintenir l’arme constamment active coûte cher, si bien que de nombreuses souches hospitalières prospères portent des plasmides ou des mutations qui l’éteignent une fois la résistance assurée. Dans l’ensemble, les auteurs soutiennent que ce système de sécrétion doit être vu non pas comme un simple facteur de virulence mais comme un « module de fitness » flexible que Acinetobacter module pour équilibrer agressivité, persistance et dépense d’énergie. Cette nouvelle perspective ouvre des pistes pratiques, des vaccins ciblant des parties conservées du T6SS à des médicaments qui bloqueraient sélectivement le mécanisme de tir, aidant les médecins à déjouer un ennemi hospitalier dangereux et adaptable.
Citation: Jie, J., Gu, S., Li, D. et al. The type VI secretion system of Acinetobacter: mechanisms, biology and therapeutic potential. Commun Biol 9, 327 (2026). https://doi.org/10.1038/s42003-026-09782-w
Mots-clés: Acinetobacter, système de sécrétion de type VI, résistance aux antibiotiques, compétition bactérienne, infections nosocomiales