Clear Sky Science · fr
Implication de l’axe hypothalamus–raphe magnus–centre spinal de la défécation dans la défécation induite par le stress chez le rat
Pourquoi le stress peut dérégler votre estomac
La plupart des gens ont déjà ressenti un estomac noué, une urgence soudaine ou même de la diarrhée lors de situations stressantes comme des examens ou la prise de parole en public. Bien que cette connexion cerveau–intestin soit bien connue, les voies nerveuses précises qui transforment le stress psychologique en course vers les toilettes sont restées étonnamment floues. Cette étude chez le rat met au jour une chaîne spécifique de circuits cérébraux et spinaux reliant le stress émotionnel à de puissantes contractions du bas-intestin, ce qui aide à expliquer pourquoi le stress se manifeste si souvent dans les sanitaires.
Une voie cérébrale de l’inquiétude vers l’intestin
Les chercheurs se sont concentrés sur une région cérébrale appelée l’hypothalamus, un centre clé de contrôle à la fois des émotions et des fonctions automatiques de l’organisme. Des travaux antérieurs avaient montré que le stress active l’hypothalamus et le tronc cérébral, et que ces zones peuvent accélérer le transit colique. Cependant, on ne savait pas exactement comment les signaux voyageaient du cerveau jusqu’au côlon distal et au rectum, qui sont cruciaux pour la défécation. En utilisant des virus traceurs qui se déplacent le long des fibres nerveuses, l’équipe a cartographié des neurones reliant l’hypothalamus à une structure du tronc cérébral connue sous le nom de raphe magnus, puis depuis celle-ci le long de la moelle épinière vers le bassin.
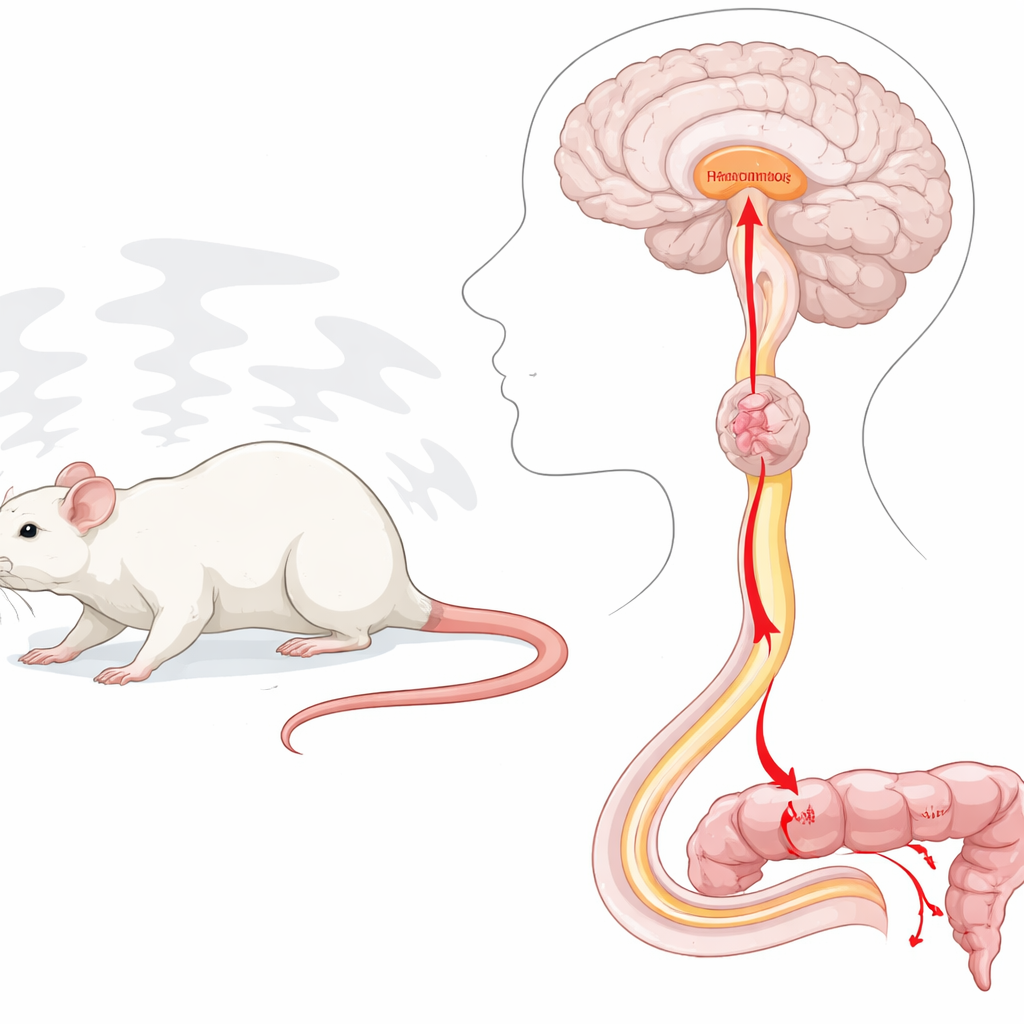
Le stress active une chaîne spécifique cerveau–moelle–côlon
Pour reproduire le stress psychologique, les rats ont été placés sur une petite plateforme entourée d’eau, un dispositif classique de « water avoidance » qui déclenche de façon fiable anxiété et augmentation des selles. Les scientifiques ont observé que, sous ce stress, les neurones hypothalamiques projetant vers le raphe magnus étaient fortement activés. Lorsqu’ils ont excité chimiquement les mêmes zones hypothalamiques—particulièrement les régions paraventriculaire et dorsomédiale—chez des rats anesthésiés, le bas côlon a présenté des contractions propulsives vigoureuses, et la pression artérielle et la fréquence cardiaque des animaux ont augmenté. Le blocage des hormones liées au stress appelées facteurs de libération de la corticotropine n’a pas empêché ces contractions intestinales, ce qui suggère qu’un autre système de signalisation était impliqué.
Du tronc cérébral à la moelle épinière puis au nerf pelvien
La question suivante était de savoir comment l’activation dans le cerveau atteignait les muscles de l’intestin. L’équipe a montré que le raphe magnus envoie de longues fibres descendantes qui libèrent le messager chimique sérotonine dans la moelle lombosacrée, où se trouve le centre de la défécation. Lorsque les chercheurs ont appliqué des médicaments directement sur la moelle pour bloquer deux types clés de récepteurs à la sérotonine, le côlon ne répondait plus à l’activation hypothalamique. De même, la section du nerf pelvien—qui véhicule les signaux parasympathiques de la moelle vers le rectum et le côlon distal—abolissait l’augmentation de la motilité. Ensemble, ces expériences révèlent une voie continue : hypothalamus vers raphe magnus, raphe vers le centre spinal de la défécation, et sortie spinale via le nerf pelvien vers l’intestin.
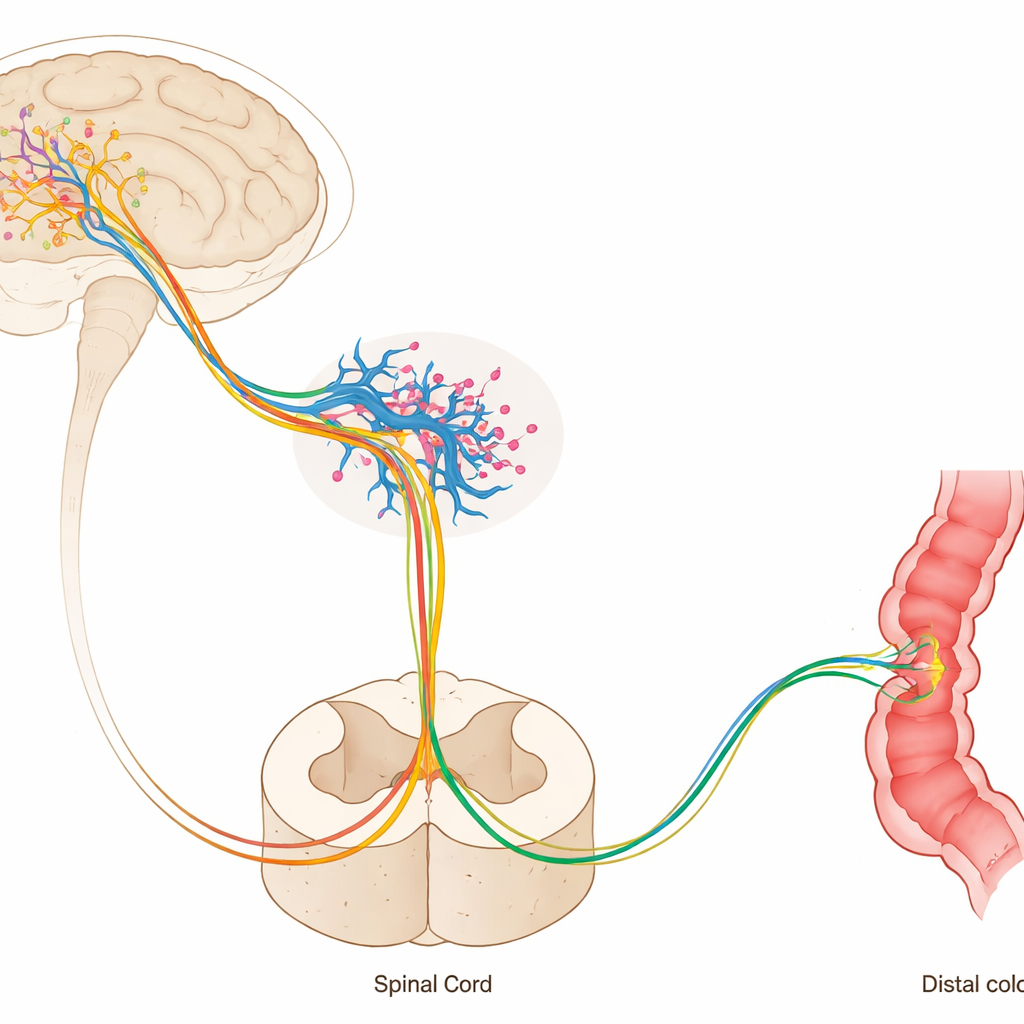
L’ocytocine donne les ordres aux neurones sérotoninergiques
Pour identifier ce qui active les neurones du raphe magnus dans cette chaîne, les chercheurs ont examiné deux candidats : le glutamate, un neurotransmetteur excitateur commun, et l’ocytocine, mieux connue comme hormone de « l’attachement ». En délivrant des drogues ciblées dans le raphe magnus pendant que l’hypothalamus était stimulé artificiellement, ils ont découvert que le blocage des récepteurs à l’ocytocine réduisait fortement les contractions coliques, alors que le blocage des récepteurs au glutamate ne le faisait pas. L’imagerie microscopique a confirmé que des fibres contenant de l’ocytocine provenant de l’hypothalamus établissent des contacts étroits avec des neurones sérotoninergiques du raphe qui projettent vers la moelle épinière. En pratique, l’ocytocine libérée dans le raphe semble activer les cellules sérotoninergiques, qui stimulent ensuite le centre spinal de la défécation.
Éteindre la voie réduit les selles induites par le stress
Enfin, l’équipe a cherché à savoir si cette voie est réellement pertinente chez des animaux éveillés soumis au stress. En utilisant une méthode « chimio‑génétique » moderne, ils ont conçu uniquement les neurones hypothalamiques projetant vers le raphe magnus pour qu’ils portent un interrupteur d’arrêt activable par un médicament. Lorsque cet interrupteur a été déclenché, la stimulation hypothalamique n’augmentait plus la motilité colique, la pression artérielle ni la fréquence cardiaque chez des rats anesthésiés. De façon plus frappante, chez des rats en liberté exposés au stress d’évitement de l’eau, la mise en silence de cette voie réduisait significativement le nombre de crottes émises, alors même que la situation stressante restait identique. Cela montre que l’axe hypothalamus–raphe–moelle–nerf pelvien n’est pas seulement présent, mais nécessaire pour la défécation complète induite par le stress.
Ce que cela signifie pour les troubles intestinaux humains
En termes simples, l’étude identifie un circuit concret « inquiétude→intestin » : des cellules sensibles au stress dans l’hypothalamus activent des neurones sérotoninergiques du tronc cérébral sensibles à l’ocytocine, qui à leur tour stimulent les nerfs spinaux et pelviens faisant contracter et vider le bas côlon. Bien que le travail ait été réalisé chez le rat, un câblage similaire existe probablement chez l’humain et peut contribuer à expliquer pourquoi certaines personnes font de la diarrhée et d’autres de la constipation sous pression. En ciblant des relais cérébraux et spinaux spécifiques, cette recherche ouvre de nouvelles pistes pour comprendre et éventuellement traiter les troubles intestinaux sensibles au stress, comme le syndrome de l’intestin irritable, où la communication cerveau–intestin dysfonctionne.
Citation: Yuki, N., Sawamura, T., Mori, A. et al. Involvement of the hypothalamus–raphe magnus–spinal defecation center axis in stress-induced defecation in rats. Commun Biol 9, 411 (2026). https://doi.org/10.1038/s42003-026-09779-5
Mots-clés: stress et fonction intestinale, connexion cerveau-intestin, motilité du côlon, ocytocine et sérotonine, syndrome de l’intestin irritable