Clear Sky Science · fr
Optimisation de la précision CRISPR dans les embryons de souris via un ciblage dominant par réparation par jonctions médiées par micro-homologie
Pourquoi obtenir des souris génétiquement modifiées plus nettes est important
Les outils d’édition génomique comme CRISPR ont rendu remarquablement facile la création de souris modèles de maladies humaines, mais il existe un problème caché : les modifications génétiques chez la toute première génération d’animaux sont souvent désordonnées et hétérogènes. Cela ralentit les expériences, réduit leur fiabilité et augmente le nombre d’animaux nécessaires. Cette étude présente une méthode pour orienter les coupures CRISPR dans les embryons de souris vers des résultats hautement prévisibles, de sorte que la plupart des souris fondatrices naissent avec la même mutation bien définie—apportant une biologie plus propre et une meilleure éthique à la recherche en édition génomique.
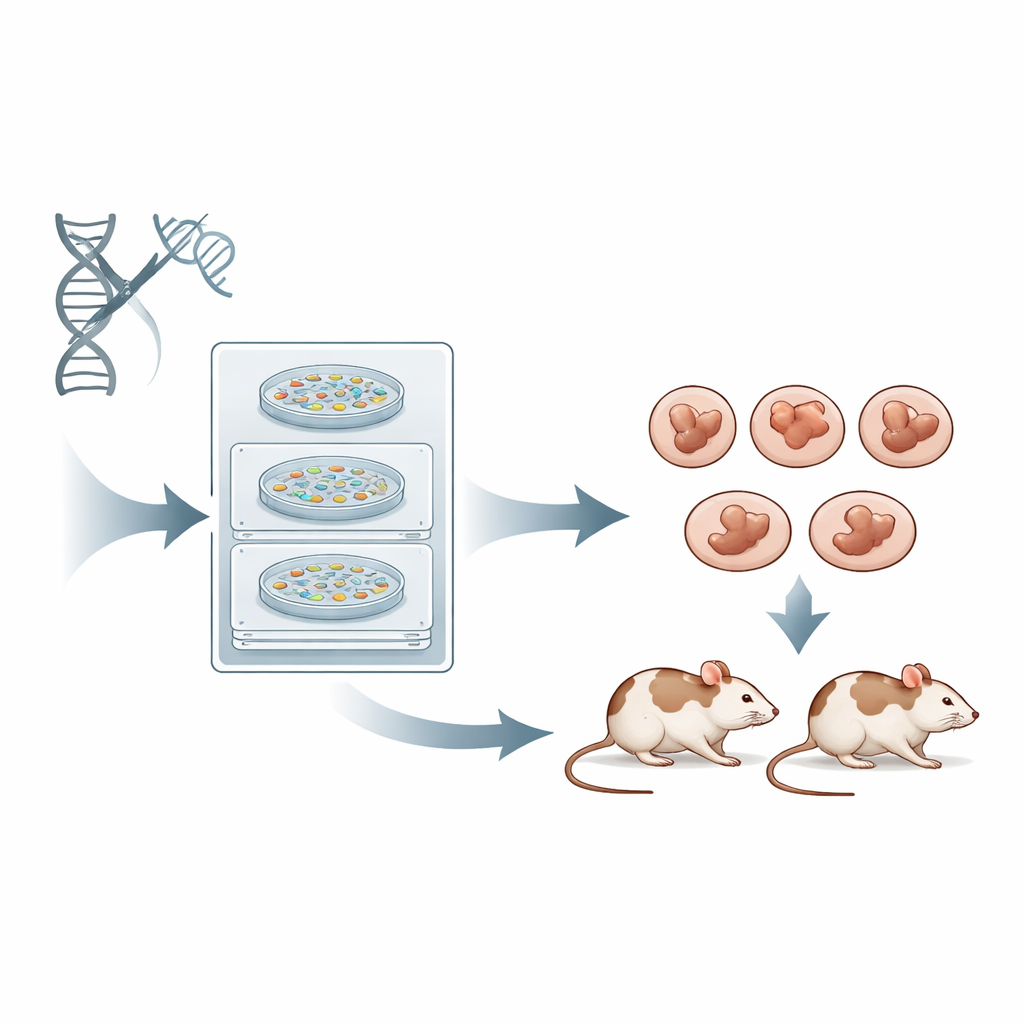
Le défi des réparations ADN désordonnées
Lorsque CRISPR coupe l’ADN, la cellule doit réparer la cassure en utilisant ses propres systèmes de réparation. La voie la plus courante, appelée jonction d’extrémités non homologue (NHEJ), est rapide mais imprécise, produisant un mélange de petites insertions et délétions au site de coupure. Une autre voie, la jonction médiée par micro-homologie (MMEJ), a tendance à supprimer des segments d’ADN de manière stéréotypée en utilisant de courtes séquences appariées comme guides. Les deux sont beaucoup plus efficaces que la voie dirigée par homologie, précise mais lente. Dans les expériences CRISPR standard, les chercheurs se concentrent principalement sur la capacité d’un ARN guide à couper fortement et sur le faible nombre de sites hors cible, et prêtent beaucoup moins d’attention à la voie de réparation favorisée ou à la mutation exacte qui résultera. Le résultat est que de nombreuses souris fondatrices portent un patchwork de mutations différentes dans différentes cellules, obligeant les chercheurs à élever la génération suivante avant de pouvoir travailler avec un génotype propre et uniforme.
Une manière plus intelligente de choisir les guides CRISPR
Les auteurs ont tenté de renverser cette logique en concevant des guides non seulement pour la puissance et la sécurité, mais aussi pour la prévisibilité. Ils ont commencé par inDelphi, un outil d’apprentissage automatique entraîné sur d’énormes jeux de données de mutations induites par CRISPR dans des cellules en culture. inDelphi n’indique pas seulement la fréquence d’édition d’un site ; il prédit l’ensemble des insertions et délétions possibles et la fréquence de chacune, en accordant une attention particulière aux événements guidés par micro-homologie. L’équipe a parcouru le gène de la tyrosinase (Tyr) chez la souris, où la perte de fonction rend les animaux albinos, et a sélectionné des ARN guides prédits pour favoriser des délétions médiées par micro-homologie fortes et répétables tout en maintenant un faible risque hors cible. Ils ont ensuite édité des embryons de souris et mesuré les mutations résultantes par séquençage profond. Globalement, le génotype préféré par inDelphi pour chaque guide est apparu à des fréquences similaires dans les embryons, comme prédit, et les guides présentant des caractéristiques de micro-homologie plus fortes ont effectivement produit des schémas de mutation plus uniformes.
Utiliser les cellules souches comme répétition
Cependant, la prédiction seule n’était pas suffisante. Lorsque l’équipe a comparé les prévisions d’inDelphi avec les schémas d’édition réels, elle n’a trouvé qu’un accord modéré. Pour combler cet écart, ils ont introduit une étape intermédiaire pratique : tester chaque guide dans des cellules souches embryonnaires de souris qui partagent de nombreuses caractéristiques avec les tout premiers embryons. Après transfec tion de ces cellules avec les composants CRISPR, ils ont trié les cellules éditées et séquencé les sites ciblés. Les profils de mutation dans les cellules souches correspondaient beaucoup mieux à ceux observés dans les embryons que le modèle informatique. Les guides produisant une suppression dominante unique dans les cellules souches faisaient typiquement de même dans les blastocystes et les embryons à un stade ultérieur. En combinant le classement d’inDelphi avec cette « répétition » en cellules souches, les chercheurs ont pu choisir de façon fiable des guides qui favorisent la réparation par micro-homologie et minimisent la diversité des allèles mutants.
De la couleur des yeux aux membres manquants
Les auteurs ont mis leur pipeline à l’épreuve sur des animaux vivants. Pour le gène Tyr, ils ont choisi trois guides représentant une précision prédite élevée, moyenne et faible et ont transféré les embryons édités dans des mères porteuses. Au jour 11.5 du développement, ils ont examiné la pigmentation des yeux et séquencé chaque embryon individuellement. Le guide fortement en faveur de la micro-homologie a produit des embryons majoritairement albinos portant une petite délétion dominante, souvent sur les deux copies du gène, avec très peu de variation. Un guide moins optimisé a produit un mélange de perte de pigment et de pigmentation partielle lié à un ensemble de mutations plus complexe. Ils ont ensuite appliqué la même approche au gène Fgf10, dont la perte de fonction entraîne des embryons sans membres. En sélectionnant un guide prédit—et confirmé dans les cellules souches—pour produire une délétion spécifique de quatre bases avec une forte probabilité d’inactiver le gène, ils ont généré des embryons au jour 15.5 uniformément dépourvus de membres et présentant un ensemble fortement enrichi des délétions attendues. Pour les deux gènes, les mêmes quelques types de mutations dominaient dans les prédictions d’inDelphi, les cellules souches, les embryons précoces et les embryons à un stade avancé.
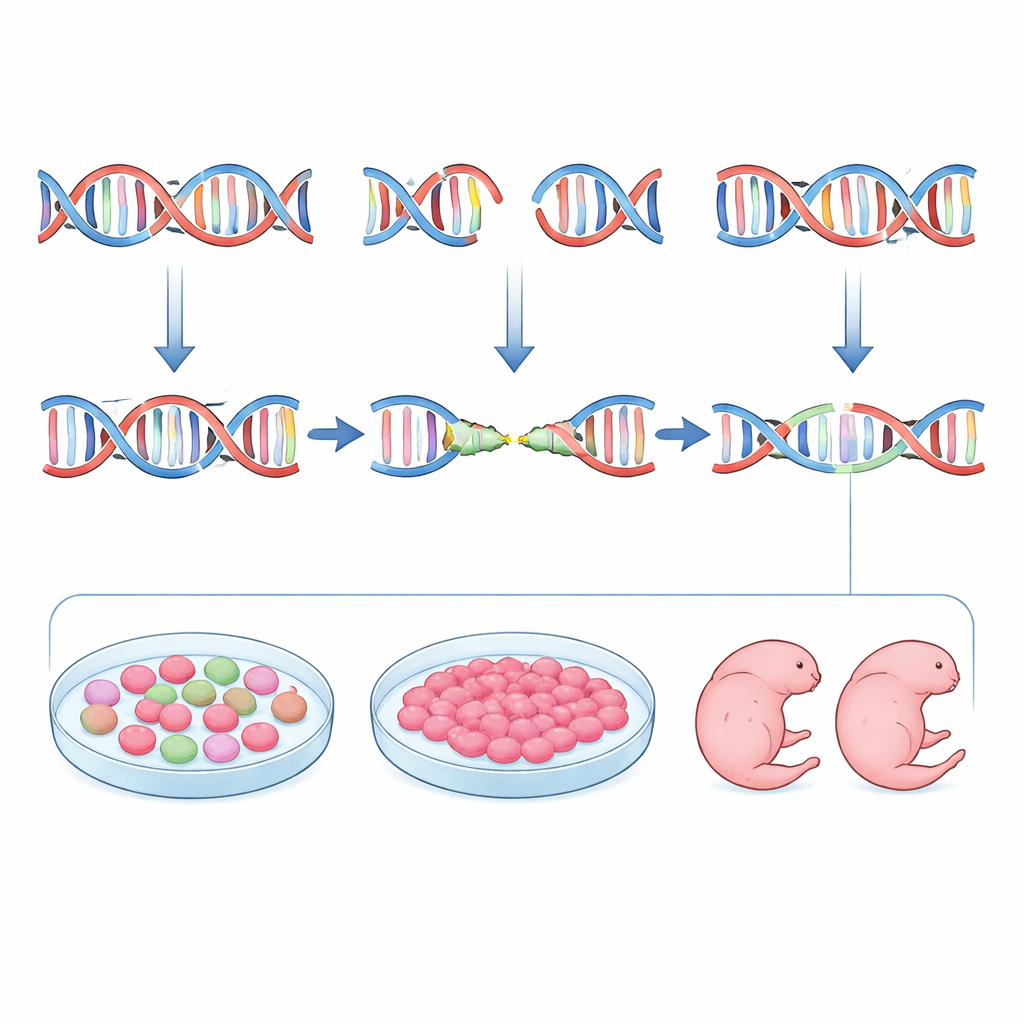
Une génétique plus nette avec moins d’animaux
Concrètement, l’étude propose un nouveau modèle pour concevoir des expériences CRISPR chez la souris. Plutôt que de passer directement d’un guide conçu par ordinateur à l’édition d’embryons, les auteurs préconisent un pipeline intégré : utiliser inDelphi et des outils d’évaluation des sites hors cible pour choisir des guides susceptibles de favoriser des délétions médiées par micro-homologie et des décalages de cadre, tester ces guides dans des cellules souches embryonnaires pour confirmer à la fois l’efficacité et l’uniformité des mutations, puis n’avancer vers le travail sur embryons que les meilleurs candidats. Cette stratégie produit des souris fondatrices dont les cellules partagent massivement la même mutation bien caractérisée, les rendant immédiatement utiles pour modéliser des maladies humaines—en particulier celles causées par des délétions récurrentes—tout en réduisant le nombre d’animaux à élever et à cribler. Le résultat est une génétique plus nette, plus reproductible et une voie plus éthique vers des modèles puissants de maladies.
Citation: Lkhagvadorj, K., Okamura, E., Taki, T. et al. Optimizing CRISPR precision in mouse embryos via microhomology-mediated end joining-dominant targeting. Commun Biol 9, 371 (2026). https://doi.org/10.1038/s42003-026-09771-z
Mots-clés: CRISPR, modèles murins, édition du génome, réparation de l’ADN, modélisation des maladies