Clear Sky Science · fr
La glycosylation comme régulateur dynamique des voies de signalisation innée RLR et cGAS‑STING
Comment les étiquettes sucrées aident les cellules à détecter les virus
Nos cellules sont en permanence à l’affût des virus envahisseurs, et une grande partie de cette défense repose sur de minuscules étiquettes sucrées fixées aux protéines. Cette revue explique comment ces marqueurs, appelés glycosylation, agissent davantage comme des variateurs que comme de simples interrupteurs marche/arrêt pour des voies antivirales clés. Comprendre ce réglage fin basé sur les sucres pourrait ouvrir de nouvelles voies pour renforcer les vaccins, traiter les infections virales et même exploiter le système immunitaire contre le cancer.
L’alarme précoce de la cellule
Lorsque des virus pénètrent dans une cellule, ils laissent des brins d’ARN ou d’ADN caractéristiques. Des systèmes « d’alarme » spécialisés patrouillent l’intérieur de la cellule à la recherche de ces débris génétiques. Une voie, appelée voie des récepteurs de type RIG‑I (RLR), détecte l’ARN viral. Une autre, connue sous le nom de voie cGAS–STING, perçoit l’ADN qui apparaît au mauvais endroit dans la cellule. Une fois déclenchées, ces deux voies activent des cascades chimiques qui aboutissent à la libération d’interférons de type I et de molécules inflammatoires — des signaux puissants qui avertissent les cellules voisines et mobilisent les défenses immunitaires. Parce qu’un signal trop faible ou trop fort peut être dangereux, la cellule doit régler soigneusement ces alarmes, et la glycosylation en est un des moyens clés. 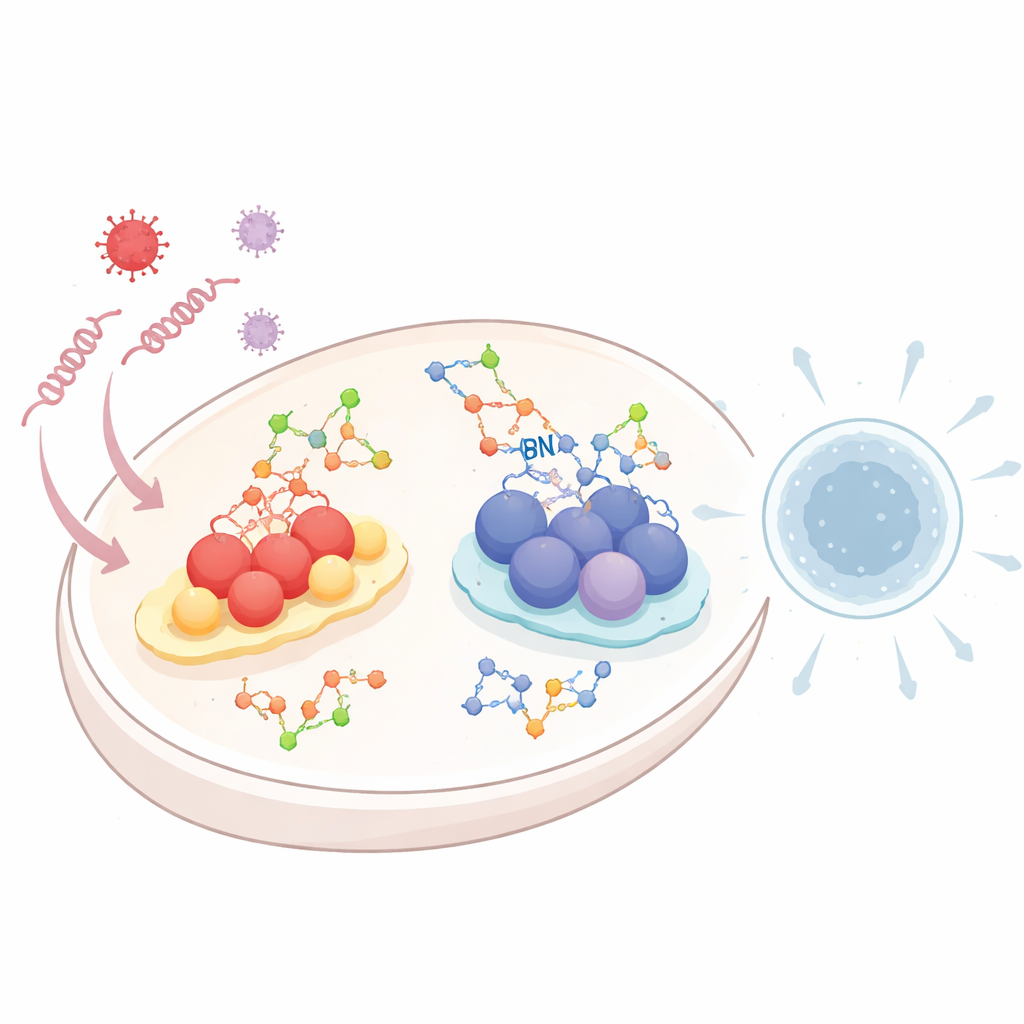
Les enveloppes sucrées comme contrôles de précision
La glycosylation ajoute de petites unités sucrées aux protéines à différents endroits de la cellule. Dans le réseau d’expédition interne de la cellule, le réticulum endoplasmique et l’appareil de Golgi, des chaînes glycanes N‑liées volumineuses aident les protéines à bien se replier, à rester stables et à atteindre la bonne membrane. En revanche, une forme plus légère appelée O‑GlcNAcylation place un seul sucre sur des protéines du cytoplasme et du noyau. Cette marque minimaliste est très dynamique, se renouvelant rapidement grâce à deux enzymes qui l’ajoutent ou l’enlèvent en réponse aux niveaux de nutriments et au stress. La revue décrit comment ces différents types de sucres ne se contentent pas d’activer ou d’inhiber les senseurs immunitaires ; ils modulent plutôt la propension des senseurs à s’agréger, leur durée de vie et l’intensité de leur signal. De cette manière, la glycosylation relie l’état métabolique de la cellule à sa capacité à lutter contre l’infection.
Régler la voie de détection de l’ARN
Dans le système RLR qui détecte l’ARN, une protéine relais centrale appelée MAVS est ancrée sur les mitochondries et sert de plaque tournante essentielle. La revue montre que l’O‑GlcNAcylation de MAVS peut à la fois accélérer et freiner la signalisation antivirale, selon le site d’attachement du sucre. Des étiquettes sucrées à certains emplacements favorisent d’autres modifications protéiques, comme un type spécifique de chaînes d’ubiquitine, qui aident MAVS à former de larges amas de signalisation et stimulent une production forte d’interféron contre les virus à ARN. D’autres sites glycosylés maintiennent MAVS dispersé et inactif en conditions normales, évitant ainsi une inflammation inutile. L’infection virale et les variations du métabolisme conduisant à la production de sucres peuvent déplacer l’équilibre entre ces marques activatrices et inhibitrices. Des modifications apparentées sur un autre facteur, IRF5, peuvent pousser le système immunitaire vers des « tempêtes de cytokines » dommageables, soulignant que plus de sucre n’est pas forcément mieux. Parallèlement, les virus peuvent exploiter des sucres N‑liés sur des protéines de surface cellulaire telles que le récepteur du facteur de croissance EGFR pour marquer des senseurs en amont comme RIG‑I en vue de leur dégradation, émoussant ainsi les défenses antivirales.
Régler la voie de détection de l’ADN
La voie cGAS–STING qui détecte l’ADN est également fortement modulée par la glycosylation. STING, une protéine membranaire du réticulum endoplasmique, a besoin de chaînes glycanes N‑liées pour se replier correctement, rester stable et s’assembler en complexes de signalisation une fois activée par des messagers dérivés de l’ADN. Sans ces sucres, STING ne parvient pas à former les structures d’ordre supérieur ni à circuler dans les compartiments cellulaires nécessaires à une libération robuste d’interféron. Parallèlement, l’O‑GlcNAcylation de STING en un site particulier favorise un autre ensemble de marques chimiques qui promeuvent son agrégation et son déplacement, amplifiant les signaux antiviraux contre les virus à ADN. Des chaînes sucrées appelées glycosaminoglycanes sulfatés, construites dans le Golgi, aident en outre en facilitant la polymérisation de STING activé en longues structures qui recrutent des enzymes en aval. Les virus contre‑attaquent en modifiant leurs propres glycoprotéines ou en déclenchant des voies de dégradation qui ciblent STING, souvent dans les mêmes espaces cellulaires où ces décorations sucrées sont ajoutées ou traitées. 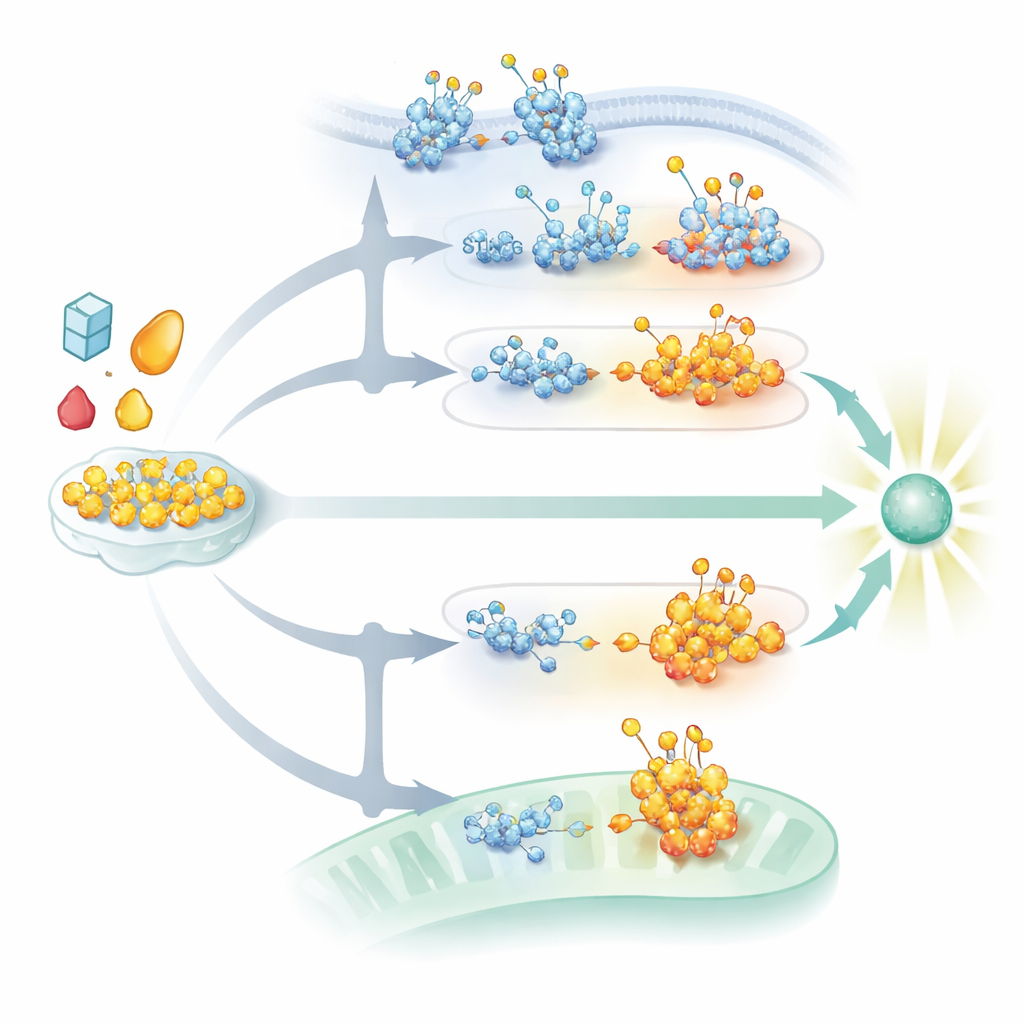
Métabolisme, maladies et thérapies futures
Parce que le principal donneur de sucre pour l’O‑GlcNAcylation est produit par une voie métabolique connue sous le nom de voie biosynthétique des hexosamines, les variations d’utilisation des nutriments façonnent directement la signalisation antivirale. De nombreux virus stimulent cette voie à leur profit, tandis que l’augmentation ou le blocage expérimentaux du flux d’hexosamines peuvent renforcer ou affaiblir les réponses antivirales dans des modèles animaux. La revue relie ces mécanismes aux maladies humaines : les tumeurs réorganisent fréquemment la glycosylation pour atténuer la signalisation des interférons et échapper à l’attaque immunitaire, tandis que le stress métabolique chronique ou des défauts héréditaires du traitement des glycannes peuvent faire pencher l’équilibre vers l’auto‑immunité néfaste. Les auteurs soutiennent que les enzymes contrôlant la glycosylation — en particulier celles qui ajoutent ou retirent l’O‑GlcNAc ou construisent des structures N‑liées clés — sont des cibles médicamenteuses prometteuses mais difficiles. Les thérapies futures devront probablement agir de manière site‑spécifique et adaptée au contexte, orientant le « code glyco » vers une meilleure protection contre les infections, le cancer et les troubles inflammatoires sans provoquer de nouveaux déséquilibres immunitaires.
La vision d’ensemble pour la santé quotidienne
En termes concrets, cet article révèle que les alarmes antivirales de première ligne du corps ne fonctionnent pas isolément — elles sont connectées à l’usage énergétique de la cellule et à sa chimie des sucres. De petites étiquettes sucrées sur une poignée de protéines critiques déterminent si un génome viral errant déclenche un avertissement mesuré, une défense complète ou une réaction excessive dangereuse. En décodant et, à terme, en apprenant à ajuster ce système de contrôle basé sur les sucres, les chercheurs espèrent concevoir des traitements qui rendent les vaccins plus efficaces, aident à éliminer des infections tenaces, dévoilent les tumeurs au système immunitaire et calment l’inflammation incontrôlée dans les maladies auto‑immunes.
Citation: Tong, J., Zhang, W., Xue, M. et al. Glycosylation as a dynamic regulator of RLR and cGAS-STING innate immune signalling pathways. Commun Biol 9, 422 (2026). https://doi.org/10.1038/s42003-026-09767-9
Mots-clés: immunité innée, glycosylation, voie RLR, cGAS‑STING, O‑GlcNAcylation