Clear Sky Science · fr
Aperçus structurels de la machinerie de type IV pilus de Thermus thermophilus assemblant deux pili distincts
De minuscules poils bactériens aux grandes fonctions
Les bactéries sont minuscules, mais nombre d’entre elles portent à leur surface d’étonnants « poils » qui leur permettent de se déplacer, de s’accrocher aux surfaces et même d’attraper de l’ADN libre dans leur environnement. Dans cette étude, les chercheurs examinent comment une bactérie thermophile, Thermus thermophilus, construit et met en œuvre une nanomachine sophistiquée qui pousse ces poils — appelés pili — à travers son enveloppe cellulaire. Comprendre cette machinerie révèle non seulement comment les microbes s’adaptent et évoluent, mais offre aussi des inspirations pour la nanotechnologie future et de nouvelles façons de neutraliser des bactéries nuisibles.
Deux poils différents issus d’une même machine
Thermus thermophilus produit deux types distincts de pili : un filament plus large et épais et un autre plus étroit et mince. Des travaux antérieurs ont montré que ces filaments sont constitués de blocs de construction différents et remplissent probablement des fonctions différentes, comme le déplacement à la surface ou la capture d’ADN. Pourtant, les deux sont assemblés par la même machine multipartite qui s’étend de la face interne à la face externe de la cellule. La question centrale de cette étude est de savoir comment un même système peut assembler deux filaments différents et les pousser à travers les couches protectrices de la cellule vers l’extérieur.
Cartographier le matériel caché
Pour découvrir comment la machine est agencée, les chercheurs ont utilisé la cryo-tomographie électronique, une technique qui fige rapidement les cellules et les image en 3D à très basse température. Ils ont combiné ces instantanés avec des modifications génétiques ciblées qui supprimaient ou altéraient des parties spécifiques de la machine. En comparant les cellules normales et des mutants dépourvus de certains composants, ils ont pu associer des formes floues de leurs cartes 3D aux protéines correspondantes. Des outils avancés de prédiction structurale ont ensuite été utilisés comme plans moléculaires, aidant à insérer ces modèles de protéines dans les densités observées et à assembler un modèle hypothétique de la machinerie dans son ensemble.
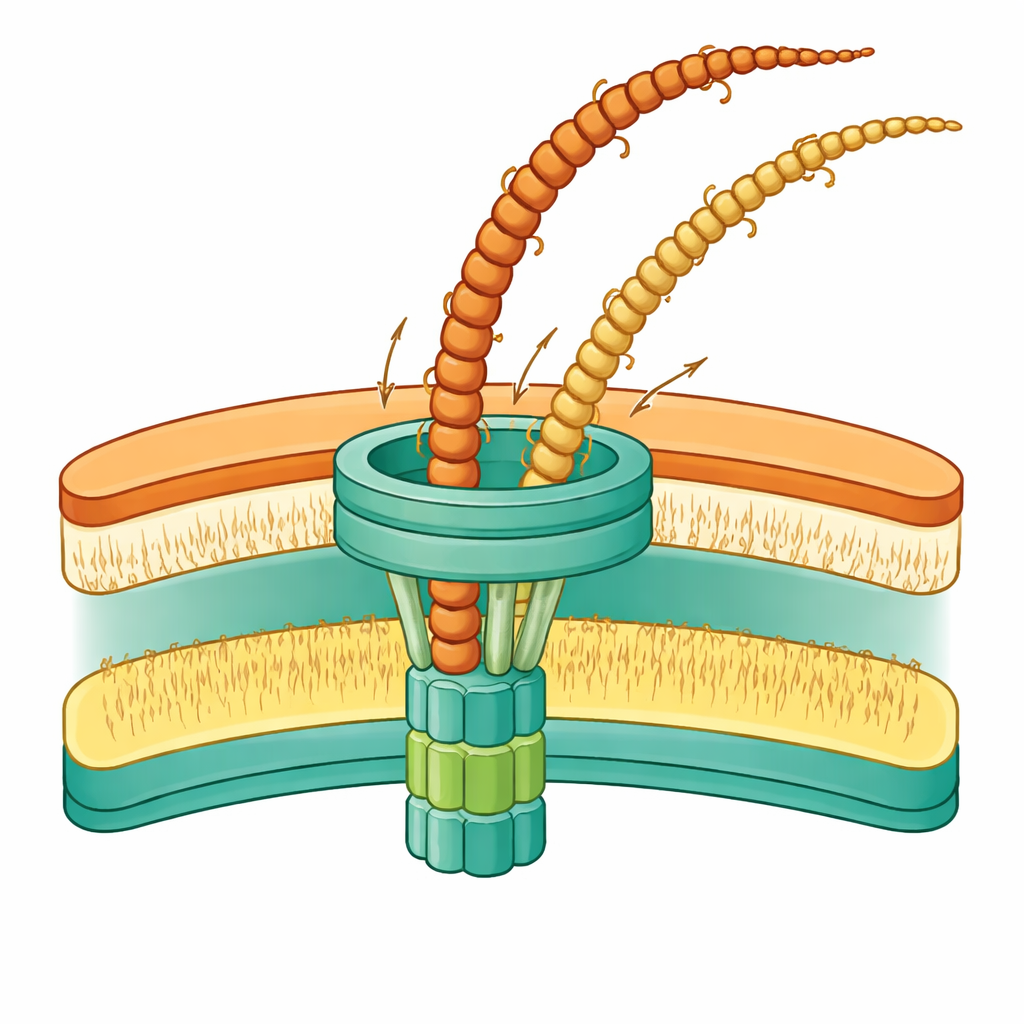
Un lien flexible qui tout retient
Un résultat marquant concerne une protéine appelée PilW. Ce composant se situe entre une porte de la membrane externe et une plate-forme interne ancrée dans la membrane interne de la cellule. Lorsque PilW manque complètement, les pili n’atteignent pas l’extérieur et s’accumulent dans l’espace entre les membranes. Lorsque seule une partie de PilW est tronquée, la machine fonctionne encore, mais ses composants internes se déplacent et les membranes environnantes se courbent vers l’intérieur. Ces observations suggèrent que PilW se comporte comme une attache flexible reliant la porte externe à la plate-forme interne, ajustant sa longueur et sa forme au gré des cycles inactifs et actifs de la machine. Les modèles de l’équipe indiquent que cette flexibilité permet au système de compenser l’écart exceptionnellement large entre les deux membranes chez Thermus, tout en alignant suffisamment les éléments pour assembler et éjecter les pili.
Observer les filaments et leurs manteaux de sucres
Parallèlement à l’imagerie in situ, les chercheurs ont également isolé les deux types de pili et les ont examinés plus en détail par cryo-microscopie électronique en simple particule. Cette approche à résolution plus élevée a révélé l’arrangement précis des blocs de construction et, surtout, a permis à l’équipe de modéliser les molécules de sucre qui décorent la surface des filaments. Le pilus plus large porte trois sites d’attachement de sucre par unité de construction, produisant un halo dense de glucides. Le pilus plus étroit n’a qu’un seul site de ce type, mais sa chaîne sucrée s’étend plus loin, donnant au filament une apparence plus volumineuse que ne le suggère son cœur protéique. Des simulations informatiques ont ensuite exploré comment ces sucres se plient et oscillent lorsque le filament traverse la porte de la membrane externe.
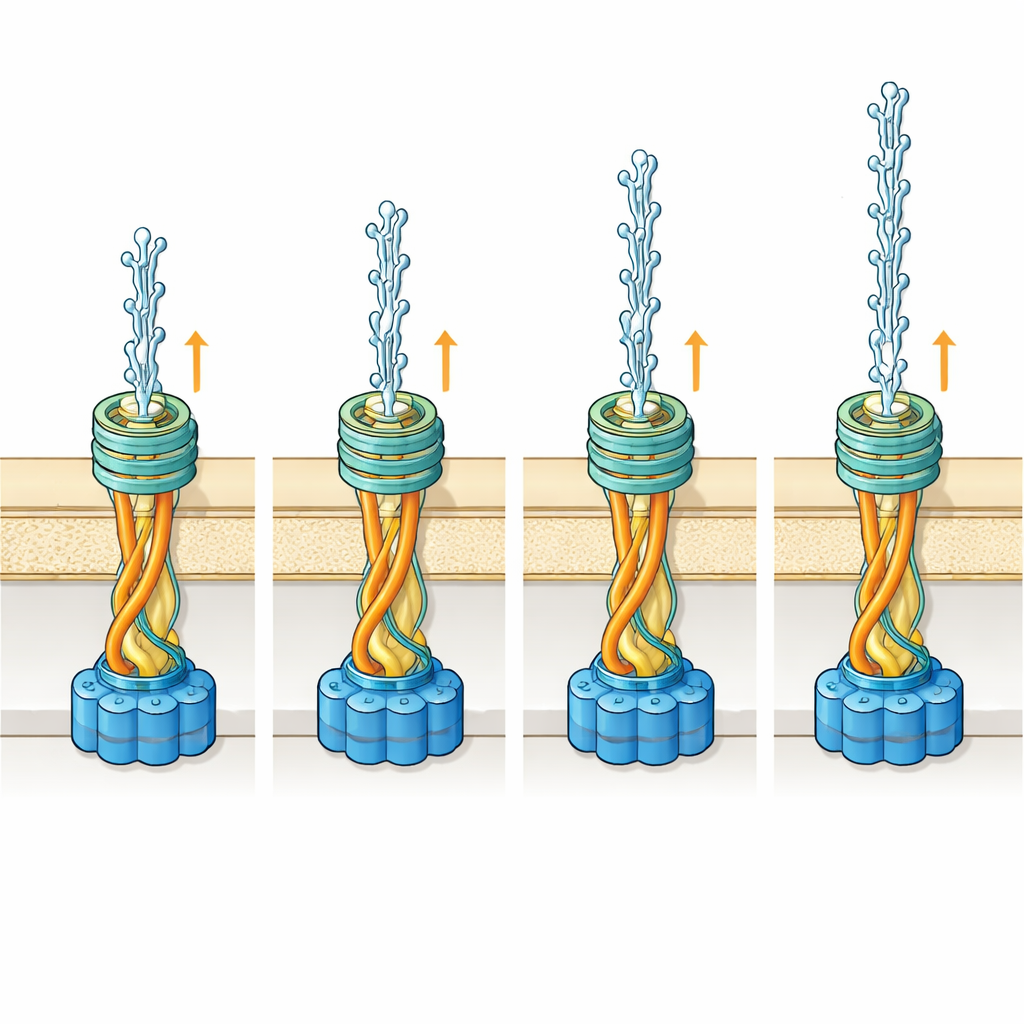
Une porte partagée pour deux câbles très différents
En positionnant leurs structures détaillées de pili dans un modèle de la porte de la membrane externe, appelée PilQ, l’équipe a constaté que les deux types de filament peuvent, en principe, glisser à travers la même ouverture. Pour le filament large, ses sucres multiples disposent de suffisamment d’espace pour adopter de nombreuses conformations en traversant la porte. Pour le filament étroit, l’espace devient restreint en un point du canal, de sorte que certaines conformations sucrées entreraient en collision avec les parois. Les simulations suggèrent que dans ce cas la chaîne sucrée resterait vraisemblablement plus serrée autour du filament pendant qu’elle est à l’intérieur de la porte et ne se déploierait qu’une fois à l’extérieur de la cellule. Plutôt que d’évoluer vers une porte plus grande et donc plus coûteuse pour accueillir confortablement les deux filaments, la bactérie semble tirer parti de la flexibilité naturelle de ces chaînes sucrées pour rendre le système efficace.
Ce que cela implique pour la vie microbienne
Dans l’ensemble, l’étude dessine un tableau cohérent de la façon dont une machine unique et adaptable assemble et exporte deux pili très différents chez une bactérie de source chaude. Une protéine de liaison flexible semble maintenir l’alignement des parties internes et externes pendant que le moteur fonctionne et que la structure se raccourcit légèrement durant la croissance active du filament. Parallèlement, les revêtements sucrés des pili leur confèrent à la fois protection et portée, tout en restant assez flexibles pour se faufiler à travers un canal de sortie relativement étroit. Pour les non-spécialistes, le message clé est que même des microbes simples reposent sur des assemblages mobiles hautement coordonnés pour survivre et évoluer — des dispositifs moléculaires dont l’élégance et l’efficacité rivalisent, et parfois surpassent, les machines humaines à l’échelle nanométrique.
Citation: Neuhaus, A., McLaren, M., Isupov, M.N. et al. Structural insights into the Thermus thermophilus type IV pilus machinery assembling two distinct pili. Commun Biol 9, 474 (2026). https://doi.org/10.1038/s42003-026-09762-0
Mots-clés: pili de type IV, nanomachines bactériennes, cryo-microscopie électronique, glycosylation des protéines, Thermus thermophilus