Clear Sky Science · fr
La modélisation axée sur le taux de croissance suggère que l’adaptation phénotypique conduit à la résistance aux médicaments dans le mélanome porteuse de BRAFV600E
Des cellules cancéreuses qui apprennent à vivre avec les médicaments
Les traitements ciblés ont transformé la prise en charge de nombreuses personnes atteintes de mélanome, un cancer cutané grave. Pourtant, ces médicaments cessent presque toujours d’être efficaces : des tumeurs qui régressaient recommencent à croître. Cette étude pose une question simple mais puissante : au lieu de s’appuyer uniquement sur des mutations génétiques, les cellules de mélanome peuvent‑elles « apprendre » à survivre au traitement en modifiant leur comportement — et cet apprentissage pourrait‑il expliquer pourquoi certaines modalités d’administration des médicaments fonctionnent mieux que d’autres ?
D’un état sensible à la survie
Les chercheurs se sont concentrés sur des cellules de mélanome porteuses d’une altération fréquente du gène BRAF, qui les rend particulièrement sensibles à une classe de médicaments appelés inhibiteurs de BRAF. Dans des expériences en laboratoire issues de travaux antérieurs, ces cellules ont été exposées à l’agent encorafénib à des doses et pendant des durées variées. En mesurant attentivement la vitesse de croissance ou de mort cellulaire dans chaque condition, les auteurs ont réparti les cellules en deux grandes catégories : les cellules naïves vis‑à‑vis du médicament, qui ne l’avaient jamais rencontré, et les cellules adaptées au médicament, qui y avaient été exposées pendant au moins une semaine. Les cellules naïves se développaient bien sans traitement mais étaient fortement ralenties ou tuées par le médicament. Les cellules adaptées, en revanche, croissaient mieux en présence du médicament mais perdaient cet avantage lorsque le médicament était retiré — ce qui suggère que leur survie était liée à un changement d’état flexible et réversible plutôt qu’à une altération génétique permanente.
Une carte des comportements cellulaires cachés
Pour comprendre ces changements, l’équipe a construit un modèle mathématique où chaque cellule cancéreuse se voit attribuer un « état phénotypique » — une position abstraite sur une échelle allant de très sensible à très résistante au médicament. Plutôt que de supposer seulement deux types de cellules, ils ont permis de nombreux états intermédiaires, reflétant des transitions progressives observées dans des marqueurs biologiques de résistance. Pour chaque combinaison d’état et de dose de médicament, ils ont estimé un taux de croissance net, qui peut être positif (plus de divisions que de morts) ou négatif (plus de morts que de divisions). Tous ces taux ont été disposés dans une grille, ou « matrice de fitness », qui fonctionne comme un paysage : certains états à certaines doses sont favorables à la survie des cellules, d’autres sont mortels. Dans le modèle, les cellules peuvent se déplacer pas à pas à travers ce paysage lorsque le traitement est activé ou arrêté.
Les cellules dérivent‑elles ou gravissent‑elles la pente vers un avantage ?
La question clé était de savoir comment les cellules se déplacent dans ce paysage. Les auteurs ont testé quatre stratégies possibles. Dans la première, les cellules ne changent jamais d’état : toute cellule résistante doit donc être présente dès le départ. Dans la seconde, les cellules errent au hasard entre états voisins, comme une marche aléatoire, indépendamment de l’amélioration ou non de leur situation. Dans les deux stratégies restantes, les cellules ont tendance à se diriger vers des états où leur taux de croissance est plus élevé — soit de manière bruitée, avec quelques erreurs, soit de façon forte et déterminée, grimpant toujours vers une meilleure survie. Lorsque l’équipe a exécuté des simulations informatiques et les a comparées aux données expérimentales réelles, en particulier aux expériences où le médicament était administré en continu ou en mode on–off (une semaine on, une semaine off), seules les stratégies où les cellules gravissent la pente vers une fitness supérieure ont reproduit l’observé : un traitement intermittent à forte dose supprimait plus efficacement le nombre de cellules qu’un traitement continu avec le même temps total et une quantité globale plus élevée de médicament.
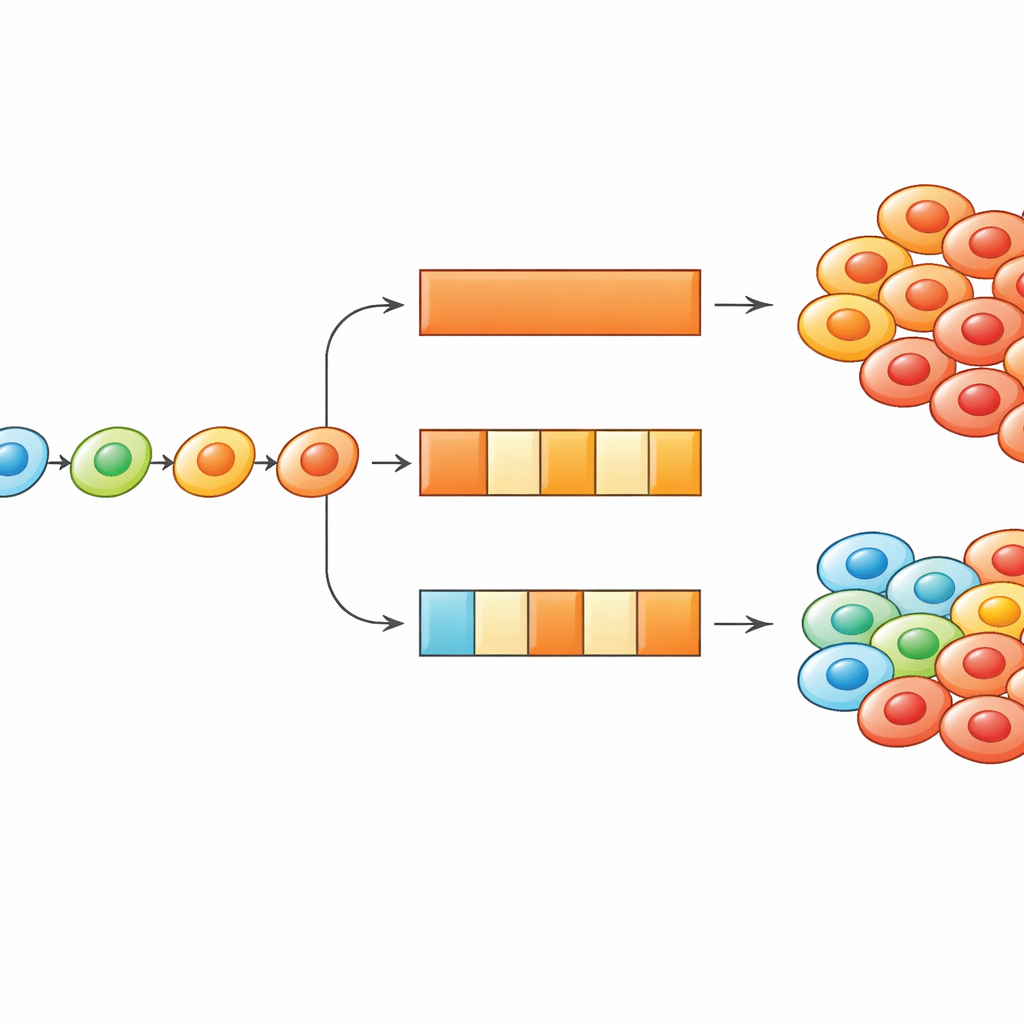
Utiliser une posologie on–off pour retourner l’adaptation contre le cancer
En approfondissant, les chercheurs ont utilisé à la fois des simulations et des équations plus simples pour explorer à quelle fréquence les cellules peuvent changer d’état et quelle doit être la durée des périodes avec ou sans médicament. Ils ont constaté que, lorsque les cellules s’adaptent de manière dirigée, les calendriers de traitement peuvent être ajustés soit pour ralentir, soit pour exploiter cette adaptation. Raccourcir la fréquence à laquelle les cellules peuvent mettre à jour leur état — conceptuellement, ralentir les mécanismes biologiques qui permettent le changement phénotypique — tend à rendre les traitements intermittents plus puissants, car les cellules ne peuvent pas si rapidement atteindre des états très résistants. À l’inverse, si les cellules commencent dans un état fortement résistant, des pauses médicamenteuses peuvent leur laisser le temps de revenir vers des états plus sensibles, de sorte que la réintroduction du médicament provoque une vague de mortalité cellulaire. L’étude montre comment le timing des doses et la vitesse d’adaptation cellulaire façonnent ensemble quel schéma est le plus efficace.
Ce que cela signifie pour les soins futurs du cancer
Pour le non‑spécialiste, le message central est que les cellules cancéreuses ne sont pas de simples ennemis fixes ; ce sont des métamorphes. Dans ce système de mélanome, les cellules semblent activement se diriger vers des comportements qui les aident à croître dans les conditions auxquelles elles sont confrontées. Le modèle des auteurs suggère que cette adaptation dirigée à elle seule — sans faire intervenir différents clones permanents — peut expliquer pourquoi des schémas on–off surpassent parfois un traitement continu, même lorsqu’ils utilisent globalement moins de médicament. Bien que ces résultats proviennent de cellules cultivées en laboratoire et nécessitent des travaux supplémentaires avant d’orienter la prise en charge des patients, l’approche offre un cadre pratique : en mesurant la vitesse et la direction de l’adaptation des cellules cancéreuses, les cliniciens pourraient un jour concevoir des calendriers de traitement qui non seulement attaquent les tumeurs mais aussi orientent leur « apprentissage » phénotypique vers des impasses plutôt que des échappatoires.
Citation: Hamis, S., Browning, A.P., Jenner, A.L. et al. Growth rate-driven modelling suggests that phenotypic adaptation drives drug resistance in BRAFV600E-mutant melanoma. Commun Biol 9, 385 (2026). https://doi.org/10.1038/s42003-026-09760-2
Mots-clés: mélanome, résistance aux traitements, plasticité cellulaire, thérapie intermittente, modélisation mathématique