Clear Sky Science · fr
Base structurale de l’activation par dimérisation de la réductase de l’oxyde nitrique dépendante du quinol de Neisseria meningitidis
Comment les bactéries déjouent notre défense immunitaire
Lorsque des bactéries nocives envahissent l’organisme, nos cellules immunitaires libèrent des molécules toxiques comme l’oxyde nitrique pour les éliminer. Certains agents pathogènes ont toutefois développé des stratagèmes moléculaires pour neutraliser cette attaque et survivre. Cette étude révèle, au niveau atomique, comment une enzyme bactérienne clé se réorganise en paires pour devenir bien plus efficace dans la détoxification de l’oxyde nitrique, et pourquoi comprendre ce comportement polymorphe pourrait ouvrir de nouvelles pistes pour la conception d’antibiotiques.
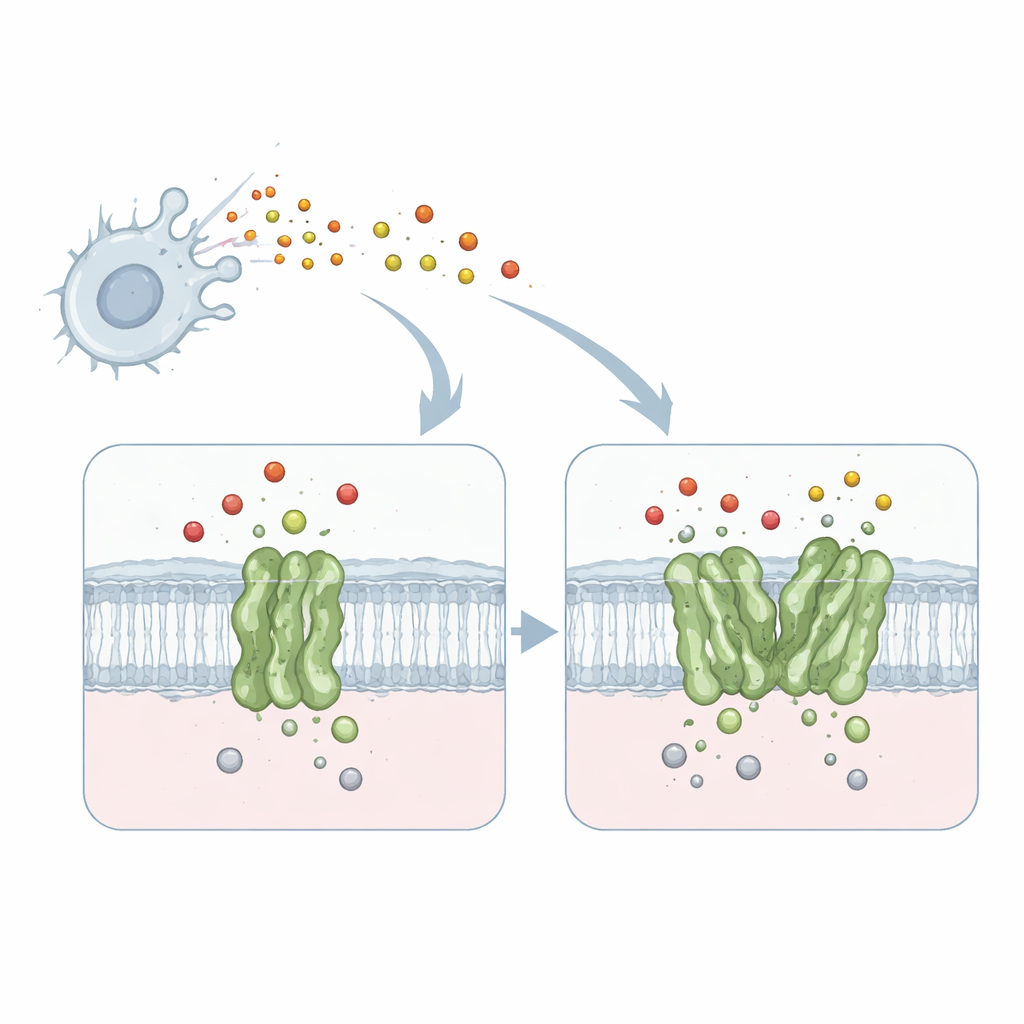
Une minuscule machine qui désarme un gaz toxique
Le travail porte sur une protéine membranaire appelée réductase de l’oxyde nitrique dépendante du quinol, ou qNOR, provenant de la bactérie responsable de la méningite, Neisseria meningitidis. qNOR se situe dans la membrane bactérienne et convertit l’oxyde nitrique — un gaz toxique produit par notre système immunitaire — en produits moins nocifs. Cette détoxification permet au microbe de continuer à respirer et à croître même dans des environnements hostiles comme les macrophages humains. Parce que la respiration et l’élimination de l’oxyde nitrique sont vitales pour la survie du pathogène, qNOR constitue une cible intéressante pour de nouveaux médicaments antimicrobiens.
Quand un exemplaire suffit mais deux valent mieux
Des études biochimiques antérieures ont montré que qNOR peut exister soit comme unité unique (monomère), soit en paire (dimère), et que le dimère neutralise l’oxyde nitrique deux à quatre fois plus rapidement. Jusqu’à présent, on ignorait pourquoi le simple appareillage de deux copies de la même enzyme avait un effet aussi spectaculaire sur la performance. Pour répondre à cette question, les chercheurs ont utilisé la cryo-microscopie électronique monoparticule à haute résolution pour capturer des structures tridimensionnelles détaillées du qNOR monomérique et dimérique issus de la même souche bactérienne. Ils ont obtenu des vues quasi atomiques — 1,89 Å pour le dimère et 2,25 Å pour le monomère — suffisamment nettes pour localiser des chaînes latérales d’acides aminés individuelles, des ions métalliques et de nombreuses molécules d’eau.
Une hélice flexible devient une bride stabilisatrice
De manière surprenante, le cœur catalytique de l’enzyme — le centre métallique où l’oxyde nitrique est converti — apparaissait presque identique dans les deux formes. Les différences clés se situaient plutôt à distance, dans une hélice transmembranaire appelée TM10 et dans la manière dont elle contacte une autre hélice (TM2) lorsque deux molécules de qNOR s’associent. Dans le monomère, TM10 est faiblement ancrée et peut osciller et se plier de façon importante, comme l’a révélé l’analyse computationnelle des données cryo-EM. Dans le dimère, TM10 de chaque partenaire se verrouille contre celle de l’autre pour former un faisceau de quatre hélices, limitant fortement son mouvement. Cette stabilisation repositionne subtilement un acide aminé crucial, une glutamate nommée Glu563, le rapprochant d’une autre glutamate (Glu494) près du site actif et façonnant une voie plus concentrée pour les protons entrants nécessaires à la réaction.
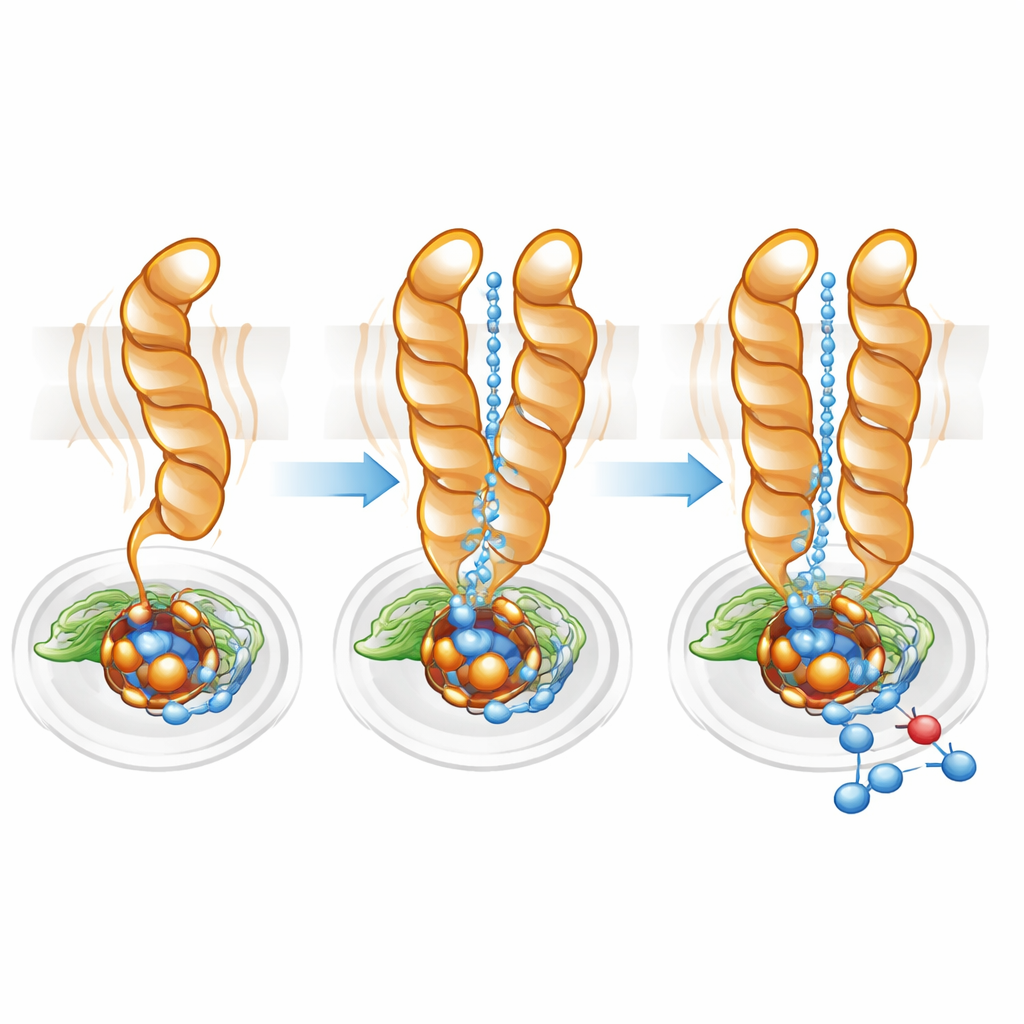
Ajuster finement l’autoroute aux protons
Les protons — ions hydrogène chargés positivement — doivent être livrés efficacement depuis l’intérieur de la cellule jusqu’au site actif enfoui pour que la réduction de l’oxyde nitrique puisse avoir lieu. À l’aide d’un logiciel de cartographie des voies, l’équipe a identifié une cavité hydrophile reliant le cytoplasme au site actif chez le monomère comme chez le dimère. Cependant, dans le monomère ce canal était plus large et plus diffus, cohérent avec la plus grande mobilité de TM10. Dans le dimère, la position verrouillée de TM10 et l’orientation favorable de Glu563 ont contribué à définir un trajet plus direct et mieux organisé. La mutation de Glu563 en acides aminés incapables de former les mêmes interactions a réduit l’activité de l’enzyme à moins de 10 % de la normale et a également déstabilisé le dimère, tandis que des mutations à des positions apparentées ont diminué la quantité de fer non héminique essentielle au site actif. Ensemble, ces résultats montrent que la formation du dimère et le positionnement précis de Glu563 et Glu494 sont étroitement liés à la fois à l’intégrité structurelle et à l’efficacité catalytique.
Transformer les découvertes structurelles en nouveaux traitements
Les résultats établissent un lien clair entre l’association des protéines à la surface membranaire et des ajustements fins en profondeur du site actif qui contrôlent l’efficacité de l’élimination de l’oxyde nitrique par qNOR. En termes simples, lorsque deux copies de l’enzyme s’assemblent, elles redressent et rigidifient un segment flexible qui aide à canaliser les protons vers le centre réactionnel, augmentant ainsi le rendement de l’enzyme. Pour le développement de médicaments, cela suggère une stratégie non conventionnelle : au lieu de bloquer directement le site actif, on pourrait concevoir des molécules qui forcent la dissociation du dimère ou perturbent l’interaction Glu563–Glu494, contraignant l’enzyme à son état monomérique lent. Étant donné que qNOR et des enzymes apparentées sont cruciales pour la survie de plusieurs pathogènes dangereux et résistants aux médicaments, de telles approches guidées par la structure pourraient contribuer à la prochaine génération d’antimicrobiens ciblés.
Citation: Gopalasingam, C.C., Egami, H., Shigematsu, H. et al. Structural basis of Neisseria meningitidis quinol dependent nitric oxide reductase activation by dimerization. Commun Biol 9, 433 (2026). https://doi.org/10.1038/s42003-026-09754-0
Mots-clés: détoxification de l’oxyde nitrique, respiration bactérienne, enzymes membranaires, cryo-microscopie électronique, cibles médicamenteuses antimicrobiennes