Clear Sky Science · fr
La multi-omique spatiale révèle les caractéristiques immuno-métaboliques induites par électroporation irréversible dans la marge inflammatoire du cancer du foie
Pourquoi un nouveau traitement du cancer du foie mérite d’être examiné de plus près
L’électroporation irréversible (IRE) est une méthode récente pour détruire les tumeurs hépatiques en utilisant de courts impulsions électriques à haute tension au lieu de la chaleur. Parce qu’elle peut préserver les vaisseaux sanguins et les voies biliaires adjacents, elle est particulièrement utile pour les cancers situés dans des zones délicates. Pourtant, jusqu’à un tiers des patients voient la tumeur réapparaître juste à côté de la zone traitée. Cette étude interroge ce qui se passe dans cette étroite région frontalière après l’IRE — et si des changements discrets dans les cellules immunitaires et le métabolisme cellulaire à cet endroit pourraient discrètement préparer le terrain à une rechute tumorale.
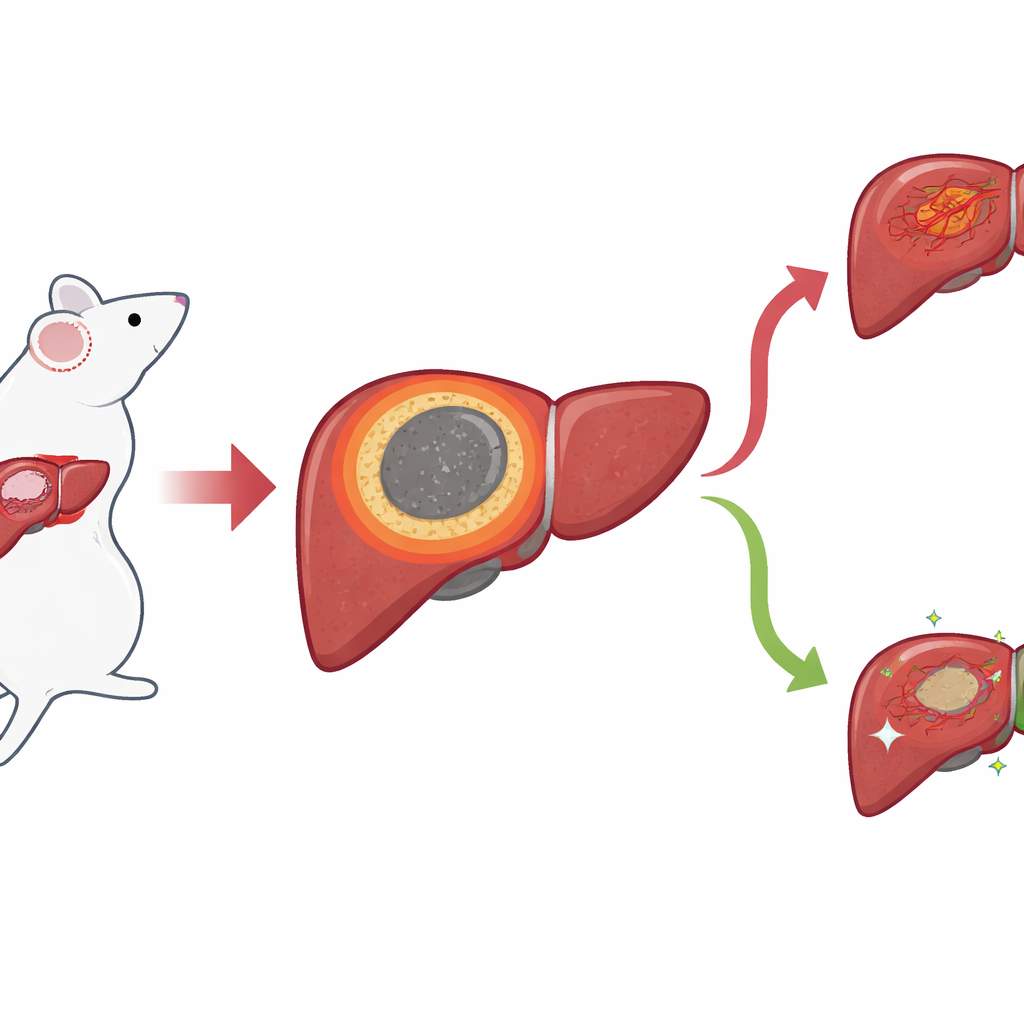
Une bordure étroite aux grandes conséquences
À l’aide d’un modèle murin de cancer du foie, les chercheurs se sont concentrés sur l’anneau mince de tissu qui se forme entre le noyau nécrotique ablaté et le foie sain environnant après l’IRE. Ils l’appellent la marge inflammatoire (IM). Les images microscopiques standard montraient que cette zone se situe précisément là où surviennent généralement les récidives locales, mais ses limites étaient difficiles à tracer à l’œil nu. Pour obtenir une image plus nette, l’équipe a appliqué des méthodes « spatiales » qui identifient les gènes et les petites molécules présentes tout en préservant leur localisation dans le tissu. Grâce à la transcriptomique spatiale, ils ont cartographié l’activité génique point par point et découvert un groupe distinct de points qui s’alignait précisément sur l’IM, séparant le centre nécrotique des zones de foie normal et de tumeur.
Les cellules immunitaires affluent — mais beaucoup freinent l’attaque
Les scientifiques ont ensuite utilisé le séquençage ARN mono‑cellule et mono‑noyau, ainsi qu’une puissante méthode de profilage nommée CyTOF, pour inventorier les types cellulaires individuels à travers le foie. Ils ont constaté que l’IM est dominée par un type de cellule immunitaire appelé macrophages. En particulier, un sous‑ensemble ressemblant à des « macrophages associés aux lipides » (LAM) a envahi l’IM en quelques jours après l’IRE. Ces cellules présentent des marqueurs de surface et des signatures géniques associés à l’immunosuppression, notamment des niveaux élevés de PD‑L1, une molécule connue pour atténuer les réponses des lymphocytes T. Les analyses d’expression génique suggèrent que ces macrophages sont performants pour engloutir du matériel, répondre aux signaux chimiotactiques et émettre des signaux capables de restreindre les lymphocytes T nécessaires pour éliminer les cellules cancéreuses. L’imagerie a confirmé que les macrophages PD‑L1‑positifs étaient bien plus abondants dans l’IM que dans le tissu normal adjacent.
Un point chaud de chimie lipidique altérée
Ensuite, l’équipe a superposé ce paysage immunitaire avec la métabolomique spatiale, une approche d’imagerie par spectrométrie de masse qui cartographie la distribution de centaines de petites molécules. Ils ont montré que l’IM possède une empreinte métabolique distincte ni comparable au noyau nécrotique ni au foie environnant. Dans cette bande étroite, de nombreuses voies lipidiques étaient fortement stimulées, y compris la production d’acides gras insaturés, de dérivés de l’acide arachidonique et de sphingolipides. Des lipides de signalisation clés tels que les prostaglandines et les leucotriènes, dérivés de l’acide arachidonique, étaient enrichis dans l’IM, tandis que d’autres voies enzymatiques traitant la même molécule étaient relativement atténuées. Une autre famille lipidique, les sphingolipides — incluant céramides et sphingomyélines — s’accumulait également, soutenue par une expression accrue des enzymes qui les synthétisent et les remodelent.
Une transition progressive du dommage vers une niche riche en carburant
En subdivisant la marge inflammatoire en trois couches minces du centre nécrotique vers l’extérieur, les chercheurs ont observé un glissement graduel de la chimie. Près de la zone nécrotique, les lipides complexes et les molécules liées au cholestérol étaient les plus abondants, tandis qu’à mesure que l’on s’éloignait, de petites molécules liées à l’énergie telles que le glucose et certains acides aminés augmentaient. Ce schéma suggère qu’en quelques millimètres, le tissu passe d’un environnement chargé en lipides et riche en signaux à un milieu orienté vers l’alimentation en énergie et la survie cellulaire. Les auteurs proposent que cette reprogrammation progressive aide à soutenir les macrophages immunosuppresseurs, affamés en lipides, qui dominent l’IM et pourraient discrètement préparer le terrain pour que les cellules tumorales se réinstallent.
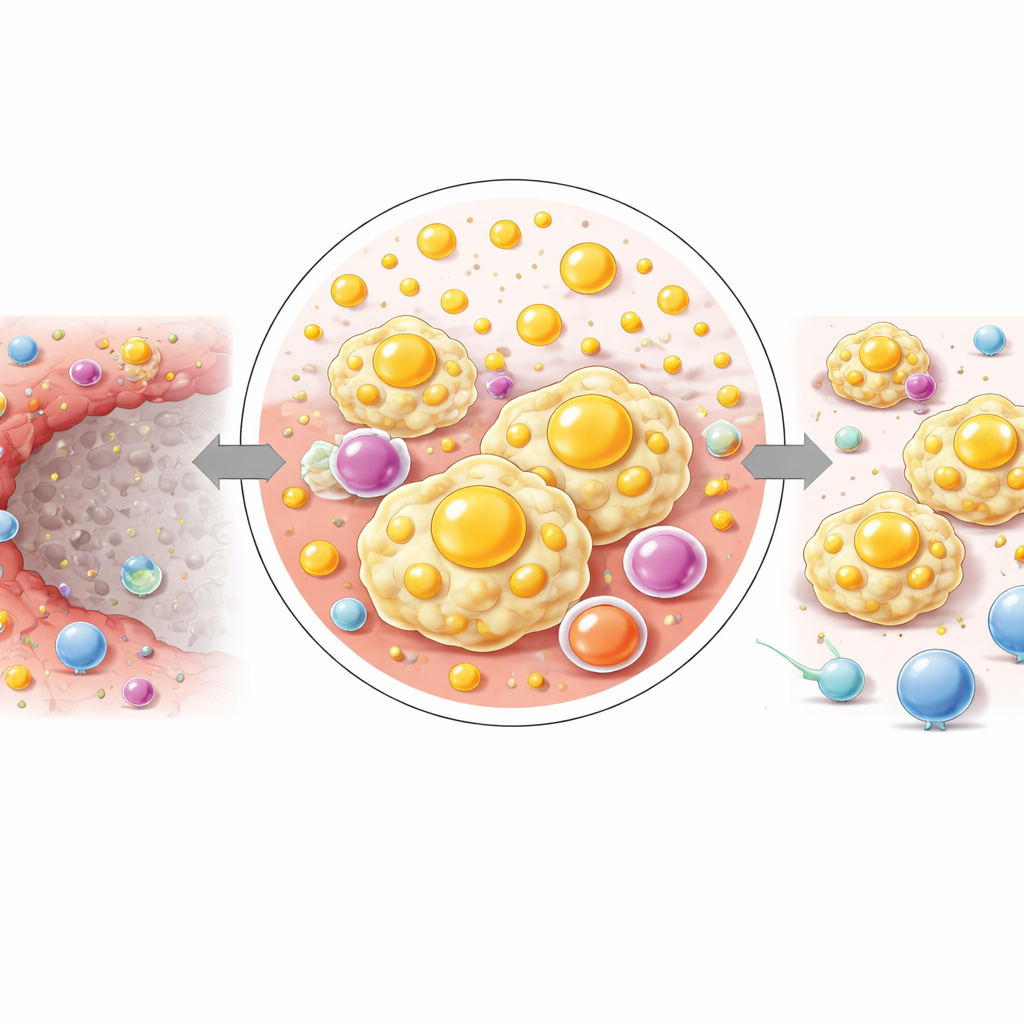
Ce que cela signifie pour les soins futurs du cancer du foie
En termes simples, ce travail montre que l’IRE fait plus que tuer des cellules tumorales : elle crée aussi un anneau étroit de tissu où cellules immunitaires et chimie lipidique forment ensemble un quartier protégé et favorable à la tumeur. Les macrophages dans cette zone sont abondants, chargés en lipides et orientés vers l’extinction des lymphocytes T plutôt que leur activation. Parce que ces changements sont étroitement liés à des voies métaboliques spécifiques, ils suggèrent de nouveaux angles thérapeutiques. Combiner l’IRE avec des médicaments ciblant le métabolisme lipidique ou bloquant PD‑L1 dans cette marge pourrait, en principe, transformer une bordure sujette aux récidives en une zone qui achève réellement l’élimination du cancer du foie.
Citation: Liu, J., Guan, S., Sun, Z. et al. Spatial multiomics reveals irreversible electroporation-induced immuno-metabolic characteristics of the inflammatory margin in liver cancer. Commun Biol 9, 458 (2026). https://doi.org/10.1038/s42003-026-09742-4
Mots-clés: cancer du foie, ablation tumorale, microenvironnement immunitaire, macrophages, métabolisme des lipides