Clear Sky Science · fr
Quantification ultrarapide et spécifique des microARN par cinétique d’extinction de fluorescence au niveau d’une seule molécule
Pourquoi des tests rapides sont essentiels
Diagnostiquer des maladies comme le cancer ou des infections virales revient souvent à repérer de minuscules traces de matériel génétique dans le sang ou d’autres fluides corporels. Les tests de référence actuels peuvent être très précis mais sont parfois lents, coûteux ou ont du mal à détecter des signaux très rares. Cette étude présente une nouvelle méthode basée sur le microscope, appelée Q‑FISH, capable de lire ces indices génétiques en moins d’une seconde. Si elle est adaptée aux outils cliniques, une telle rapidité et précision pourrait faciliter la détection précoce des maladies, suivre l’efficacité des traitements et personnaliser les soins pour chaque patient.
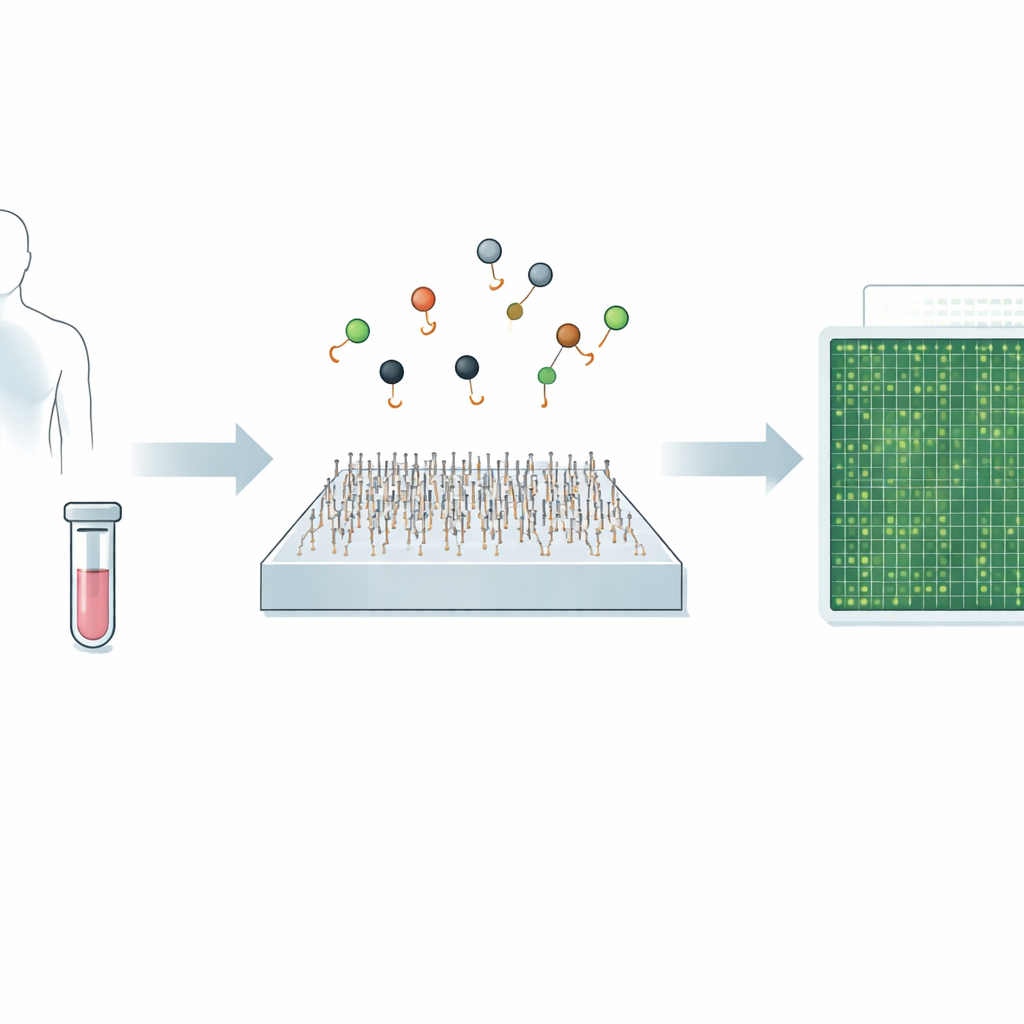
Une nouvelle façon de voir de minuscules messages génétiques
Les travaux se concentrent sur les microARN — de courts fragments d’ARN qui régulent l’utilisation de nos gènes et qui sont fortement liés à de nombreux cancers, maladies cardiaques, infections et troubles cérébraux. Parce que les microARN sont très courts et diffèrent souvent d’un ou deux nucléotides seulement, les méthodes standards comme la PCR et le séquençage de nouvelle génération ont parfois du mal à distinguer des types très proches, surtout lorsque leur abondance est très faible. Des approches récentes d’imagerie monoclonale ont amélioré cette spécificité en suivant l’association et la dissociation de sondes individuelles, mais elles restaient relativement lentes, nécessitant environ dix minutes pour analyser une seule cible.
Observer des scintillements lumineux pour trouver la bonne cible
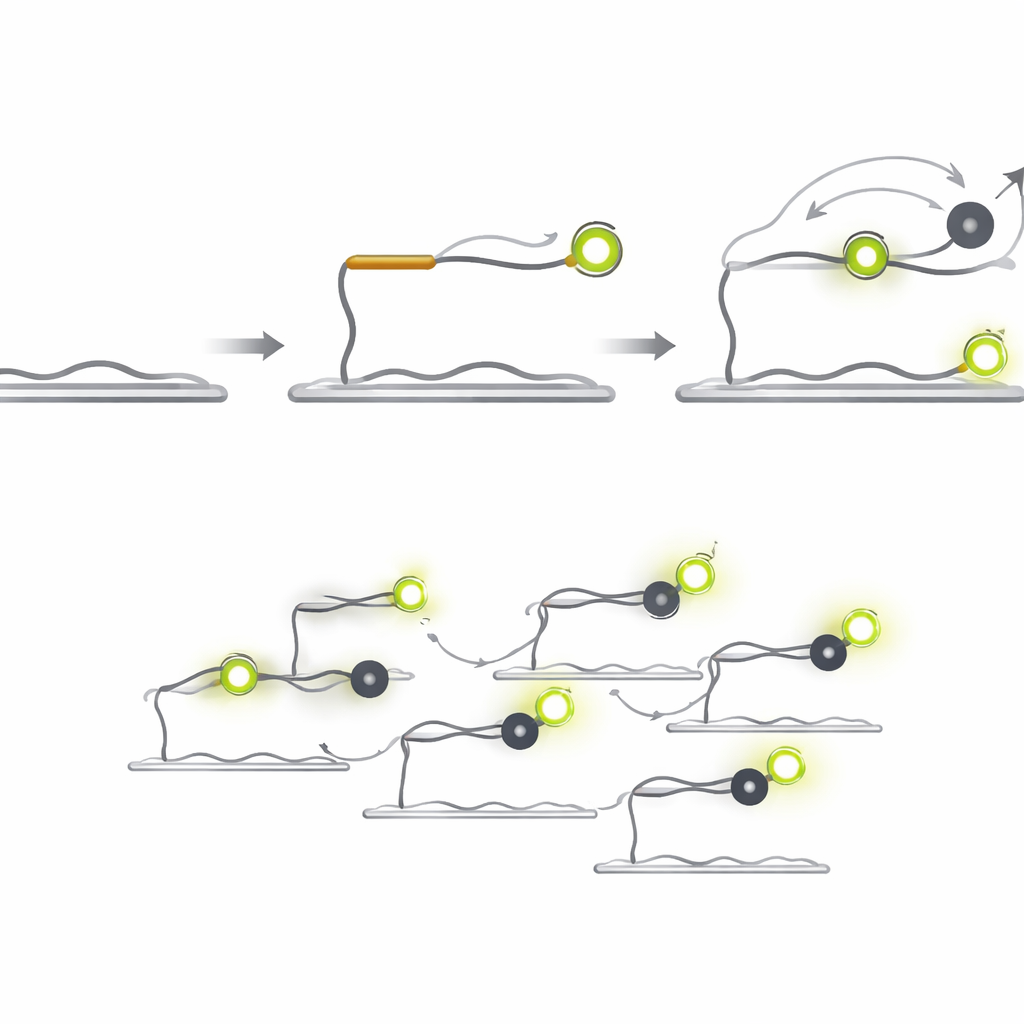
Q‑FISH renverse la problématique en exploitant les brefs scintillements de la fluorescence émise par des molécules uniques. La méthode utilise deux courtes sondes d’ADN qui reconnaissent des emplacements voisins sur un microARN cible. Une sonde porte un colorant fluorescent qui brille sous laser, tandis que l’autre porte un « éteignoir » (quencher) qui absorbe la lumière lorsqu’il se rapproche. La sonde fluorescente se fixe sur la cible et reste suffisamment longtemps pour être détectée, tandis que la sonde quencher est conçue pour se fixer puis se détacher très rapidement. Chaque fois que le quencher se place à côté du colorant, la lumière chute soudainement ; lorsqu’il s’en va, la lumière remonte instantanément. En enregistrant ces flashes d’allumage/extinction rapides issus de molécules individuelles et en analysant la durée des périodes lumineuses et sombres, le système peut déterminer si une vraie cible est présente.
Des minutes aux millisecondes
Parce que la sonde quencher n’émet pas sa propre lumière, elle peut être utilisée à des concentrations bien plus élevées que les sondes fluorescentes sans créer d’éblouissement de fond. Raccourcir la sonde quencher augmente sa vitesse de dissociation, et augmenter sa concentration accroît la fréquence de ses collisions. Ensemble, ces choix de conception conduisent à un bond spectaculaire en vitesse. Dans des tests sur un microARN lié au cancer appelé let‑7a, Q‑FISH a atteint plus de 70 % de son efficacité maximale de détection en seulement une seconde d’observation. Les méthodes monoclonales comparables nécessitaient des dizaines à des centaines de secondes pour obtenir des performances similaires, rendant Q‑FISH plus de 600 fois plus rapide en pratique.
Classer des signaux presque identiques et mesurer des échantillons réels
Les chercheurs ont également démontré que Q‑FISH peut distinguer plusieurs membres de la famille let‑7 de microARN, qui partagent presque la même séquence mais jouent des rôles différents dans la régulation de gènes liés au cancer. Ils ont utilisé deux stratégies de multiplexage. Dans l’une, différentes sondes quencher ont été introduites les unes après les autres, chacune ajustée à un microARN légèrement différent ; dans l’autre, les sondes étaient marquées de couleurs différentes et imagées simultanément. Dans les deux cas, l’analyse des motifs de clignotement a permis à l’équipe d’identifier correctement chaque microARN en environ une seconde. Enfin, ils ont appliqué la méthode à l’ARN total extrait de tissus humains de foie et de poumon. En ajoutant des quantités connues de microARN synthétiques et en comptant les points résultants, ils ont construit des courbes d’étalonnage puis déterminé les niveaux naturels présents dans les tissus, révélant des différences nettes entre organes.
Ce que cela pourrait signifier pour les tests à venir
Dans l’ensemble, l’étude montre que Q‑FISH peut repérer des microARN spécifiques avec une très grande précision, même lorsqu’ils sont presque identiques les uns aux autres, et ce à des vitesses qui surpassent largement les méthodes monoclonales antérieures. Bien que les expériences aient été réalisées sur des échantillons préparés à l’aide d’un microscope spécialisé, l’idée sous-jacente — utiliser des événements rapides d’extinction de fluorescence plutôt que la simple association lente — pourrait être adaptée à de nombreux types de biomarqueurs génétiques, y compris des fragments d’ADN tumoral dans le sang. Avec des améliorations d’ingénierie et une préparation d’échantillons simplifiée, cette approche pourrait contribuer à rapprocher des diagnostics moléculaires rapides, hautement multiplexés et extrêmement sensibles de l’usage clinique courant.
Citation: Kim, J., Hohng, S. Ultrafast and specific miRNA quantification via single-molecule fluorescence quenching kinetics. Commun Biol 9, 432 (2026). https://doi.org/10.1038/s42003-026-09714-8
Mots-clés: détection de microARN, imagerie monoclonale, diagnostic moléculaire, extinction de fluorescence, biopsie liquide