Clear Sky Science · fr
Une stratégie en deux étapes médiée par l’actine permet à Campylobacter jejuni de favoriser l’agrégation mitochondriale et l’homéostasie du fer pour la survie intracellulaire et la persistance
Pourquoi ce petit combat à l’intérieur des cellules compte
L’intoxication alimentaire due au poulet insuffisamment cuit est souvent imputée à une bactérie nommée Campylobacter jejuni. La plupart des personnes récupèrent, mais ce microbe sait étonnamment bien survivre dans de nombreux environnements, ce qui facilite sa diffusion de la ferme à l’assiette. Cette étude examine ce qui se passe lorsque la bactérie se cache à l’intérieur d’une amibe libre — un microbe d’eau douce commun — et révèle un tour de survie étonnamment sophistiqué centré sur la reconfiguration du squelette interne de la cellule, le regroupement des « batteries » productrices d’énergie appelées mitochondries, et le contrôle du fer et de la chimie oxygénée nuisible. Comprendre cette phase cachée de son cycle de vie pourrait indiquer de nouvelles voies pour réduire la contamination avant que la bactérie n’atteigne les humains.
Un microbe qui s’entraîne dans les amibes
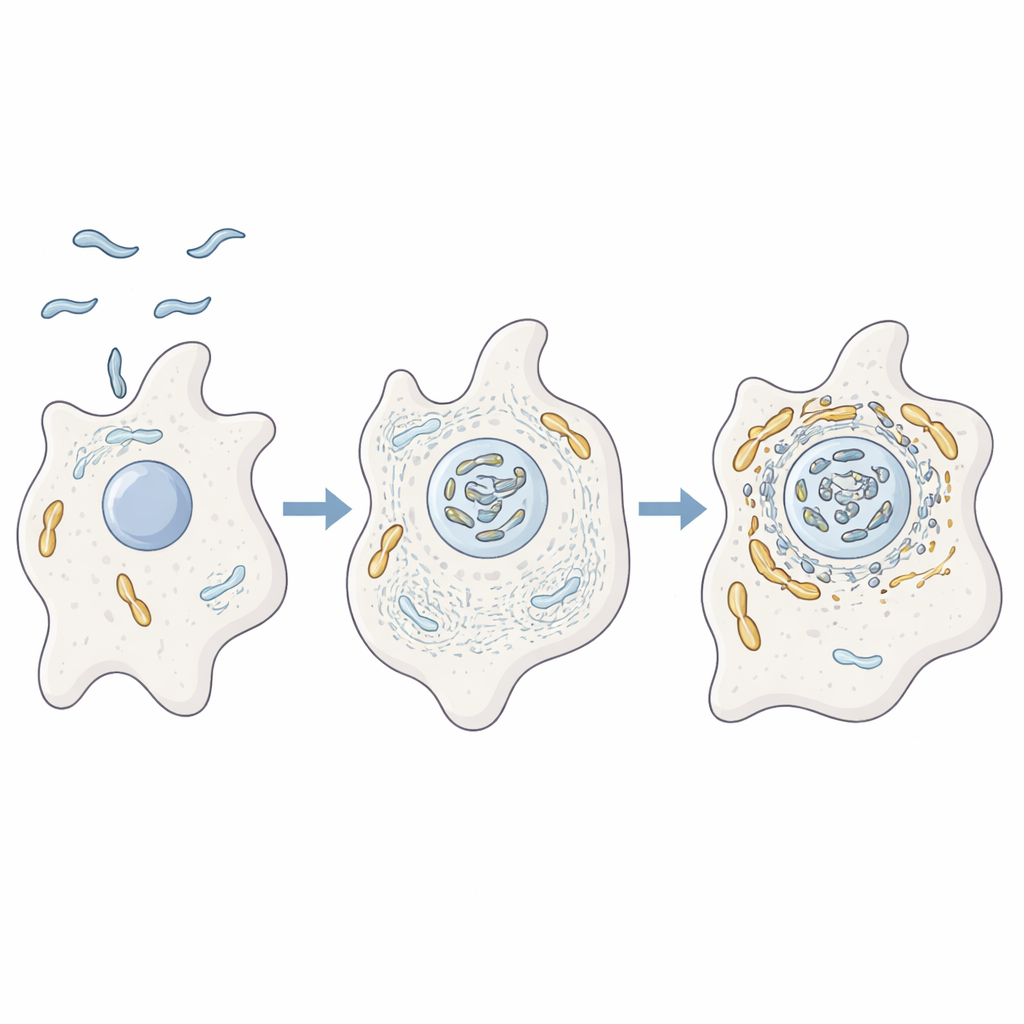
Les auteurs ont étudié le comportement de C. jejuni à l’intérieur de l’amibe Acanthamoeba castellanii, un organisme unicellulaire vivant dans le sol et l’eau. Ces amibes servent de terrains d’entraînement pour de nombreuses bactéries pathogènes, offrant protection contre des conditions défavorables et contre les désinfectants. Grâce à des analyses protéiques avancées, la microscopie et des mutants génétiques, les chercheurs ont montré que lorsque C. jejuni infecte des amibes, elle se retrouve étroitement associée aux mitochondries de l’hôte. Parallèlement, l’échafaudage interne de l’amibe constitué d’actine, ainsi que des protéines qui régulent sa forme et ses mouvements, sont fortement enrichis près de ces mitochondries, ce qui suggère que la bactérie réorganise activement l’architecture interne de la cellule hôte.
Plier le squelette cellulaire pour déplacer les batteries
Pour vérifier si l’actine pilote réellement cette interaction, l’équipe a bloqué la formation de filaments d’actine ou leur ramification en réseaux. Dans ces conditions, les mitochondries ne se rassemblaient plus près des bactéries et restaient réparties en points épars, et la survie de la bactérie chutait. Ils se sont ensuite concentrés sur deux protéines bactériennes auxiliaires, CiaD et CiaI, qui sont injectées dans les cellules hôtes via le flagelle de la bactérie, une sorte de queue fouetteuse. CiaD s’est avérée stimuler la croissance de l’actine et favoriser des projections épineuses à la surface de l’amibe, aidant la cellule à engloutir la bactérie. Une fois à l’intérieur, les mitochondries ont été observées en grappes autour du compartiment bactérien de manière dépendante de l’actine, plaçant la bactérie dans une zone privilégiée riche en machinerie énergétique de l’hôte.
Un interrupteur moléculaire qui remodèle les mitochondries
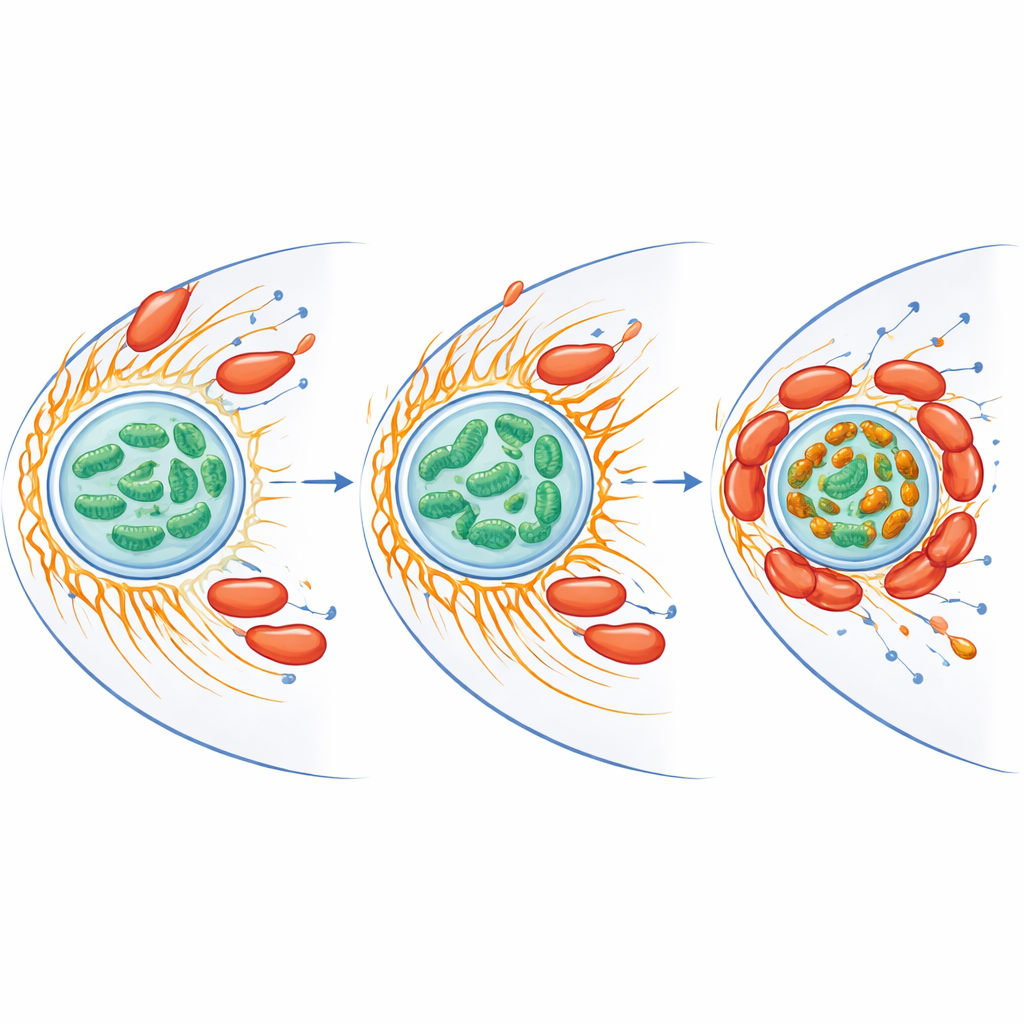
Tandis que CiaD est clé pour l’entrée, CiaI contrôle ce qui se passe ensuite. Lorsque les chercheurs ont supprimé le gène codant CiaI, C. jejuni n’induisait plus de fort regroupement mitochondrial et survivait moins bien à l’intérieur des amibes. L’ajout de CiaI purifiée liée à de minuscules billes, sans aucune bactérie vivante, suffisait à provoquer la fusion et l’agrégation des mitochondries à proximité et à éliminer localement l’actine. Des tests biochimiques ont montré que CiaI se lie aux molécules porteuses d’énergie de façon coopérative, se comportant comme un interrupteur moléculaire susceptible d’activer ou d’inhiber son activité selon les conditions à l’intérieur de l’hôte. Les auteurs proposent qu’après la croissance d’actine induite par CiaD qui rapproche les mitochondries, CiaI provoque la dégradation locale de l’actine et remodèle le réseau mitochondrial en agrégats denses entourant le compartiment contenant la bactérie.
Reconfigurer le fer et le stress à l’intérieur de la cellule hôte
Les mitochondries font plus que produire de l’énergie — elles gèrent aussi le fer et produisent des espèces réactives de l’oxygène, des formes oxygénées chimiquement agressives qui peuvent tuer les microbes. Les chercheurs ont constaté que l’infection réduisait le fer libre global à l’intérieur des mitochondries mais, en même temps, créait des grappes brillantes riches en fer là où les mitochondries s’agrégeaient autour des bactéries. Les protéines impliquées dans la gestion du fer et dans la défense contre le stress oxydatif augmentaient à la fois chez l’hôte et chez la bactérie. Lorsque l’équipe a éliminé le fer libre à l’aide d’un chélateur, l’explosion d’espèces réactives de l’oxygène de l’amibe a diminué et la survie de C. jejuni a augmenté de manière spectaculaire. Les mitochondries des cellules infectées présentaient également un potentiel de membrane plus élevé, signe d’une activité accrue, ce qui suggère que la bactérie pousse les « batteries » de l’hôte dans un état favorisant sa propre persistance tout en limitant la chimie oxygénée dommageable.
Ce que cela signifie pour la sécurité alimentaire et l’infection
Dans l’ensemble, les résultats soutiennent une stratégie en deux étapes : d’abord, CiaD stimule la croissance de l’actine pour aider la bactérie à pénétrer dans les amibes et attirer les mitochondries vers le site d’entrée ; ensuite, CiaI démantèle localement l’actine et remodèle les mitochondries en grappes riches en fer enveloppant le compartiment bactérien, tout en atténuant les défenses oxydatives de l’hôte. Ce contrôle fin de la forme cellulaire, de l’utilisation de l’énergie et de l’équilibre des métaux aide C. jejuni à survivre à l’intérieur des amibes et contribue probablement à sa capacité à persister dans l’environnement puis à infecter les humains. En révélant les acteurs clés de cette lutte microscopique, l’étude met en lumière de nouvelles cibles — telles que les protéines Cia, les contacts actine‑mitochondries ou les voies de gestion du fer — qui pourraient être perturbées pour réduire la contamination et la maladie.
Citation: Nasher, F., Wren, B.W. A two-step actin-mediated strategy enables Campylobacter jejuni to promote mitochondrial aggregation and iron homeostasis, for intracellular survival and persistence. Commun Biol 9, 431 (2026). https://doi.org/10.1038/s42003-026-09713-9
Mots-clés: Campylobacter, amibes, mitochondries, cytosquelette d’actine, homéostasie du fer