Clear Sky Science · fr
Régulation multicouche des récepteurs kainate GluK3 médiée par les sous‑unités Neto et le zinc
Pourquoi des interrupteurs microscopiques comptent
Chaque pensée, souvenir et humeur dans le cerveau dépend d’interrupteurs microscopiques qui laissent passer des particules chargées à l’intérieur et à l’extérieur des cellules nerveuses. Cette étude se concentre sur l’un de ces interrupteurs, un récepteur peu connu nommé GluK3. En dévoilant comment des protéines partenaires et des ions zinc ajustent finement le comportement de GluK3, le travail fournit des clés pour comprendre comment les circuits cérébraux restent en équilibre — et comment cet équilibre peut basculer dans des troubles tels que l’épilepsie, la dépression et la schizophrénie.
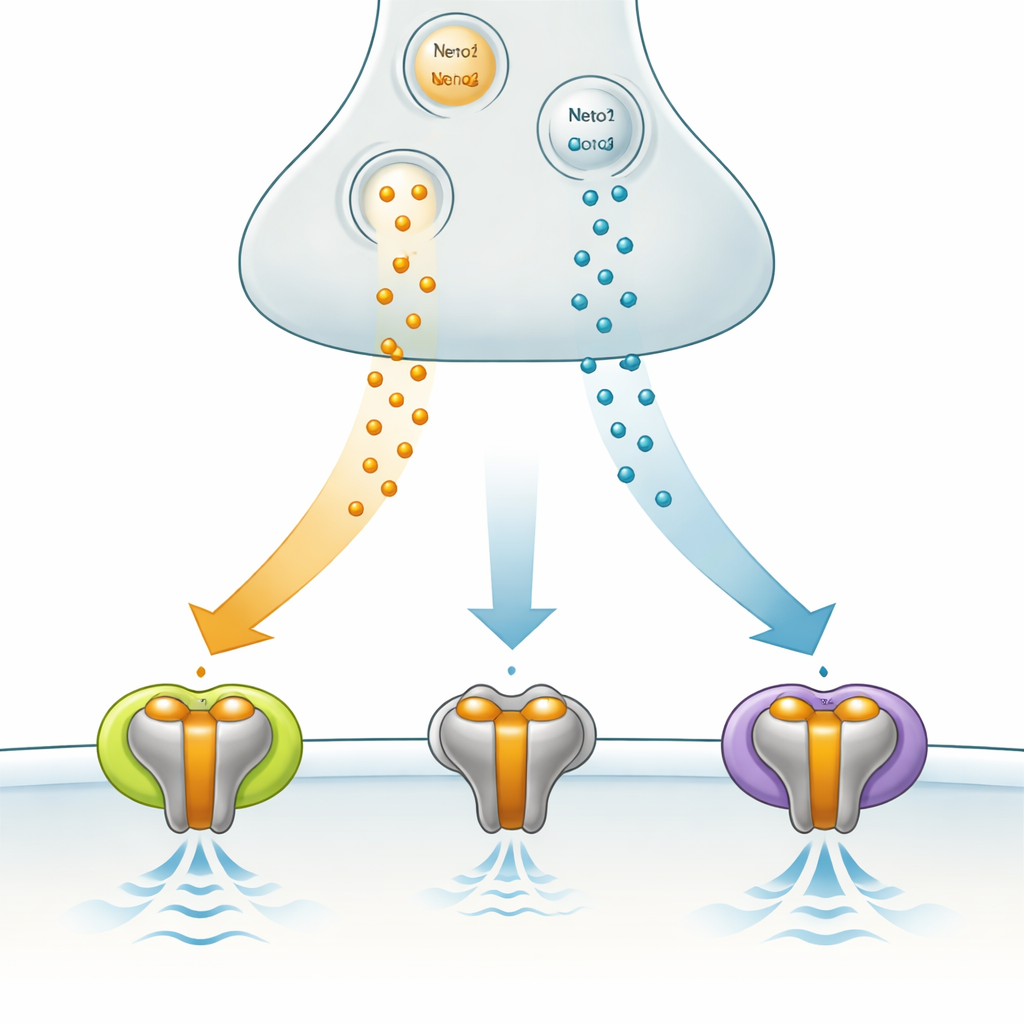
Une porte de signalisation spécialisée dans le cerveau
GluK3 appartient à la famille des récepteurs kainate, qui fait partie du groupe plus large des récepteurs au glutamate assurant la communication rapide entre neurones. Contrairement à certains de ses cousins, GluK3 ne se contente pas d’allumer ou d’éteindre les signaux ; il agit plutôt comme un filtre qui répond le mieux aux rafales brèves et intenses du messager chimique glutamate. Il est enrichi dans des régions cérébrales telles que l’hippocampe, crucial pour la mémoire et la structuration des rythmes du réseau, et des altérations de la fonction de GluK3 ont été liées à des comportements associés à l’anxiété. Ces caractéristiques font de GluK3 une cible prometteuse, mais encore mal comprise, pour moduler l’activité cérébrale en santé et en pathologie.
Protéines auxiliaires qui tirent les ficelles
L’équipe a étudié comment deux protéines auxiliaires, Neto1 et Neto2, modifient le comportement de GluK3 dans des cellules humaines génétiquement modifiées pour produire ces composants. Les deux auxiliaires ralentissaient la vitesse à laquelle GluK3 se ferme après activation, et diminuaient une forme intrinsèque d’obstruction interne qui limite normalement le flux de courant. Cependant, ils ont des effets opposés sur la rapidité de réutilisation du récepteur. Avec Neto1, les récepteurs se rétablissaient rapidement, prêts à répondre à des signaux rapides et répétés. Avec Neto2, la récupération devenait beaucoup plus lente, favorisant l’intégration des signaux sur des intervalles plus longs. En substance, en choisissant différentes protéines auxiliaires, une synapse peut décider si GluK3 se comporte comme un détecteur à tir rapide ou comme un capteur plus lent faisant la moyenne des signaux.
Le zinc comme second niveau de contrôle
Beux nombreux terminaisons libérant du glutamate libèrent également du zinc, qui peut se lier aux récepteurs et modifier leur fonctionnement. Des travaux antérieurs ont montré que le zinc augmente de façon inhabituelle l’activité de GluK3, tandis qu’il tend à atténuer d’autres types de récepteurs. Ici, les auteurs ont constaté que cette augmentation dépend fortement de la présence de la protéine Neto. Lorsque GluK3 est isolé, le zinc double approximativement le temps pendant lequel le récepteur reste actif et augmente modestement le courant. L’ajout de Neto1 atténue cet effet. En revanche, lorsque GluK3 s’associe à Neto2, zinc et Neto2 agissent en synergie pour amplifier fortement le courant, bien plus que chacun ne le ferait seul. Cela suggère que les synapses riches en Neto2 et en zinc peuvent fortement amplifier les signaux médiés par GluK3 lors d’activités intenses, tandis que les synapses riches en Neto1 restent plus contenues.
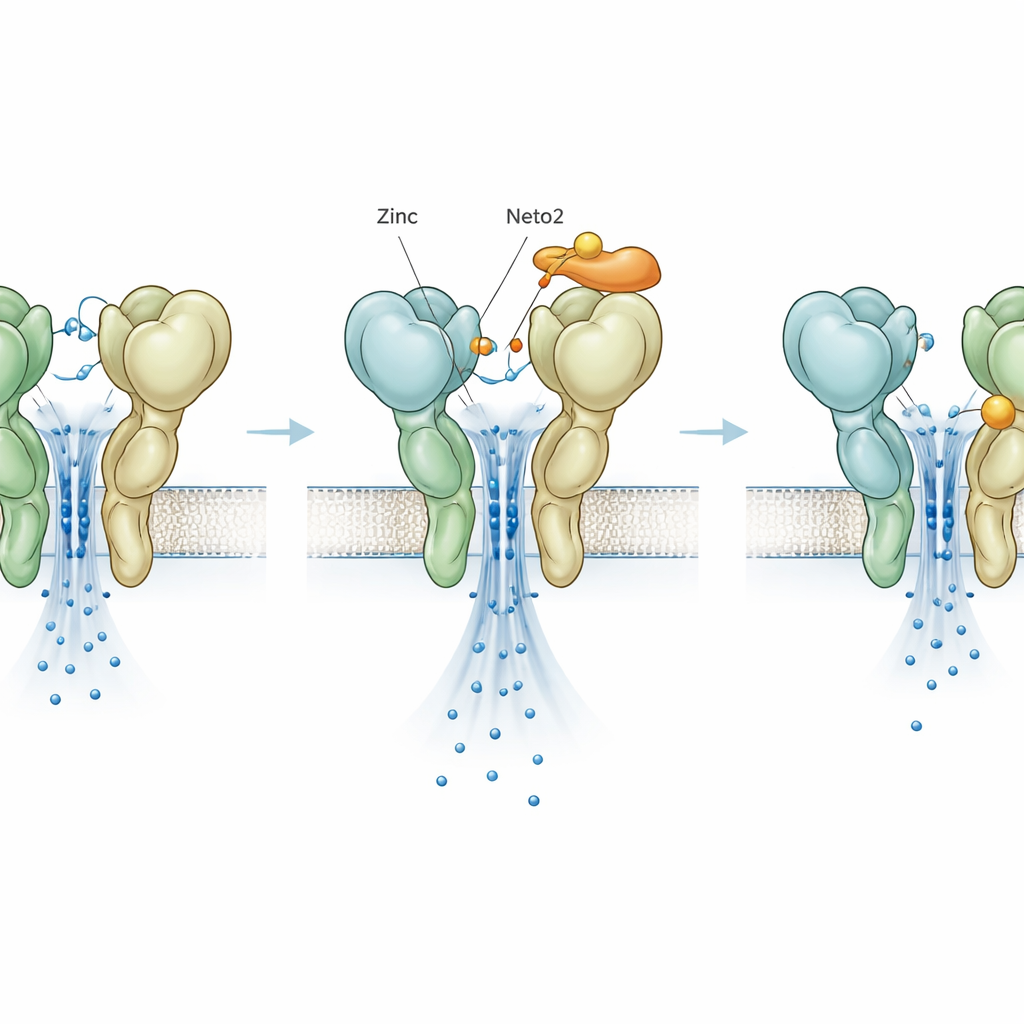
Un frein caché révélé par une mutation
Pour séparer les actions du zinc de celles des protéines auxiliaires, les chercheurs ont introduit une modification d’une seule lettre dans GluK3, appelée D759G, qui supprime un site de liaison au zinc connu. Comme prévu, cette mutation rendait le récepteur plus stable et plus lent à se fermer, imitant l’effet habituel du zinc. De façon surprenante, lorsque le zinc était ajouté à ce mutant, il n’augmentait plus l’activité ; au contraire, il accélèrait la fermeture et réduisait le courant, révélant un second site de zinc auparavant caché qui agit comme un frein. Neto1 et Neto2 exerçaient toujours leurs effets caractéristiques sur le mutant, montrant que leur influence principale ne dépend pas du site de zinc original. Pourtant, même cette action inhibitrice de zinc nouvellement découverte était modulée différemment par les deux auxiliaires, ajoutant un autre réglage ajustable au système.
Voir la structure derrière le comportement
Pour relier fonction et forme, l’équipe a utilisé la cryo‑microscopie électronique pour visualiser le récepteur GluK3 mutant figé dans un état non actif. Les images ont révélé que la région qui lie le glutamate forme une unité plus compacte et densément empaquetée dans le mutant D759G comparée au GluK3 normal. Ce resserrement structurel rend probablement plus difficile pour le récepteur de basculer vers une conformation d’arrêt, ce qui explique pourquoi le mutant, à l’instar de GluK3 lié au zinc, reste actif plus longtemps. En même temps, les images ont montré que toutes les parties du récepteur n’étaient pas verrouillées dans une seule configuration, indiquant une architecture intrinsèquement flexible particulièrement sensible aux petites sollicitations chimiques.
Ce que cela signifie pour la santé cérébrale
Pris ensemble, les résultats décrivent GluK3 non pas comme un simple interrupteur marche–arrêt mais comme un centre finement réglable où convergent le glutamate, les protéines auxiliaires et le zinc. Neto1 et Neto2 déterminent la vitesse d’atténuation des signaux et la rapidité de la réactivité des récepteurs, tandis que le zinc peut soit augmenter encore l’activité soit, dans certaines conditions, la restreindre via plusieurs sites de liaison. Parce que GluK3, les protéines Neto et le zinc coexistent aux synapses impliquées dans la mémoire et sont impliqués dans l’épilepsie et des troubles psychiatriques, la compréhension de ce contrôle multicouche pourrait orienter des thérapies futures visant à réajuster en douceur la signalisation synaptique plutôt qu’à l’interrompre complètement.
Citation: Vinnakota, R., Dawath, B.K., Assaiya, A. et al. Multilayered regulation of GluK3 kainate receptors is mediated by Neto subunits and zinc. Commun Biol 9, 420 (2026). https://doi.org/10.1038/s42003-026-09707-7
Mots-clés: récepteurs kainate, GluK3, protéines Neto, zinc synaptique, plasticité synaptique