Clear Sky Science · fr
Abus de drogues addictives et dépression — un focus sur l’épigénétique
Pourquoi cette recherche importe dans la vie quotidienne
Les drogues addictives et la dépression sont souvent traitées comme des problèmes distincts, mais elles apparaissent fréquemment ensemble chez une même personne. Cette revue explique comment l’usage prolongé de substances telles que la méthamphétamine, la cocaïne, les opioïdes et le cannabis peut laisser des « cicatrices moléculaires » durables dans le cerveau qui augmentent le risque de dépression. En mettant au jour ces changements cachés, l’article ouvre la voie à de futurs tests capables d’identifier les personnes les plus vulnérables — et à des traitements plus précis susceptibles d’inverser les dommages plutôt que de simplement masquer les symptômes.
Comment l’addiction et le mauvais moral s’entremêlent
Les auteurs commencent par décrire le lien clinique étroit entre l’abus de drogues et la dépression. Les personnes qui consomment de façon répétée des substances addictives sont beaucoup plus susceptibles de déclarer une tristesse persistante, une perte de plaisir, des troubles du sommeil et des idées suicidaires. Les régions cérébrales qui contrôlent la récompense, la motivation, la mémoire et la prise de décision — la zone tegmentale ventrale, le noyau accumbens, le cortex préfrontal et l’hippocampe — sont centrales pour les deux affections. L’exposition chronique aux drogues perturbe des neurotransmetteurs comme la dopamine et la sérotonine, les hormones du stress régulées par l’axe hypothalamo-hypophyso-surrénalien, les signaux immunitaires et l’approvisionnement énergétique des neurones. Ensemble, ces modifications rendent le cerveau moins résilient au stress et plus susceptible aux états dépressifs, y compris longtemps après la dernière prise.
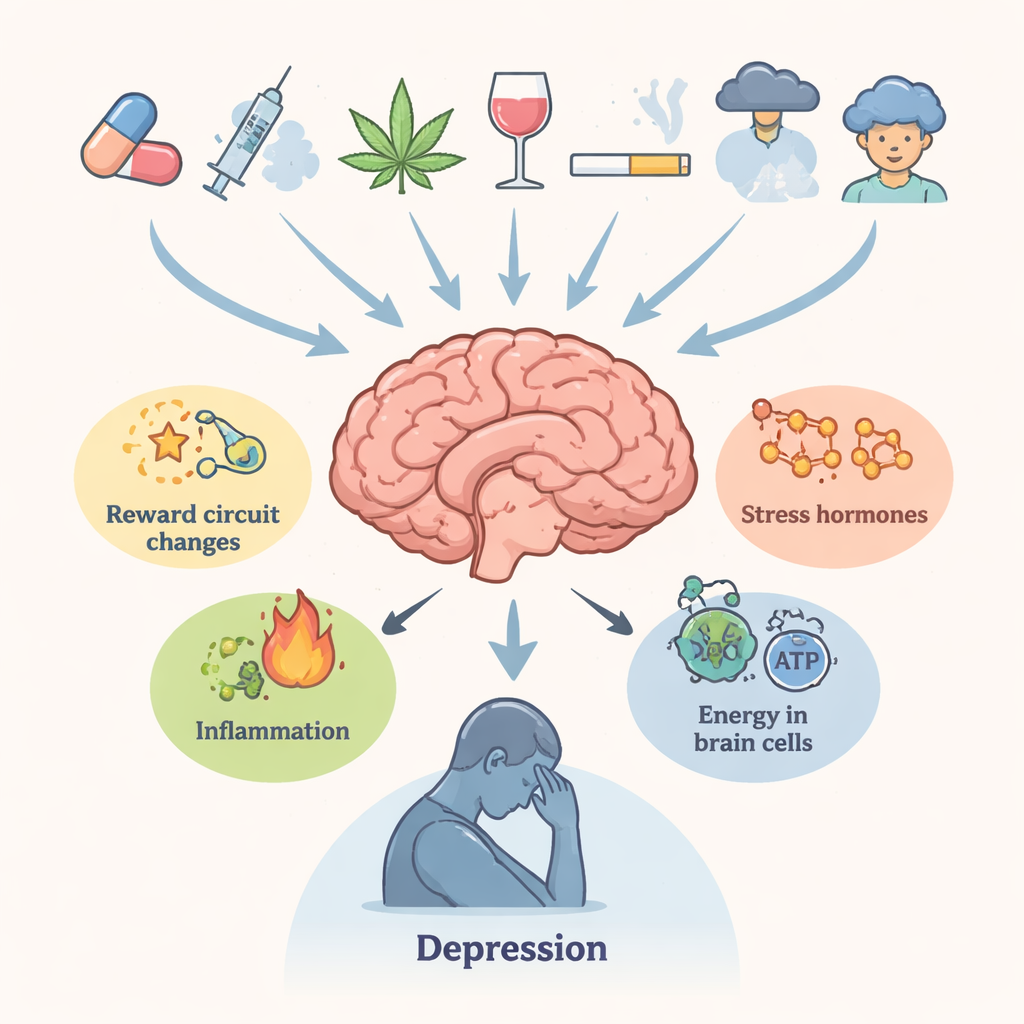
Des drogues qui reconfigurent la chimie cérébrale
La revue passe en revue plusieurs grandes classes de drogues. Les stimulants de type amphétamine et leurs apparentés, y compris les « sels de bain » synthétiques, provoquent des poussées puissantes de dopamine et d’autres transmetteurs qui, avec le temps, endommagent les terminaisons nerveuses, perturbent l’équilibre du glutamate, mettent à rude épreuve le réticulum endoplasmique et poussent les cellules vers une autophagie délétère. L’usage du cannabis à l’adolescence est associé à un risque ultérieur de dépression et de suicide, probablement via des changements durables des récepteurs cannabinoïdes, de la structure de la substance blanche et de la sensibilité des circuits dopaminergiques. Les opioïdes, tout en soulageant la douleur, peuvent déclencher une inflammation, une défaillance mitochondriale et une diminution des signaux favorisant la croissance comme le facteur neurotrophique dérivé du cerveau (BDNF). La cocaïne active de façon répétée le système de stress et modifie des régulateurs clés tels que FKBP5, contribuant à l’anxiété et au mauvais moral lors du sevrage. Dans chaque cas, les perturbations biologiques tendent à persister, ce qui aide à expliquer pourquoi les symptômes émotionnels peuvent durer au-delà de l’intoxication apparente.
Épigénétique : la mémoire de l’exposition
Pour comprendre pourquoi les effets des drogues perdurent, les auteurs se concentrent sur l’épigénétique — des balises chimiques et des interrupteurs moléculaires qui modulent l’activité des gènes sans altérer les lettres de l’ADN. Les drogues addictives modifient la méthylation de l’ADN (une marque sur les bases cytosine), changent les groupes chimiques sur les protéines histones qui emballent l’ADN et altèrent les ARN non codants qui ajustent finement la production des protéines. Par exemple, la méthamphétamine et la cocaïne déplacent les schémas de méthylation dans les régions liées à la récompense, modifiant les niveaux d’enzymes qui ajoutent ou retirent ces marques. Les opioïdes et les stimulants remodèlent l’acétylation et la méthylation des histones sur des gènes contrôlant les récepteurs du glutamate, la signalisation du stress et la structure synaptique. Des dizaines de microARN, d’ARN longs non codants et d’ARN circulaires augmentent ou diminuent avec l’exposition aux drogues, influençant collectivement l’inflammation, la croissance neuronale et la force des synapses. Ces changements épigénétiques agissent comme une « mémoire » moléculaire de l’histoire de consommation.
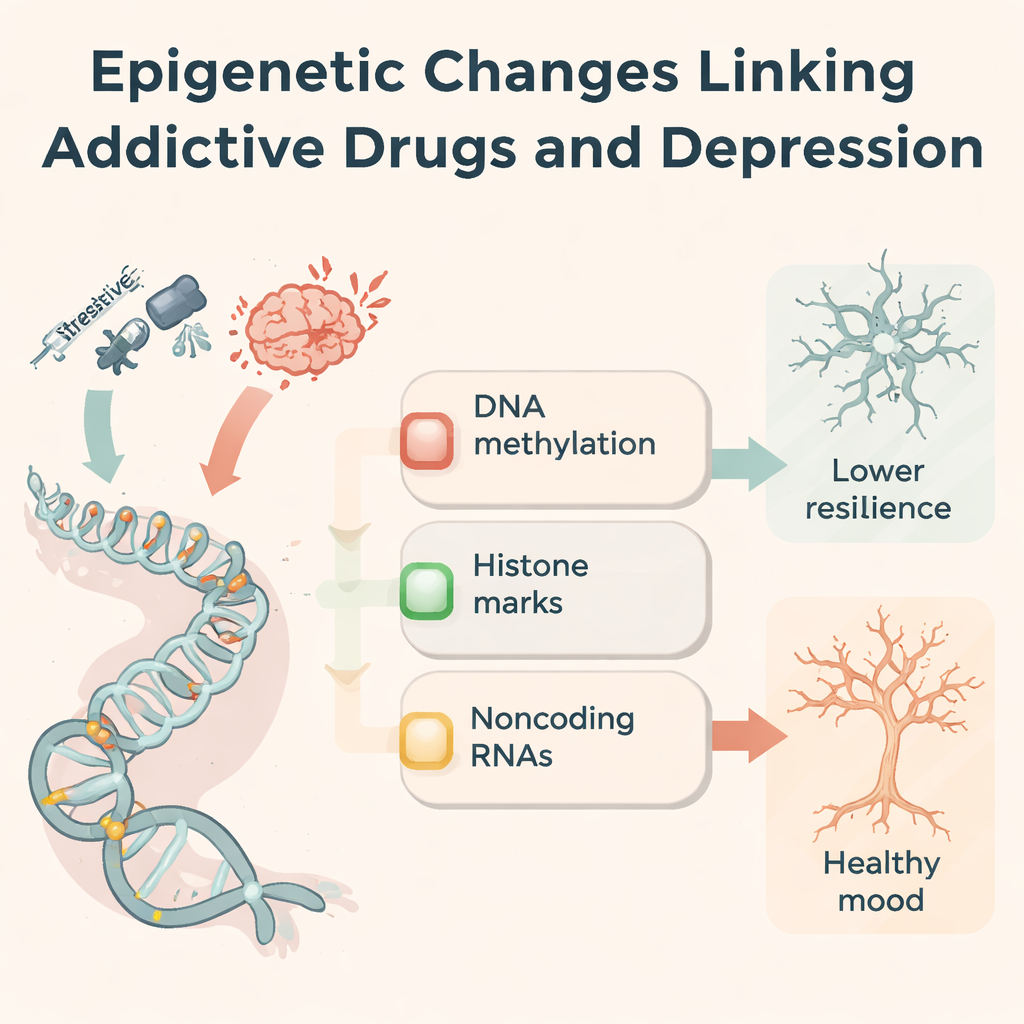
Voies moléculaires partagées dans la dépression et l’addiction
La même machinerie épigénétique apparaît également chez des personnes et des animaux souffrant de dépression qui n’ont jamais consommé de drogues. Des expériences stressantes peuvent modifier la méthylation des récepteurs des hormones du stress (comme NR3C1 et FKBP5), réduire des facteurs de croissance utiles tels que le BDNF et reconfigurer les voies immunitaires et du glutamate. Beaucoup des mêmes ARN non codants modifiés par les drogues sont aussi déréglés dans la dépression, affectant la naissance de nouveaux neurones, la réponse des microglies à l’inflammation et la force des connexions synaptiques. Les auteurs proposent un cadre en trois volets : la régulation de la réponse au stress, le remodelage des circuits de la récompense et la plasticité synaptique. À travers ces axes, addiction et dépression convergent à plusieurs reprises sur un petit ensemble de gènes et de marques, ce qui suggère une raison biologique à la forte comorbidité des deux troubles.
Ce que cela signifie pour la prévention et le traitement futurs
En conclusion, la revue soutient que les changements épigénétiques pourraient devenir des biomarqueurs d’alerte précoce et des cibles pour des traitements de nouvelle génération. Des médicaments à action large qui effacent des marques épigénétiques ont déjà montré certains effets antidépresseurs chez l’animal, mais ils sont trop grossiers pour un usage clinique courant chez l’humain. De nouveaux outils — tels que des éditeurs d’épigénome basés sur CRISPR et des thérapies modulant des microARN ou des ARN longs spécifiques — pourraient un jour ajuster des gènes problématiques dans des cellules cérébrales particulières tout en épargnant les autres. Les auteurs mettent en garde que la plupart des données actuelles proviennent de rongeurs et de tissus cérébraux en masse, et que la biologie humaine est plus complexe. Néanmoins, en révélant comment drogues addictives et dépression s’inscrivent sur le même « cahier » moléculaire, ce travail offre une voie prometteuse vers des thérapies plus personnalisées et durables.
Citation: Zhang, W., Xu, M., Wang, C. et al. Addictive drug abuse and depression-a focus on epigenetics. Commun Biol 9, 297 (2026). https://doi.org/10.1038/s42003-026-09705-9
Mots-clés: addiction et dépression, épigénétique, abus de drogues, méthylation de l’ADN, ARN non codants