Clear Sky Science · fr
Med13 participe à la migration radiale et à la projection controlatérale des neurones corticaux via PlxnA4
Comment un seul gène aide à construire le cerveau pensant
Les cerveaux ne se contentent pas de croître ; ils se construisent, cellule par cellule, en couches et en circuits précisément organisés. Cette étude explore comment un gène, nommé Med13, aide les jeunes cellules corticales à se déplacer au bon endroit et à se connecter entre les deux hémisphères. Parce que des erreurs subtiles dans ce processus de construction sont de plus en plus associées à des affections comme l’autisme et la déficience intellectuelle, comprendre Med13 offre une fenêtre sur la manière dont le développement précoce du cerveau peut mal tourner.
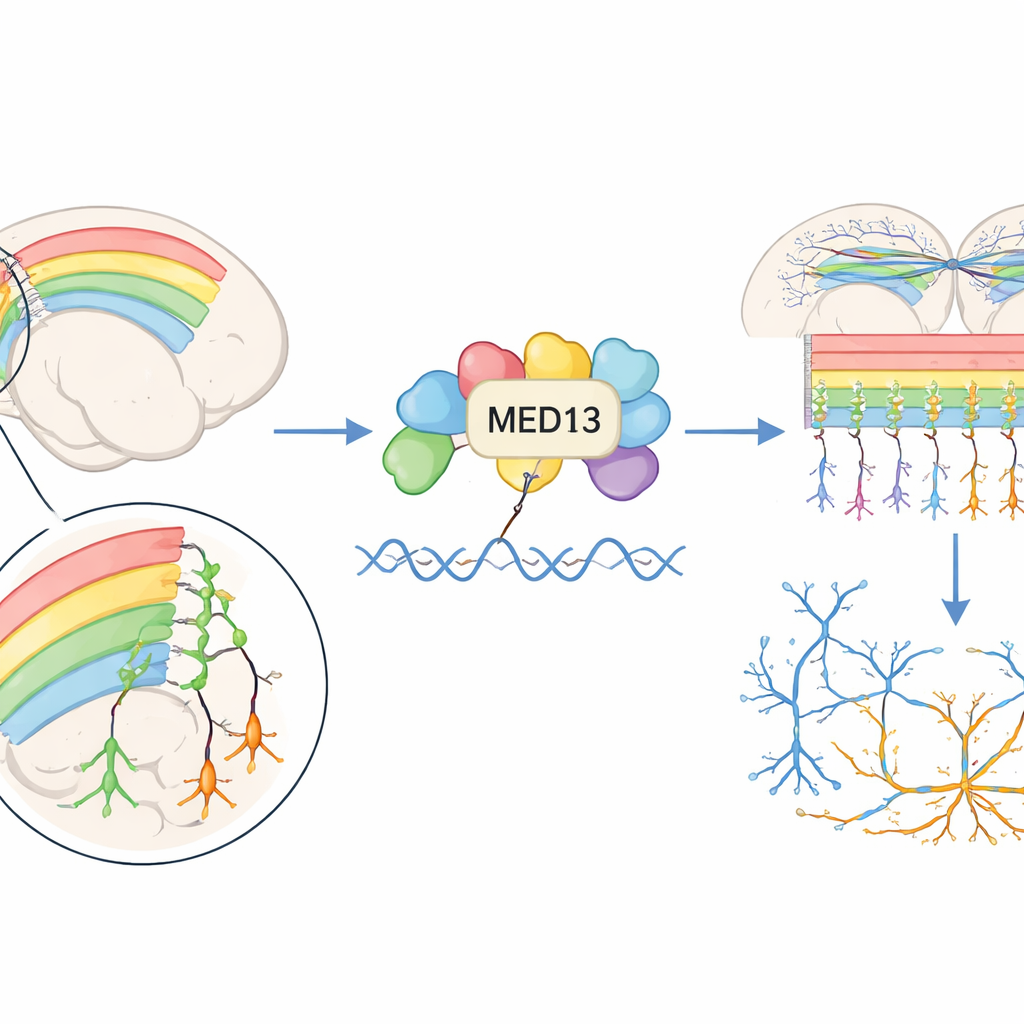
Construire le « quartier » à six couches du cerveau
Le cortex cérébral, la couche extérieure plissée du cerveau, est organisé en six couches de neurones qui se forment durant la vie embryonnaire. Les neurones nouvellement nés se forment profondément dans le cerveau puis migrent vers l’extérieur selon une séquence « de l’intérieur vers l’extérieur » pour former ces couches. Les auteurs ont d’abord cherché où et quand Med13 est actif au cours de ce processus. Chez l’embryon de souris, Med13 était présent à des niveaux élevés dans les régions où les cellules souches neurales se divisent et où les jeunes neurones sont en mouvement, en particulier autour d’un point clé de la gestation médiane quand de nombreux neurones corticaux sont générés. Med13 était présent à la fois dans les cellules précurseurs en division et dans les neurones en maturation, ce qui suggère qu’il participe largement à la formation du cortex.
Quand les neurones perdent leur chemin
Pour tester ce que Med13 accomplit réellement, l’équipe a réduit sélectivement son expression chez des neurones corticaux en développement de souris en utilisant une technique qui introduit de l’ADN sur mesure dans le cerveau fœtal. Les neurones marqués privés de Med13 ont été suivis au fil du temps. Par rapport aux neurones témoins, de nombreuses cellules déficientes en Med13 se sont arrêtées en cours de route au lieu d’atteindre les couches corticales supérieures où elles doivent se trouver. Même plusieurs jours après la naissance, une grande fraction restait dispersée dans les tissus plus profonds ou dans la matière blanche sous le cortex. Ces cellules mal placées présentaient aussi des signes d’immaturation : certaines n’exprimaient pas les marqueurs typiques des neurones de couche supérieure pleinement développés, sans pour autant se transformer en d’autres types cellulaires comme les neurones de couches inférieures ou les cellules gliales. Cela indique que Med13 est nécessaire non seulement pour que les neurones atteignent leur destination, mais aussi pour qu’ils adoptent pleinement leur identité correcte.
Des ponts brisés entre les hémisphères cérébraux
Le bon fonctionnement du cerveau dépend de connexions à longue distance entre neurones, y compris des fibres qui croisent la ligne médiane via le corps calleux pour relier les hémisphères gauche et droit. Les chercheurs ont constaté que les neurones dépourvus de Med13 projectionnaient beaucoup moins vers le côté opposé du cerveau. Moins d’axones pénétraient dans la région adéquate du cortex controlatéral, et ce déficit s’accentuait au fur et à mesure du développement. Parallèlement, les « arbres » dendritiques qui reçoivent les signaux étaient sensiblement plus simples : les neurones déficients en Med13 présentaient moins de branches et une longueur dendritique totale réduite. Ensemble, ces changements désignent Med13 comme un organisateur clé à la fois de l’emplacement des neurones et de la richesse de leurs connexions.
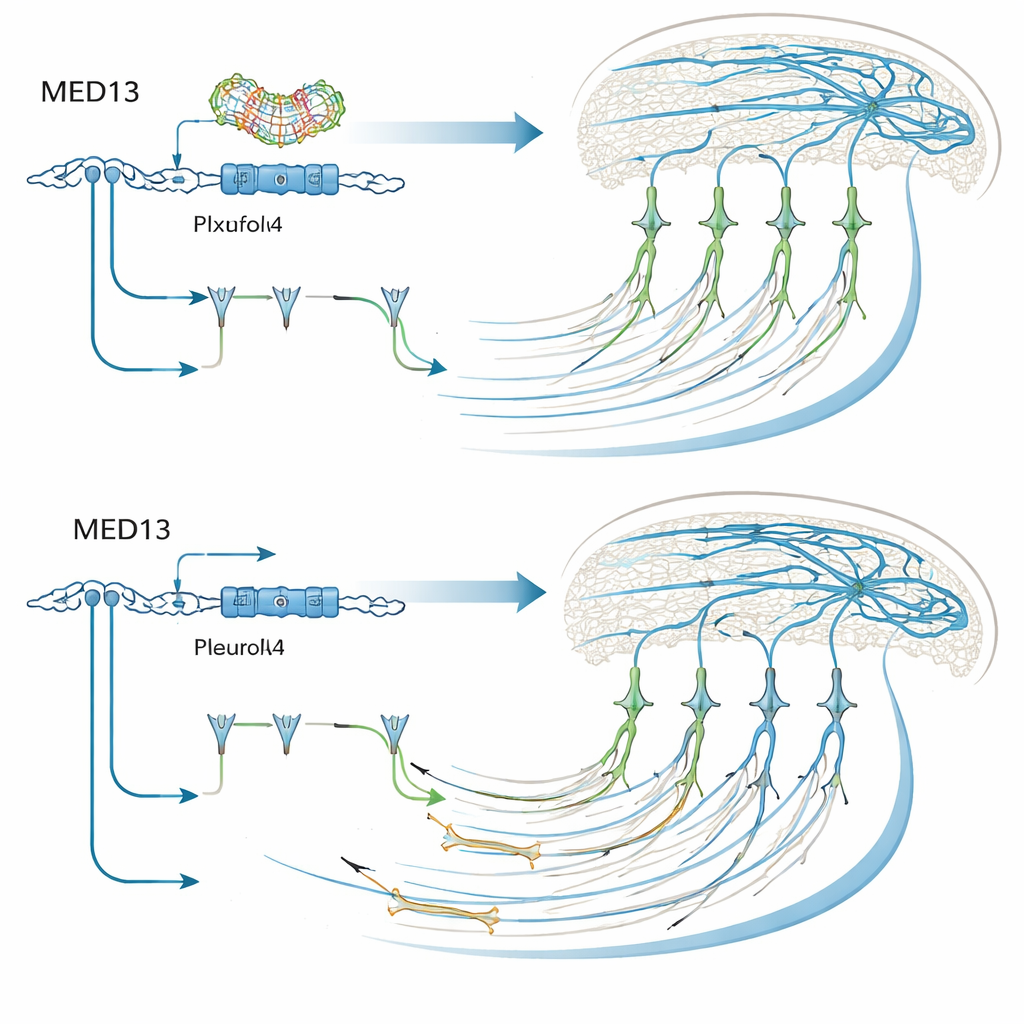
Du contrôle génétique aux signaux de guidage
Med13 fait partie d’un grand complexe protéique qui contrôle l’activation ou la répression de nombreux autres gènes ; les auteurs ont donc cherché ensuite des acteurs en aval susceptibles d’expliquer ses effets. En utilisant des cellules humaines de type nerveux génétiquement privées de MED13, ils ont catalogué des milliers de protéines et identifié plus d’une centaine dont les niveaux étaient modifiés. Nombre d’entre elles interviennent dans la morphologie neuronale, le mouvement et le développement cortical, et plusieurs chevauchent des gènes de risque connus pour des troubles du neurodéveloppement. Un élément a particulièrement retenu l’attention : PlxnA4, un récepteur qui aide les neurones à répondre aux signaux de guidage pendant leur migration et l’allongement des axones. Les niveaux de PlxnA4 chutaient lorsque MED13 faisait défaut, aussi bien dans des cellules humaines en culture que dans des neurones de souris avec Med13 réduit. De manière remarquable, forcer la surexpression de PlxnA4 chez les neurones pouvait en grande partie réparer leurs problèmes de migration et restaurer une bonne partie de leur projection callosale, même lorsque Med13 était supprimé. En revanche, cela ne corrigeait pas l’architecture dendritique simplifiée, ce qui implique que Med13 agit aussi via d’autres cibles pour façonner les ramifications neuronales.
Quelles implications pour les troubles cérébraux
Ensemble, ces résultats montrent que Med13 aide les jeunes neurones corticaux à se positionner dans les couches appropriées et à établir des connexions longue distance, en partie en maintenant le récepteur de guidage PlxnA4. Lorsque Med13 est perturbé, les neurones se placent mal, sous-développent leurs branches et envoient moins de fibres à travers le corps calleux — autant de changements qui font écho à des altérations observées dans certains troubles du neurodéveloppement. Bien que de nombreux autres gènes et signaux soient clairement impliqués, positionner Med13 comme régulateur central offre une image plus nette de la façon dont des altérations génétiques précoces peuvent se propager pour modifier le câblage cérébral et, en fin de compte, le comportement.
Citation: Li, ZX., Tu, SX., Li, YW. et al. Med13 is involved in the radial migration and contralateral projection of cortical neurons via PlxnA4. Commun Biol 9, 394 (2026). https://doi.org/10.1038/s42003-026-09704-w
Mots-clés: développement cortical, migration neuronale, corps calleux, troubles du neurodéveloppement, régulation génétique