Clear Sky Science · fr
Hétérogénéité entre les neurones VIP et GRP sous-tend la signalisation des récepteurs AVP dans le noyau suprachiasmatique de la souris
Pourquoi notre horloge biologique est si difficile à réinitialiser
Quiconque a souffert après un long vol ou a dû affronter des nuits de travail sait que notre horloge interne n’aime pas les changements soudains d’emploi du temps. Cet article pose une question très précise au cœur de ce problème : à l’intérieur de l’horloge maîtresse du cerveau, pourquoi certaines cellules nerveuses perçoivent-elles fortement un signal temporel alors que leurs voisines l’ignorent pour la plupart ? En suivant un signal chimique unique à travers ce minuscule circuit d’horloge chez la souris, les auteurs mettent au jour un sous-groupe de cellules qui contribuent à déterminer la rigidité de notre horloge biologique face au « jet lag ». 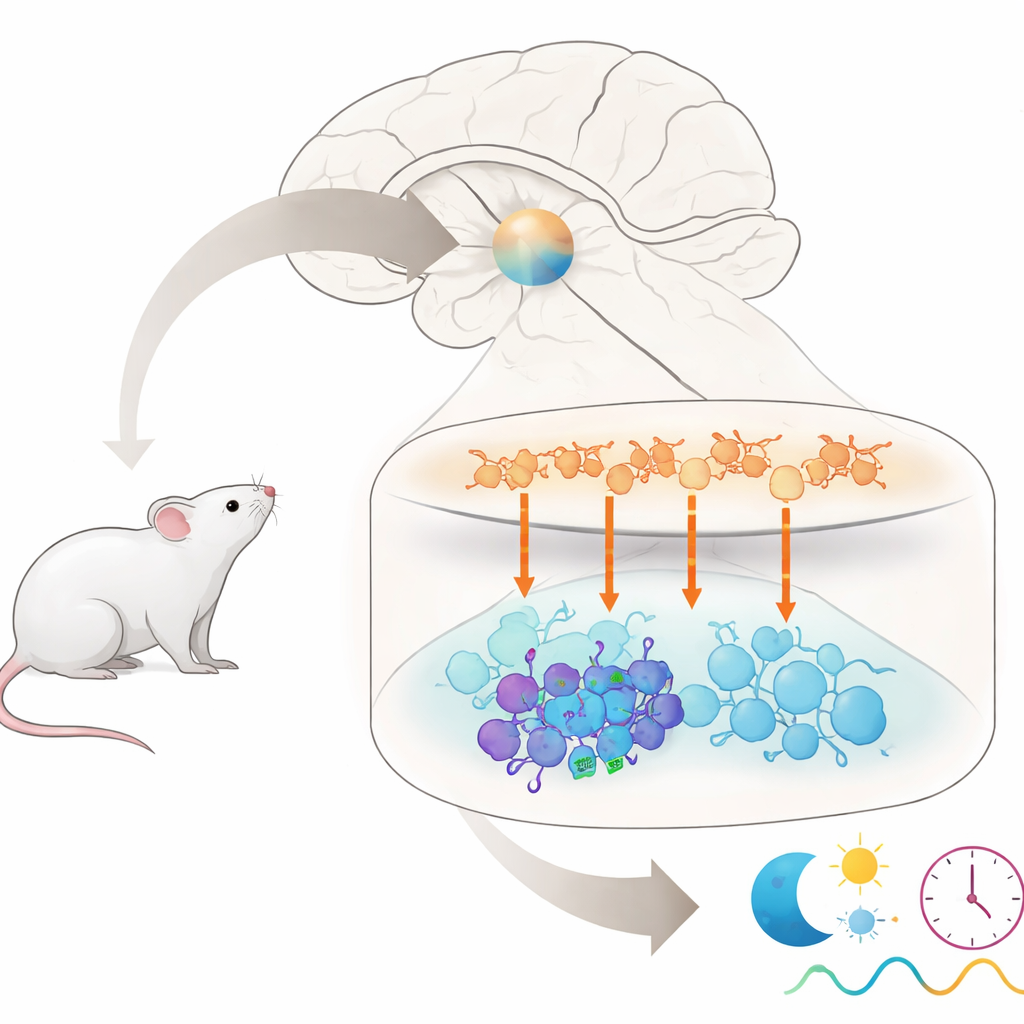
Une petite horloge aux nombreux acteurs
L’horloge maîtresse chez les mammifères se situe dans une petite région du cerveau appelée noyau suprachiasmatique, ou NSC. Bien qu’il ne contienne qu’environ 20 000 neurones, il est composé de plusieurs groupes distincts qui communiquent entre eux par différents messagers chimiques. Les cellules de la région supérieure dite « coque » libèrent principalement un messager appelé arginine vasopressine (AVP), tandis que les cellules de la région inférieure dite « cœur » libèrent souvent d’autres messagers, notamment le peptide intestinal vasoactif (VIP) et le peptide libérant la gastrine (GRP). Ensemble, ces groupes doivent rester synchrones pour générer les rythmes de 24 heures qui régulent le sommeil, la sécrétion hormonale et de nombreuses autres fonctions corporelles. Mais quelles cellules exactes du cœur écoutent les signaux des cellules AVP de la coque restait incertain.
Suivre les connexions de l’émetteur au récepteur
Les chercheurs ont d’abord cartographié comment les cellules AVP de la coque se connectent physiquement aux cellules VIP et GRP du cœur. Ils ont utilisé un virus pour marquer les fibres sortantes et les points de contact possibles des neurones AVP chez la souris, puis coloré des coupes de cerveau pour voir où ces fibres terminaient. Ils ont constaté que les fibres AVP formaient des sites d’apposition apparents sur les cellules VIP et GRP, mais en proportions différentes : environ un quart des cellules VIP et plus de la moitié des cellules GRP présentaient ces appositions. Cela montrait que les neurones AVP atteignent les deux types de cellules du cœur, sans pour autant révéler lesquelles répondent effectivement au signal. Pour tester cela, l’équipe a utilisé l’optogénétique — activant les neurones AVP par lumière bleue — et recherché la protéine c‑Fos, un marqueur d’activation cellulaire, dans les neurones VIP et GRP.
Un petit sous-groupe VIP qui « entend » vraiment l’AVP
Lorsque les neurones AVP étaient stimulés par la lumière, de nombreuses cellules AVP elles-mêmes exprimaient c‑Fos, comme prévu. De manière importante, un petit sous-ensemble de cellules VIP du cœur montrait également une activation de c‑Fos, bien qu’elles n’exprimaient pas directement la protéine sensible à la lumière. Cela indiquait qu’elles étaient activées indirectement par l’entrée AVP. En revanche, les cellules GRP montraient rarement du c‑Fos, malgré la présence d’appositions AVP. Les auteurs ont alors recherché le message génétique du récepteur AVP connu sous le nom de V1a dans ces populations en utilisant des méthodes d’imagerie ARN sensibles. Ils ont découvert que V1a était présent seulement dans une minorité de cellules VIP et à peine détectable dans les cellules GRP. Ainsi, parmi les nombreux neurones VIP, un petit sous-groupe V1a‑positif semble spécialement accordé pour recevoir et répondre aux signaux AVP, tandis que la plupart des neurones GRP ne le sont pas. 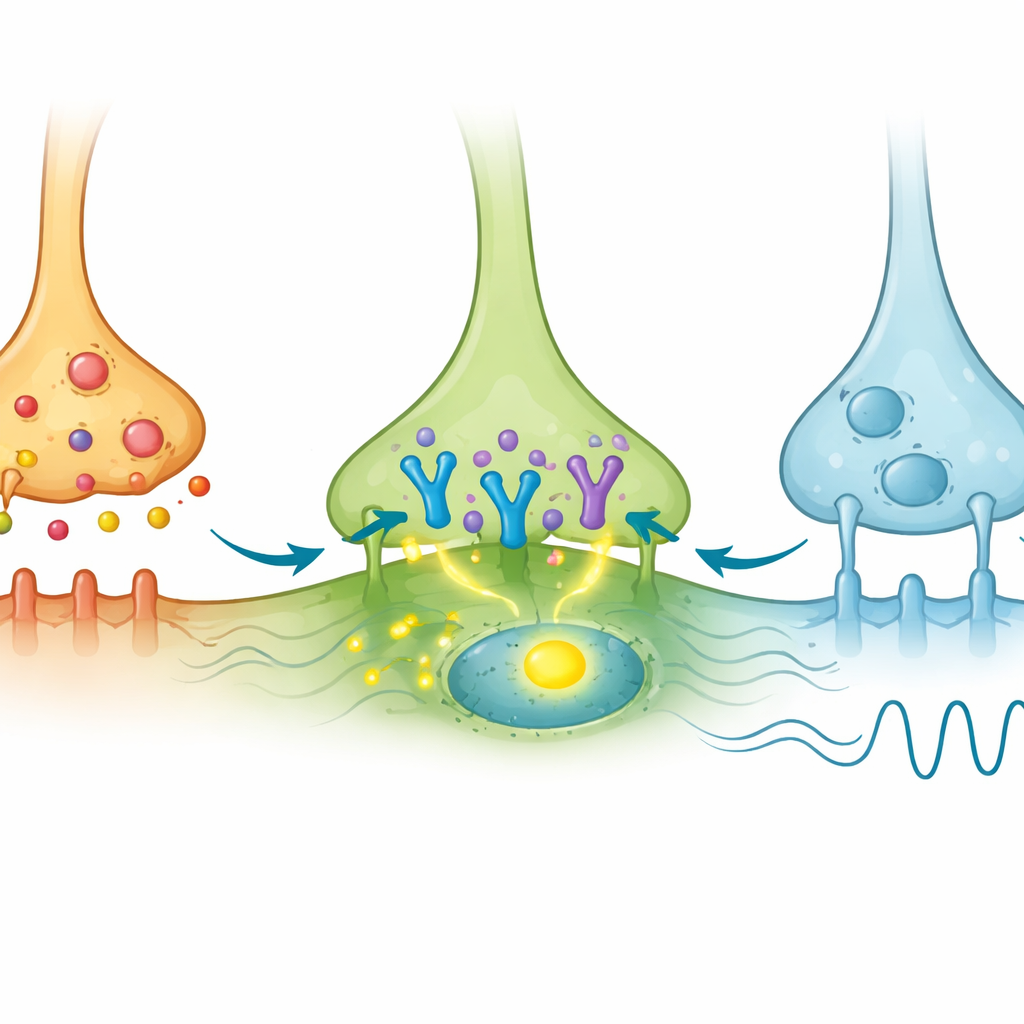
Comment un petit groupe cellulaire influence la récupération après jet lag
Pour sonder la fonction de ces neurones VIP porteurs de V1a, les chercheurs ont créé des souris dont le récepteur V1a était supprimé uniquement dans les cellules VIP. Ces animaux conservaient une durée de rythme quotidien normale en obscurité constante, montrant que ce récepteur dans les neurones VIP n’est pas nécessaire pour régler la cadence de base de l’horloge. Cependant, lorsque le cycle lumière‑obscurité a été avancé ou retardé soudainement de huit heures pour imiter le décalage horaire, les souris modifiées ont ajusté leurs schémas d’activité plus rapidement que leurs congénères normaux, en particulier après des avances et chez les mâles. Dans d’autres expériences, la délétion de V1a à l’échelle du cerveau ou spécifiquement dans le NSC avait produit un comportement similaire de « résistance au jet lag ». Les nouveaux résultats suggèrent donc qu’un groupe étonnamment petit de neurones VIP portant les récepteurs V1a peut exercer une influence disproportionnée sur la rigidité ou la flexibilité de l’horloge globale.
Ce que cela signifie pour notre perception du temps
Concrètement, cette étude montre que, au sein de l’horloge centrale du cerveau, les neurones producteurs d’AVP jouent le rôle d’horlogers dans un niveau supérieur, envoyant des signaux via les récepteurs V1a à un ensemble restreint de neurones VIP du niveau inférieur. Ces quelques cellules VIP aident le réseau entier à résister aux changements brusques du cycle lumière‑obscurité, ralentissant la réinitialisation de l’horloge après un décalage. La suppression de leur récepteur sensible à l’AVP rend le système plus enclin à se décaler, facilitant les ajustements de type jet lag chez la souris. En cartographiant cette diversité cachée parmi les neurones de l’horloge, ce travail offre un schéma de connectivité plus détaillé de la façon dont notre sens interne du temps est stabilisé — et suggère que, un jour, cibler sélectivement des voies similaires chez l’humain pourrait aider à gérer le décalage horaire ou d’autres troubles des rythmes.
Citation: Zhou, H., Moriyasu, D., Hsiao, SW. et al. Heterogeneity between VIP and GRP neurons underlies AVP receptor signaling in the mouse suprachiasmatic nucleus. Commun Biol 9, 414 (2026). https://doi.org/10.1038/s42003-026-09694-9
Mots-clés: horloge circadienne, noyau suprachiasmatique, signalisation de la vasopressine, neurones VIP, décalage horaire