Clear Sky Science · fr
Caractéristiques pathologiques des variants de SARS-CoV-2 et réponses immunitaires induites dans un modèle de macaque pour la COVID-19
Pourquoi cette étude compte dans la vie quotidienne
Le coronavirus responsable de la COVID-19 n’a cessé d’évoluer, entraînant des vagues dominées par les variants Alpha, Delta, Omicron et d’autres. De nombreuses personnes ont contracté la COVID-19 à plusieurs reprises, même après vaccination ou infection antérieure. Cette étude a utilisé des singes présentant une maladie similaire à la COVID-19 pour poser deux questions directement pertinentes pour l’humain : comment les différents variants se comportent-ils à l’intérieur du corps, et comment une première rencontre avec le virus façonne-t-elle la réponse immunitaire aux variants ultérieurs ?
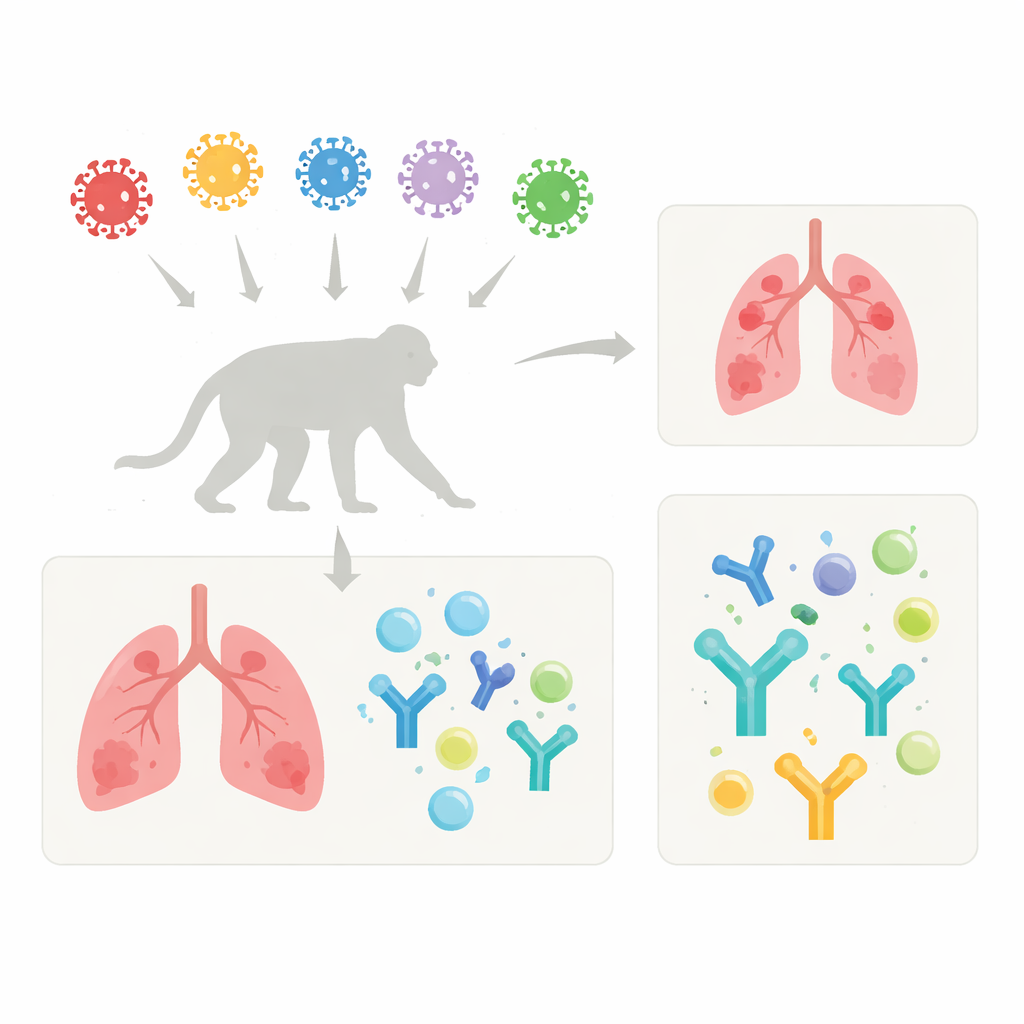
Suivre les variants à travers le corps
Les chercheurs ont infecté des macaques cynomolgus, un type de singe dont les symptômes de COVID-19 ressemblent à une forme légère chez l’humain, avec la souche originale de Wuhan et six variants majeurs : Alpha, Beta, Gamma, Delta, et Omicron BA.1 et BA.2. Tous les animaux ont reçu la même dose directement dans la trachée afin de comparer équitablement les infections. Les singes n’ont présenté que des signes bénins et temporaires de maladie, comme de courtes fièvres et des variations d’appétit, leur poids étant resté stable. Un marqueur sanguin de l’inflammation, la protéine C-réactive, a augmenté après infection mais avait tendance à être plus bas avec Omicron, ce qui laisse supposer que ces variants plus récents déclenchent moins d’inflammation systémique que les premiers.
Vitesse de réplication virale et atteinte pulmonaire
L’équipe a réalisé des prélèvements répétés du nez et de la gorge des macaques pour suivre la quantité de virus excrétée et la durée d’excrétion. Le variant Delta s’est distingué : il atteignait les niveaux viraux les plus élevés et persistait le plus longtemps, en particulier dans les prélèvements de gorge qui reflètent la réplication dans les voies aériennes inférieures. Omicron BA.1 et BA.2, en revanche, étaient à peine détectables dans les prélèvements nasaux et présentaient une réplication globale beaucoup plus faible, ce qui corrobore l’idée qu’Omicron est moins adapté à infecter le tissu pulmonaire profond. Les scanners thoraciques (CT) ont confirmé ce schéma. Les variants antérieurs, en particulier Gamma et Delta, ont souvent produit des zones nettes de pneumonie, tandis que les infections par Omicron entraînaient des modifications pulmonaires plus pâles et plus limitées, cohérentes avec la maladie plus bénigne généralement observée chez l’humain.
Secondes infections et pneumonie surprenante
Pour reproduire les réinfections du monde réel, certains singes ont été réexposés au même variant ou à un variant différent environ trois mois après la première infection. Lorsque Delta a été utilisé pour la seconde exposition, tous les animaux sont redevenus brièvement positifs à la PCR, montrant que la réinfection pouvait survenir, mais aucun n’a développé de pneumonie ; l’immunité préalable semblait limiter les lésions même si elle n’empêchait pas totalement la présence virale. Omicron s’est comporté différemment. Seuls environ la moitié des singes sont devenus PCR-positifs lors d’une réexposition à Omicron, et pourtant chaque animal qui a développé une pneumonie après le second épisode avait reçu une souche Omicron pour cette seconde exposition. Dans ces cas, peu ou pas de virus vivant n’a été retrouvé dans les tissus, ce qui suggère que l’inflammation pulmonaire a été déterminée non seulement par la quantité de virus présente mais aussi par la manière dont le système immunitaire avait été préalablement amorcé.
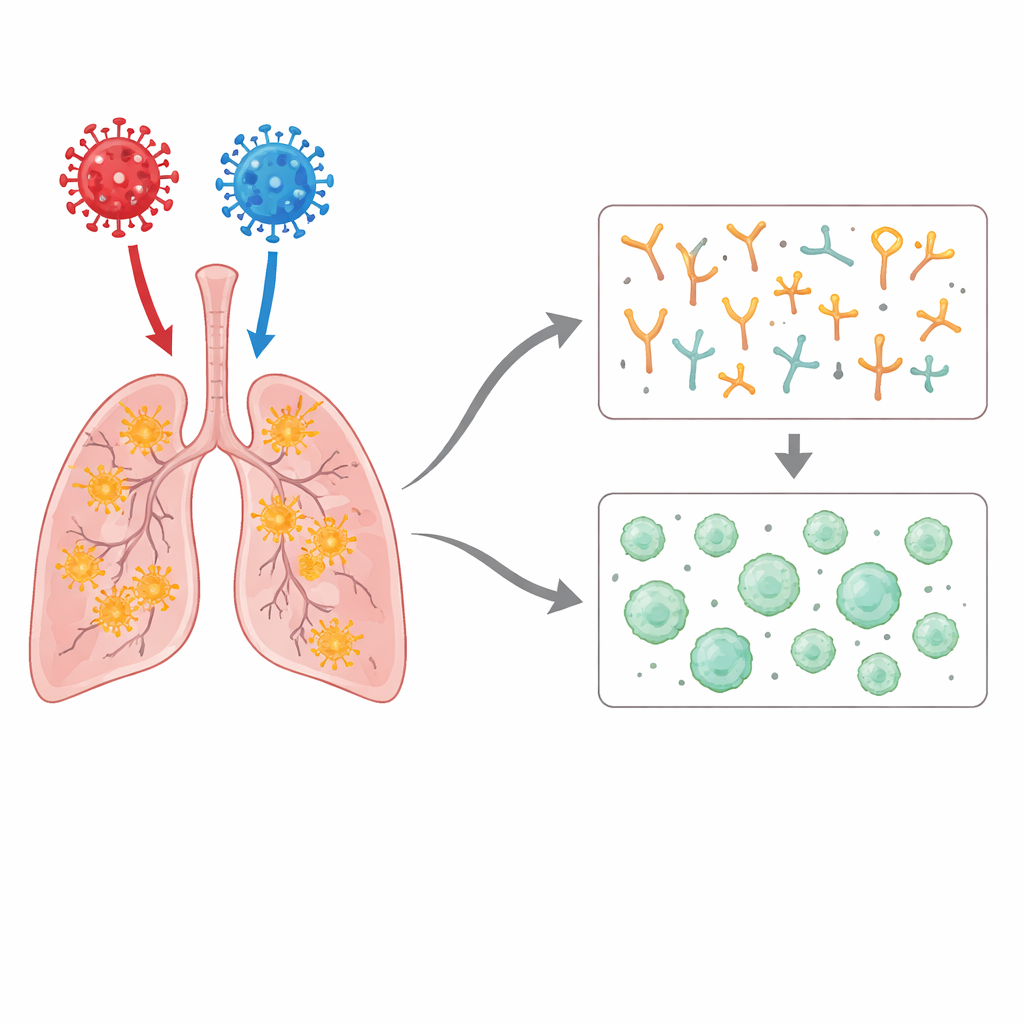
Mémoire immunitaire et attraction de la première souche
Les scientifiques ont examiné de près les anticorps et les lymphocytes T, les deux principaux volets de l’immunité adaptative. Après une infection par Wuhan ou Delta, les singes ont produit des anticorps puissants qui reconnaissaient la souche originale et plusieurs variants précoces. Cependant, même lorsque l’infection était causée par Omicron, les anticorps se liant fortement à la région clé de surface d’Omicron étaient faibles et lents à apparaître. Au lieu de cela, le système immunitaire favorisait à plusieurs reprises des réponses dirigées contre la protéine spike de type Wuhan, un schéma connu sous le nom de « premier péché antigénique », où la première version d’un virus rencontrée par l’organisme laisse une empreinte durable sur les réponses ultérieures. Les réactions des lymphocytes T à Omicron étaient également généralement plus faibles que celles observées pour les variants antérieurs, surtout après une seule infection par Omicron, renforçant l’idée d’un variant qui se propage bien en étant moins inflammatoire et moins visible par le système immunitaire.
Ce que cela signifie pour les vaccins et la protection future
En termes simples, l’étude montre que tous les variants de la COVID-19 ne sont pas équivalents à l’intérieur du corps. Delta se réplique vigoureusement et peut causer une atteinte pulmonaire importante, mais il induit aussi une immunité robuste et croisée. Omicron se réplique mal dans les poumons et provoque une maladie plus bénigne, et pourtant il enseigne mal le système immunitaire, surtout lorsque des expositions antérieures à des virus de type Wuhan continuent d’orienter les réponses d’anticorps vers la souche originale. À long terme, cet ancrage immunologique et la faible immunogénicité d’Omicron peuvent aider à expliquer pourquoi les vagues d’Omicron et leurs sous-variants ont perduré. Ces résultats, issus d’un modèle de macaque soigneusement contrôlé, soutiennent des stratégies vaccinales axées sur la souche épidémique la plus actuelle tout en reconnaissant que la majorité de la mémoire immunitaire mondiale renvoie encore à la première version du virus.
Citation: Urano, E., Okamura, T., Higuchi, M. et al. Pathological characteristics of SARS-CoV-2 variants and immune responses induced in a COVID-19 macaque model. Commun Biol 9, 426 (2026). https://doi.org/10.1038/s42003-026-09684-x
Mots-clés: Variants de SARS-CoV-2, Immunité Omicron, Réinfection COVID-19, premier péché antigénique, modèle de macaque