Clear Sky Science · fr
La malonylation des lysines régule la motilité des spermatozoïdes humains
Pourquoi le mouvement des spermatozoïdes compte
Pour de nombreux couples confrontés à une infertilité inexpliquée, un problème caché clé est que les spermatozoïdes ne nagent tout simplement pas assez bien pour atteindre et féconder l’ovule. Cette étude explore une « étiquette » chimique subtile sur les protéines spermatiques — appelée malonylation des lysines — qui semble agir comme un frein invisible sur leur mouvement. En dévoilant comment cette marque altère l’approvisionnement énergétique des spermatozoïdes et leurs signaux internes, le travail pointe vers de nouvelles voies pour diagnostiquer et potentiellement traiter une forme courante d’infertilité masculine liée à une faible motilité des spermatozoïdes.
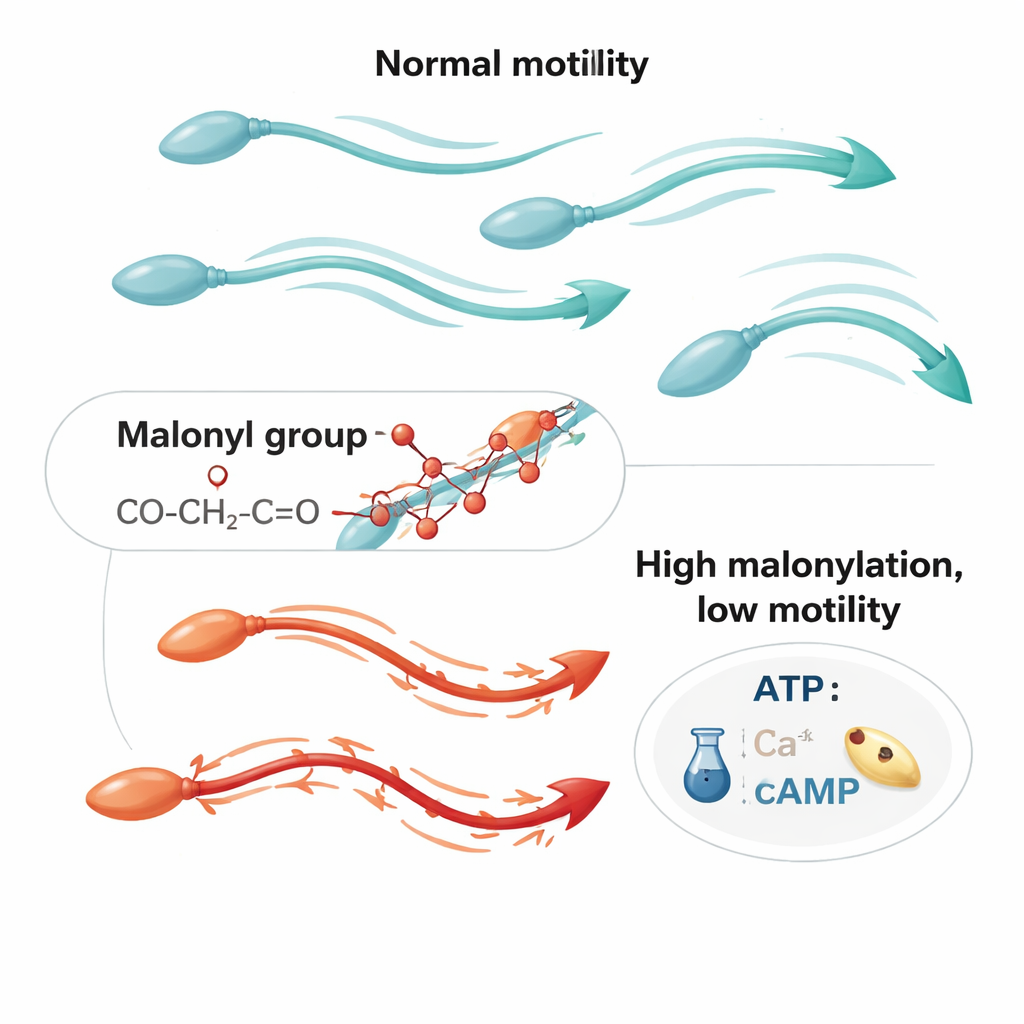
Une nouvelle étiquette chimique sur les protéines spermatiques
Les protéines de nos cellules sont souvent modifiées après leur synthèse, en acquérant de petits groupes chimiques qui peuvent activer ou désactiver leur activité. Une de ces modifications, la malonylation des lysines, n’a été découverte qu’en 2011 et a été reliée au métabolisme énergétique dans de nombreux types cellulaires. Les auteurs avaient précédemment montré que les spermatozoïdes humains portent de nombreuses protéines malonylées, mais il était incertain ce que cela signifiait pour la fertilité. Dans la nouvelle étude, ils ont cartographié les lieux d’apparition de cette marque dans les spermatozoïdes et ont constaté qu’elle se concentre dans la queue — la longue structure en fouet dont le battement rythmique propulse le mouvement vers l’avant. À l’aide de tests biochimiques et de microscopie haute résolution, ils ont montré que les protéines malonylées sont particulièrement abondantes dans les mitochondries de la queue et le fluide qui les entoure, des sites clés pour la production d’énergie et le contrôle du mouvement.
Qui pose et qui enlève le frein
L’équipe s’est ensuite demandé quelles molécules installent et retirent cette marque de malonylation dans les spermatozoïdes humains. Ils ont trouvé des preuves qu’une enzyme connue sous le nom de P300 agit comme un « écrivain », aidant à transférer des groupes malonyl sur des résidus de lysine, tandis qu’une autre enzyme, SIRT5, sert d’« effaceur » qui les retire. Quand ils ont bloqué SIRT5 avec un inhibiteur chimique, la malonylation globale augmentait ; quand ils ont inhibé P300, la malonylation diminuait. Ils ont également montré que le malonate de sodium, une petite molécule absorbée par les spermatozoïdes et convertie en malonyl-CoA, renforçait la malonylation sans perturber d’autres marques chimiques similaires. Ensemble, ces résultats décrivent un système régulateur dans lequel le malonyl-CoA fournit la marque, P300 l’attache et SIRT5 l’enlève — ajustant finement les protéines de la queue spermique qui contrôlent le mouvement.
Plus de malonylation dans les spermatozoïdes peu mobiles
Pour savoir si cette chimie a rapport à l’infertilité réelle, les chercheurs ont comparé des spermatozoïdes d’hommes ayant des profils de sperme normaux à ceux diagnostiqués avec une asthénospermie, une condition définie par une faible motilité progressive. Les spermatozoïdes du groupe asthénospermique présentaient des niveaux significativement plus élevés de malonylation des lysines et des niveaux plus faibles de SIRT5. Dans l’ensemble des échantillons, une malonylation plus importante corrélait fortement avec une moins bonne nage en avant et avec une réduction de l’ATP cellulaire, la principale monnaie énergétique. Dans un sous-groupe d’hommes présentant une malonylation particulièrement élevée, les spermatozoïdes montraient une glycolyse nettement affaiblie — la voie de la combustion du sucre qui fournit une grande partie du carburant pour le mouvement des spermatozoïdes humains. Ces schémas suggèrent qu’une malonylation excessive est liée à la fois à une production d’énergie déficiente et à une performance de nage réduite.
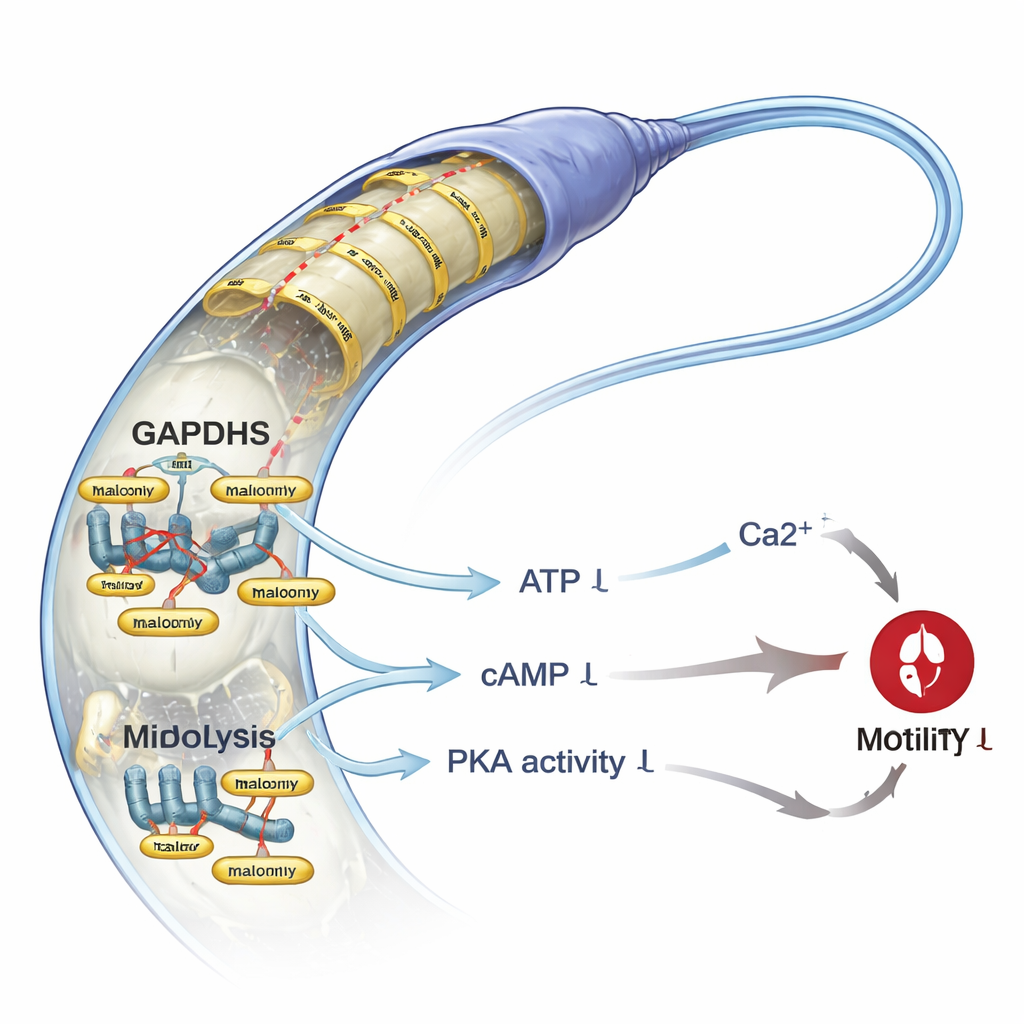
Augmenter expérimentalement le frein
Les scientifiques ont ensuite cherché ce qui se passe s’ils augmentent délibérément la malonylation dans des spermatozoïdes par ailleurs sains. Le traitement d’échantillons d’hommes ayant des paramètres spermatiques normaux avec du malonate de sodium a augmenté les niveaux de malonylation sans tuer les cellules. Cependant, cela a réduit de manière significative la motilité totale et progressive et a rendu plus difficile pour les spermatozoïdes de se frayer un chemin à travers un milieu visqueux mimant le tractus reproducteur féminin. Des tests mécanistes ont révélé pourquoi : les spermatozoïdes traités au malonate de sodium présentaient une production glycolytique plus faible, moins d’ATP et des quantités réduites d’AMPc, un messager qui active l’enzyme clé PKA. L’activité de PKA a chuté, tout comme la phosphorylation de protéines en aval connues pour soutenir la motilité. Parallèlement, les niveaux de calcium intracellulaire des spermatozoïdes ont diminué d’environ moitié, bien que le principal canal calcique des spermatozoïdes, CatSper, n’ait pas été directement affecté. Cette combinaison — moins d’énergie, des signaux affaiblis et une baisse du calcium — offre une explication cohérente de la perte de motilité observée.
Des marques moléculaires à la fertilité masculine
En regroupant tous les résultats, l’étude propose que la malonylation des lysines agit comme un régulateur négatif de la motilité des spermatozoïdes humains. Quand les niveaux de malonylation augmentent — parce que SIRT5 est faible, que le malonyl-CoA est élevé ou que des voies associées sont perturbées — des protéines clés qui pilotent la glycolyse et la gestion du calcium, telles que GAPDHS et VDAC3, deviennent excessivement marquées. Cela atténue la production d’énergie et les cascades de signalisation critiques dans la queue spermique, entraînant un mouvement ralenti et une capacité réduite à pénétrer des fluides denses. Pour le lecteur non spécialiste, le message est que les spermatozoïdes n’ont pas seulement besoin d’un nombre suffisant ; ils ont aussi besoin de systèmes de contrôle chimique finement réglés pour alimenter leur nage. Les perturbations d’une petite marque réversible comme la malonylation peuvent contribuer à une infertilité masculine autrement inexpliquée et pourraient à terme offrir de nouveaux biomarqueurs ou cibles thérapeutiques visant à restaurer la vigueur des spermatozoïdes.
Citation: Cheng, Y., Tian, Y., Chen, H. et al. Lysine malonylation regulates human sperm motility. Commun Biol 9, 178 (2026). https://doi.org/10.1038/s42003-026-09683-y
Mots-clés: motilité des spermatozoïdes, infertilité masculine, modification post-traductionnelle, malonylation des lysines, métabolisme énergétique